Lynelle R. Johnson DVM, PhD, Dip ACVIM (iekšējā medicīna)
Kalifornijas Universitāte, ASV
Pamatnoteikumi
Visbiežāk trahejas kolapss notiek mazo šķirņu, pusmūža suņiem ar lieko ķermeņa masu. Dažreiz šī patoloģija rodas jauniem lieliem suņiem.
Trahejas sabrukums visbiežāk notiek dorsoventrālajā virzienā. Pirms tam notiek trahejas skrimšļa gredzenu vājināšanās un retināšana, kā rezultātā rodas prolapss aizmugurējā siena traheju savā lūmenā.
Sakļaut dzemdes kakla reģions traheja visbiežāk rodas iedvesmas laikā, un krūšu kurvja trahejas sabrukums notiek izelpas laikā.
Labākais veids, kā diagnosticēt, ir vizuāla pārbaude elpceļi. Ar bronhoskopiju var iegūt gaisa paraugus no dziļajām elpceļu daļām.
Trahejas sabrukums ir trahejas skrimšļa gredzenu neatgriezeniskas patoloģijas sekas. Ārstēšana ietver uzturēšanu labā stāvoklī augšējie un apakšējie elpceļi.
Suņiem ar aizdusu un smagu klepu, kas saistīts ar dzemdes kakla trahejas kolapsu, ir indicēta ķirurģiska iejaukšanās un trahejas daļas nomaiņa ar bojātiem skrimšļa gredzeniem.
Ievads
Trahejas sabrukums veterinārajā praksē ir diezgan izplatīts. Tas izraisa klepu un elpceļu obstrukciju mazo šķirņu suņiem. Dažreiz šī patoloģija rodas jauniem suņiem. lielas šķirnes. Lai gan trahejas sabrukuma cēloņi nav pilnībā zināmi, tiek uzskatīts, ka tas šī patoloģija ir iedzimtu anomāliju, jo īpaši hondroģenēzes ģenētisku traucējumu, sekas. Trahejas sabrukums bieži attīstās sakarā ar hroniskas slimības elpceļi, skrimšļa deģenerācija, traumas un trahejas muskuļa inervācijas trūkums (musculus trachealis dorsatis). Visbiežāk trahejas kolapss attīstās dorsoventrālā virzienā ar vājās muguras trahejas membrānas prolapsu trahejas lūmenā.
Atpazīt trahejas sabrukumu klīniskie apstākļi pietiekami vienkārši. Dzīvnieka apgrūtinātas elpošanas pakāpes noteikšana, faktori, kas veicina pastiprinātu klepu, un savlaicīga iejaukšanās palīdz izvēlēties pacientam atbilstošu ārstēšanu, kas uzlabo slimības iznākumu un samazina smagu komplikāciju iespējamību.
Fizioloģija un patofizioloģija
Trahejas sienas ir pastiprinātas ar 30-45 hialīna skrimšļa gredzeniem. Skrimšļaino struktūru galus nostiprina trahejas muguras pusē, veidojot pilnīgu gredzenu (1. attēls). Trahejas gredzeni ir savienoti viens ar otru ar gredzenveida saitēm. Trahejas iekšpuse ir izklāta ar pseidostratificētu, ciliāru un kolonnu epitēliju. Augšējos elpceļos, epitēlija slānī, tiek atrastas Goblet šūnas, kas rada gļotas, kas pārklāj epitēliju. Šīs gļotas un epitēlija šūnu ciliārais aparāts ir daļa no mehānisma, kas aizsargā plaušas no bojājumiem.
Traheja ir unikāla struktūra: tās dzemdes kakla rajonā iekšējais spiediens atmosfēras, savukārt krūšu rajonā tas ir negatīvs (atbilst spiedienam iekšā pleiras dobums) (2.a attēls). Ieelpojot, krūtis paplašinās un diafragma virzās uz sāniem vēdera dobums. Tā rezultātā palielinās pleiras dobuma tilpums un samazinās spiediens tajā (26. attēls). Vilnis zems asinsspiediens pārnēsā pa elpceļiem, kā rezultātā gaiss nokļūst plaušās. Izelpojot, spiediens pleiras dobumā palielinās, un spiediena gradients izspiež gaisu no elpceļiem. Veseliem dzīvniekiem trahejas skrimšļa gredzeni pilnībā novērš būtiskas trahejas diametra izmaiņas elpošanas cikla fāzēs.
Suņiem ar trahejas kolapsu skrimšļa gredzeni zaudē savu elastību un zaudē spēju novērst trahejas diametra izmaiņas elpošanas laikā spiediena svārstību dēļ. Dažiem mazo šķirņu suņiem ar trahejas kolapsu ir nepietiekams hondrocītu skaits un hondroitīna sulfāta un kalcija satura samazināšanās elpceļu skrimšļos. Tiek uzskatīts, ka glikoproteīnu un glikozaminoglikānu trūkums izraisa ievērojamu saistītā ūdens daudzuma samazināšanos skrimšļa audos, izžūstot un retinot skrimšļus. Patoloģiskas izmaiņas, kas konstatēta elpceļu skrimšļos suņiem ar trahejas kolapsu, var būt saistīta gan ar traucētu hondroģenēzi, gan ar hialīna skrimšļa deģenerāciju. Nepietiekama hondrocītu skaita cēlonis var būt gan ģenētiski faktori, gan uztura novirzes.
Slimiem suņiem trahejas sabrukums notiek dažādas nodaļas traheja atkarībā no elpošanas cikla fāzes (2. attēls, b un c). Vājinātie skrimšļu gredzeni dzemdes kakla trahejā iedvesmas laikā zaudē spēju izturēt negatīvo spiedienu, tāpēc traheja sabrūk (sabrūk) dorsoventrālā virzienā. Ar atkārtotu vai pastāvīgu sabrukumu skrimšļa gredzeni deformējas, izstiepjot trahejas muguras sienu. Šī siena noliecas lūmenā, kairinot pretējo sienu, izraisot trahejas epitēlija bojājumus un iekaisumu. Iekaisuma dēļ palielinās gļotu sekrēcija un palielinās šūnu skaits, kas ražo gļotādas gļotas. Mukopurulentā sekrēta daudzums var būt tik liels, ka veidojas plēvīte, līdzīga tai, kāda veidojas ar difteriju. Tas viss izraisa pacienta klepu, traucē elpceļu ciliārā aparāta darbību un ievērojami palielina infekcijas risku.

1. attēls.
Normālas trahejas endoskopiskais attēls. Ir redzami C veida skrimšļveida gredzeni, kuru galus savieno muguras trahejas membrāna (šajā fotoattēlā- uz augšu). Asinsvadi ir redzami caur elpošanas epitēliju.
Daudziem slimiem suņiem kolaps skar ne tikai dzemdes kakla, bet arī krūšu kurvja traheju, galvenos bronhus un pat mazos elpceļus. Ar intensīvu izelpu vai klepu pleiras dobumā rodas pozitīvs spiediens un tiek pārnests uz elpceļiem. Tāpēc sabrūk krūšu kurvja reģioni elpceļi parasti rodas izelpas laikā (2. attēls, c). Nav zināms, vai suņiem ar trahejas kolapsu ir samazināts hondrocītu skaits krūšu kurvja trahejas skrimšļainajos gredzenos. Dažreiz suņiem ir arī vispārējs visa krūšu elpceļu sabrukums.
Slimības vēsture un simptomi
Visbiežāk trahejas sabrukums notiek mazos un punduru šķirnes: Čivava. Pomerānijas, rotaļu pūdeļi, Jorkšīras terjeri, Maltas suņi un mopši. Suņu vecums, kam pirmās slimības pazīmes parādās, svārstās no 1 gada līdz 15 gadiem. Tomēr slimība visbiežāk parādās pieaugušā vecumā. Dzimuma nosliece uz slimību nav noteikta. Trahejas sabrukums ir reti sastopams arī jauniem lielu šķirņu suņiem (piemēram, zelta retrīveriem vai labradoru retrīveriem).
Lielākajai daļai suņu ar sabrukušu traheju ilgstoši ir stiprs klepus. Kopumā mājdzīvnieku īpašnieki šo klepu raksturo kā “sausu”, “plaukstošu” un pakāpeniski pieaugošu klepu. Bieži īpašnieki norāda, ka viņu suņa klepus lēkmes sākas pēc ēšanas vai dzeršanas. Tā rezultātā dažiem suņiem sāk justies slikti, dzīvnieki var aizrīties ar pārtiku vai pat vemt. Dažos gadījumos šādi klepus lēkmes attīstās tik akūti, ka saimniekiem liekas, ka suns būtu nokļuvis trahejā. svešķermenis. Klepus pakāpeniski kļūst paroksizmāls, un to pavada sekundāri elpceļu bojājumi. Attīstās elpas trūkums, palielinās elpošana, samazinās fiziskā izturība. Kad slodze palielinās elpošanas sistēmas(piemēram, fiziskās aktivitātes dēļ, paaugstināta temperatūra vai mitrums vidi) pazīmes tiek novērotas elpošanas mazspēja. Bieži vien pēc intratraheālās intubācijas klīnisko simptomu smagums palielinās. Simptomu saasināšanos var izraisīt arī fiziskas aktivitātes vai asa apkakles vilkšana. Dzīvnieku īpašnieki, baidoties no sava mājdzīvnieka stāvokļa pasliktināšanās, bieži to ierobežo fiziskā aktivitāte. Tā rezultātā daudzi suņi iegūst liekais svars, un to izturību pret fiziskā aktivitāte. Pēc autora novērojumiem, tieši suņiem ar lieko svaru ir īpaši liela slodze uz elpošanas sistēmu. Dzīvniekiem ar aptaukošanos trahejas kolapsa klīnisko simptomu smagums (īpaši klepus) var būt ļoti izteikts. Tomēr saskaņā ar literatūru starp suņiem, kas pakļauti ķirurģiska iejaukšanās trahejas kolapsa dēļ tikai 9% bija smagi aptaukojušies (4).
Dzemdes kakla trahejas sabrukuma gadījumā suņiem pēc iedvesmas rodas elpas trūkums. Dzīvnieks smagi pūš, ar grūtībām ievelkot gaisu. Auskultācija atklāj stridoru un citus rupjus rales elpceļos. Šādi auskultācijas simptomi ir raksturīgi dzemdes kakla trahejas sabrukumam un vienlaicīgai balsenes paralīzei. Attīstoties balsenes maisiņu pietūkumam, var parādīties augšējo elpceļu obstrukcijas simptomi. Tas izpaužas kā pārejošs "izspiedošs" klepus un augstspiediena ieelpojot.

2.a attēls. Trahejas posmi un spiediens, kas iedarbojas uz atsevišķām elpceļu daļām: trahejas kakla daļa ir pakļauta atmosfēras spiediens, un krūtis- pleiras.

26. attēls. Ieelpojot, diafragma paplašinās un virzās atpakaļ. Tā rezultātā spiediens pleiras dobumā kļūst negatīvs. Negatīvā spiediena vilnis tiek pārraidīts pa elpošanas ceļiem un izraisa atmosfēras gaiss iekļūt plaušās. Suņiem ar trahejas kolapsu traheja zaudē savu elastību un spēju izturēt spiediena izmaiņas. Tā rezultātā ieelpošanas laikā tas nokrīt dorsoventrālā virzienā.

2.c attēls. Ar piespiedu izelpu vai klepu pleiras spiediens kļūst pozitīva. Tas nodrošina elpceļu atvēršanos krūtīs. Tomēr, ja skrimšļa gredzeni nav pietiekami stingri, notiek sabrukums.
Kad sunim attīstās hronisks bronhīts, ko pastiprina dzemdes kakla vai krūšu kurvja trahejas sabrukums, klepus kļūst skarbs, kļūst nemainīgs un to pavada krēpu izdalīšanās. Reti suņiem ar dzemdes kakla vai krūšu kurvja trahejas kolapsu ir pārejoša hipoksēmija, kas izraisa ģīboni. Bieži vien šāds ģībonis rodas klepus lēkmju laikā. Tomēr dažiem suņiem ģībonis rodas sekundāras attīstības rezultātā plaušu hipertensija un hipoksija.
Klīniskā izmeklēšana
Suņi ar trahejas sabrukumu miera stāvoklī izskatās veseli. Pat klepus uzbrukumu laikā to stāvoklis nerada trauksmi. Es gribu jebkuru suni ar zīmēm sistēmiskas slimības jāpārbauda, vai nav patoloģiju, kas izraisa klepus lēkmes (sirds mazspēja, pneimonija, ieelpas trakta jaunveidojumi). Rūpīga vispārējā klīniskā pārbaude noskaidros klepus cēloni un identificēs pavadošās slimības.

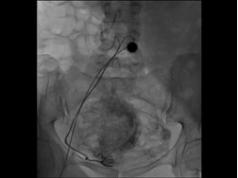
3. attēls.
10 gadus veca Jorkšīras terjera elpceļu ieelpošanas rentgenogrāfija. Sunim 2 mēnešus bija klepus lēkmes, elpas trūkums un cianoze. Radiogrāfija, kas iegūta sānu projekcijā, parāda dzemdes kakla trahejas sabrukumu, kas stiepjas līdz pat trahejas ieejai krūtis. Krūškurvja aorta ir nedaudz paplašināta. Rentgens ar Dr. Anne Babr pieklājību)
Elpošanas sistēmas pārbaude jāsāk ar rūpīgu auskultāciju un trahejas un balsenes maigu palpāciju. Sataustāmu balsenes maisiņu klātbūtne norāda uz šī orgāna darbības traucējumiem. Pēc dažu pētnieku domām, šāda disfunkcija attīstās 20-30% suņu ar trahejas kolapsu (5, 6). Gaisa plūsmas turbulizācija sašaurinātajā trahejas zonā izraisa raksturīgu skaņu veidošanos, kas dzirdama trahejas auskultācijas laikā. Dažiem suņiem ar trahejas kolapsu traheja ir ārkārtīgi jutīga, tāpēc pārbaudes laikā ir jābūt īpaši uzmanīgiem, lai novērstu lēkmes stimulāciju. Palpējot traheju, dažos sabrukšanas gadījumos ir iespējams noteikt tās skrimšļa gredzenu pārmērīgu atbilstību vai maigumu.
Suņiem ar nekomplicētu lielo elpceļu sabrukumu elpošanas skaņas plaušās bieži ir normālas. Taču auskultācijas izmeklējumu veikšana šādos gadījumos var būt apgrūtināta elpas trūkuma, paātrinātas elpas un aptaukošanās dēļ (kā rezultātā elpošanas skaņas ir apslāpētas). Turklāt spēcīgas skaņas augšējos elpceļos slāpē vājās bronhoalveolārās skaņas. Patoloģiski trokšņi plaušās (sēkšana un svilpošana) bieži vien ļauj diagnosticēt patoloģijas būtību. Sēkšana plaušās parasti norāda, ka gaiss plūst caur šķidrumu pildītām alveolām vai ar gļotām bloķētiem elpceļiem. Mīksta sēkšana pēc iedvesmas var liecināt par plaušu tūsku; asākas un skaļākas sēkšanas ir raksturīgas suņiem ar pneimoniju un plaušu fibrozi. Svilpes ir garākas skaņas, parasti dzirdamas izelpojot. Tie ir raksturīgi dzīvniekiem ar hronisku bronhītu. Raksturīga iezīme mazo elpceļu bojājumus izraisa arī vēdera sasprindzinājums izelpas laikā.
Mazo šķirņu suņiem bieži ir sirds vārstuļu nepietiekamība. Tā rezultātā sirds trokšņi var īpaši apgrūtināt klepus cēloņu diagnosticēšanu ar auskultāciju. Tahikardija parasti tiek novērota sastrēguma sirds mazspējas gadījumā. Elpošanas ceļu slimībās sirdsdarbība parasti paliek nemainīga, bet izteikta sinusa aritmija. Kad elpošanas sistēma ir noslogota, šādiem dzīvniekiem var parādīties tahikardija, kas ievērojami sarežģī diagnozi. Īpaši grūti ir diagnosticēt slimību maziem suņiem, kuri cieš no sastrēguma sirds mazspējas un trahejas un bronhu patoloģijām. Šādos gadījumos ir norādīta rentgena izmeklēšana.
Diagnostika
Lai gan trahejas sabrukuma diagnozi var veikt, pamatojoties uz vēsturi un klīniskajiem simptomiem, lai noteiktu vienlaicīgas slimības un tikšanās individuāla ārstēšana Ir nepieciešams veikt vispārēju slimā dzīvnieka klīnisko pārbaudi. Lai diagnosticētu vienlaicīgas slimības, ieteicams veikt pilnīga analīze asinis, ieskaitot šūnu skaita un seruma bioķīmisko parametru noteikšanu un urīna analīzi.
Vizualizācijas metodes
Lai precizētu trahejas kolapsa diagnozi un identificētu vienlaicīgas plaušu un sirds slimības, ir indicēta radiogrāfijas izmantošana. Parasti rentgenogrammas tiek iegūtas standarta projekcijās, bet labāk ir iegūt rentgena attēlus ventrodorsālajā projekcijā ieelpošanas un izelpas laikā. Uz rentgenogrammām, kas iegūtas pilnas iedvesmas laikā, ir skaidri redzams dzemdes kakla trahejas sabrukums. Trahejas krūšu daļu var paplašināt (3. attēls, 4a). Galveno bronhu, krūšu kurvja trahejas sabrukums vai kombinācija parasti ir redzama rentgenogrammās, kas iegūtas pilnas izelpas laikā. Trahejas kakla daļa ir uzpūsta (46. attēls).
Diagnozes precizitāte palielinās, ja rentgena izmeklējuma laikā tiek provocēts klepus lēkme. Diemžēl no statiskā rentgenogramma ir grūti pareizi interpretēt elpceļu dinamiku. Saskaņā ar dažiem pētījumiem, rentgenogrammas var noteikt trahejas sabrukumu tikai 60–84% gadījumu (4, 5). Trahejas radiogrāfiskā vizualizācija bieži ir sarežģīta barības vada vai dzemdes kakla muskuļu attēlu pārklāšanās dēļ. Šādos gadījumos radiogrāfiskās izmeklēšanas laikā ir efektīva nestandarta projekcijas izmantošana no apakšas uz augšu. Šī projekcija ļauj identificēt sabrukušās vietas dzemdes kakla trahejā, lai gan var būt grūti pareizi virzīt rentgena staru. Masu fluoroskopisko izmeklējumu laikā suņu būdās iespējams konstatēt pārejošas elpceļu kolapsa gadījumus. Ar to pašu metodi var noteikt elpošanas cikla fāzi, kuras laikā attīstās kolapss.
Bildes 4. Pūdeļa elpceļu rentgenogrāfija 13 gadu vecumā, ilgu laiku cieš no klepus lēkmēm.

4a. Rentgens, kas uzņemts iedvesmas laikā. Trahejas kakla un krūšu kurvja daļas ir brīvas. Arī galvenie bronhi ir brīvi, lai gan kreisā bronha diametrs ir nedaudz mazāks.

46. Izelpas rentgens. Ir skaidri redzams krūšu kurvja trahejas sabrukums. Sabrukums ietekmē arī galvenos bronhus un elpceļus, kas atrodas tālāk no krūšu kaula.
Nesen trahejas kolapss tika izmantots, lai diagnosticētu trahejas sabrukumu. ultrasonogrāfija(7). Kad ultraskaņas avots atrodas uz kakla, ir iespējams pārbaudīt dzemdes kakla trahejas lūmena diametru un dokumentēt tā izmaiņu dinamiku elpošanas cikla laikā. Gadījumos, kad nav iespējams veikt fluoroskopiju, kā vispiemērotākā metode trahejas kolapsa diagnosticēšanai tiek nozīmēta ultraskaņa. Diemžēl, ultraskaņas izmeklēšana parasti efektīva tikai dzemdes kakla trahejas kolapsam. Turklāt tas neļauj diagnosticēt vienlaicīgu iekaisuma procesi un apakšējo elpceļu infekcijas.
Mazo šķirņu suņiem ķermeņa tipa vai aptaukošanās dēļ var būt grūti noteikt plaušu un sirds audu novirzes, izmantojot rentgenogrāfiju. Piemēram, suņiem ar lieko svaru ķermeņa tauki krūtīs un videnē var radīt nepatiesu priekšstatu par infiltrātiem un plaušās. Tauku uzkrāšanās perikardā un samazināta plaušu mobilitāte, kas saistīta ar aptaukošanos, var maldināt kardiomegālijas klātbūtni. Tāpēc suņiem ar trahejas kolapsu intersticiālā blīvuma un sirds izmēra izmaiņas ir jāinterpretē piesardzīgi. Ja dzīvniekam ir sirds trokšņi Īpaša uzmanība Jums vajadzētu pievērst uzmanību sirds kontūras pārbaudei - ir iespējama kreisā ātrija hipertrofija, jo tā tiek saspiesta ar kreiso bronhu. Izmantojot ventrolorālo rentgenogrammu, jūs varat ne tikai pārbaudīt suņa sirds un plaušu stāvokli, bet arī novērtēt tā aptaukošanās pakāpi. Suņa saimniekam noteikti jānorāda uz taukiem tauku slānis aptver krūtis. Tas palīdzēs pārliecināt viņu par nepieciešamību samazināt dzīvnieka svaru.
Paraugu iegūšana no elpceļiem
Lai iegūtu paraugus no elpceļiem, izmanto vai nu trahejas skalošanu, vai bronhoskopiju. Abām šīm procedūrām nepieciešama anestēzija. Tomēr ir ļoti noderīgi tos veikt, jo tas ļauj iegūt šķidruma paraugus no elpceļu apakšējām daļām citoloģiskiem vai bakterioloģiskiem pētījumiem. Izmantojot šīs metodes, iespējams diagnosticēt elpceļu infekciju un novērtēt iekaisuma reakciju devumu novērotajos klīniskajos simptomos. Pirms skalošanas vai bronhoskopijas veikšanas nepieciešama rūpīga augšējo elpceļu izmeklēšana. Augšējo elpceļu obstrukcija var pastiprināt simptomus, kas saistīti ar trahejas sabrukumu. Pārbaudot augšējos elpceļus, īpaša uzmanība jāpievērš balsenes funkcijas stāvoklim, mīksto aukslēju garumam un balsenes maisiņu pietūkuma neesamībai.
Lai veiktu trahejas skalošanu, visērtāk ir izmantot transorālu pieeju (skatīt 1. protokolu). Izmantojot šo pieeju, ir mazāks risks bojāt trahejas un gļotādas skrimšļa gredzenus. Lai atvieglotu intubāciju, to labāk izmantot vispārējā anestēzija vai spēcīgiem sedatīviem līdzekļiem. Lai mazinātu gļotādas kairinājumu, jāizmanto plānas sterilas intratraheālās zondes. Ievietojot zondi trahejā, jāraugās, lai iegūtie paraugi netiktu piesārņoti ar baktēriju mikrofloru un augšējo elpceļu gļotādas šūnām. Šai procedūrai nav nepieciešams izmantot zondes aproci. Iegūtie skalošanas paraugi jānosūta bakterioloģiskai kultivēšanai, lai identificētu aerobo baktērijas. Jūs varat arī veikt kultūras mikoplazmas infekcijai.
Bakterioloģisko pārbaužu rezultātu interpretācija ir ievērojami atvieglota pēc skalošanas citoloģiskās izmeklēšanas. Piemēram, plkst veseli suņi Rīkle nav sterila, tāpēc skalošanas kultūru bakterioloģiskā izmeklēšana var atklāt baktēriju augšanu (8) (1. tabula). Kad skalošanas laikā tiek konstatētas plakanšūnas mutes dobums un baktērijas Simonsiella histoloģiskās izmeklēšanas laikā var sagaidīt šo baktēriju un mikoplazmu augšanu un in bakterioloģiskās kultūras. Bakterioloģiskā kultūra skalošanas suņiem ar trahejas sabrukumu parasti atklāj daudzas baktērijas dažādi veidi(1. tabula). Tomēr joprojām nav skaidra bakteriālas infekcijas loma šīs slimības klīnisko simptomu attīstībā.
rezultātus bakterioloģiskie pētījumi veselu suņu un suņu ar trahejas kolapsu mikrofloru
Trahejas kolapsa smagums
| I pakāpe | Trahejas skrimšļainie gredzeni saglabā gandrīz normālu gredzena struktūru. Ir vērojama neliela muguras trahejas membrānas novirze trahejas lūmenā, samazinot šī lūmena diametru ne vairāk kā par 25%. |
| II pakāpe | Skrimšļveida gredzeni ir saplacināti. Izstieptās muguras trahejas membrānas novirzes dēļ trahejas lūmena diametrs tiek samazināts par aptuveni 50%. |
| III pakāpe | Skrimšļveida gredzeni ir ļoti stipri saplacināti. Trahejas membrānas muskuļi pieskaras gredzenu iekšpusei.Trahejas lūmena diametrs ir samazināts par 75%. |
| IV pakāpe | Trahejas membrānas muskuļi pilnībā bloķē trahejas lūmenu. Smagos gadījumos trahejas lūmenis kļūst dubultā. |
Lai iegūtu apakšējos elpceļus apdzīvojošās mikrofloras paraugus, labāk izmantot bronhoskopiju. Izmantojot bronhoskopu, paraugus var iegūt, neriskējot inficēties ar baktērijām no augšējo elpceļu. Turklāt bronhoskopija var apstiprināt trahejas kolapsa diagnozi gadījumos, kad rentgenogrāfija un fluoroskopija neļauj izdarīt stingru secinājumu. Bronhoskopija ļauj tieši novērtēt trahejas vai bronhu bojāto skrimšļa pēdu atrašanās vietu un pavājināšanās pakāpi (2. tabula). kas raksturo trahejas kolapsa smagumu, kas ir īpaši svarīgi, gatavojoties operācijai. Bronhoskopija ļauj arī izpētīt bojājumu dinamiku un raksturu, noteikt gļotādu iekaisuma un kairinājuma vietas, apstiprināt vai atspēkot krūšu kurvja trahejas sabrukuma diagnozi. Tādējādi bronhoskopija ir viena no visvairāk efektīvas metodes novērtēt elpceļu slimību lomu plaušu mazspējas attīstībā.
Protokols trahejas skalošanas veikšanai suņiem
- Dodiet sunim skābekļa masku iepriekšējai skābekli.
— Ieej nomierinošs līdzeklis izpētīt augšējo elpceļu uzbūvi un funkcijas. Elpošanas laikā novērojiet balsenes darbību. Parasti suņiem aritenoīdu skrimšļi ieelpošanas laikā pārvietojas uz sāniem.
— Intubējiet dzīvnieku ar plānu, sterilu endotraheālu caurulīti. Intubācijas laikā pārliecinieties, ka zonde, nonākot elpceļos, nepieskaras rīklei.
— Caur zondi līdz krūšu kaula līmenim ievietojiet plānu, sterilu polipropilēna katetru elpošanas traktā (var izmantot zondi parenterālai barošanai). Katetra garumam jābūt tādam, lai tas varētu sasniegt 4. ribas līmeni.
- Caur katetru, izmantojot šļirci, ievadiet 4-6 ml sterila sāls šķīduma. Piesūcot ievadīto šķidrumu, lieciet sunim klepot vai masējiet krūtis - tas palielinās atsūkšanas skalošanas apjomu.
— Ja nepieciešams, atkārtojiet fizioloģiskā šķīduma injekciju un atsūkšanu. Ir nepieciešams iegūt 0,5-1 ml skalošanas. Skalošana jānosūta bakterioloģiskai (tai skaitā mikoplazmu klātbūtnes noteikšanai) un citoloģiskai izmeklēšanai.
— Pirms procedūras pabeigšanas trahejas katetrā injicējiet 1 ml 1% lidokaīna šķīduma. Tas vājinās klepus refleksu.
— Ja nepieciešams, ievietojiet pacientu skābekļa kamerā.
Sagatavojot suņus elpceļu izmeklēšanai, tiem 5 minūtes jāsaņem skābekli. pirms anestēzijas sākuma. Anestēzijai jūs varat izmantot visvairāk Dažādi ceļi. Anestēzijas mērķis in šajā gadījumā- novērst klepus refleksu un endoskopa bojājumus bronhoskopijas laikā. Izvēloties anestēzijas metodi, jums jāpievērš uzmanība vispārējais stāvoklis suņa veselība un lietotās anestēzijas līdzekļa īpašības (tā blakus efekti). Tā kā lielākā daļa suņu ar trahejas sabrukumu ir mazas šķirnes, vēlams izmantot brohoskopus, kuru diametrs nepārsniedz 4,5-5 mm. Dažreiz suns ir tik mazs, ka anestēziju nevar ievadīt ar gāzveida anestēzijas līdzekļiem un bronhoskopu nevar izlaist caur intratraheālo cauruli. Šajā gadījumā, izmantojot anestēziju ar gāzveida anestēzijas līdzekļiem trahejas un apakšējo elpošanas ceļu bronhoskopiskās izmeklēšanas laikā, suns ir jāekstubē.
Lai veiktu bronhoskopiju, suns jānovieto ar muguru uz augšu un zem zoda jānovieto neliels spilvens. Lai procedūras laikā nostiprinātu muti atvērtā stāvoklī, tiek izmantoti 2 lieli mutes atvērēji. Pirmkārt, ar bronhoskopa palīdzību tiek pārbaudīta balsene un augšējie elpceļi. Pēc tā ievadīšanas trahejā tiek noteikta tās sabrukšanas pakāpe un dinamika (5. attēls). Izmantojot zīmes uz atlikušās bronhoskopa ārējās daļas, varat noteikt trahejas sabrukušās daļas garumu vai skrimšļa gredzenu skaitu, kuru struktūra ir traucēta. Pēc bronhoskopa ievietošanas elpceļu retrosternālajā daļā tiek pārbaudīti galvenie bronhi. Veselīgi bronhi ir atvērti un tiem ir apaļš vai eliptisks šķērsgriezums

(6. attēls). Elpošanas laikā elpceļu diametram vajadzētu nedaudz mainīties, un izdalījumu daudzumam tajos jābūt minimālam. Suņiem ar vispārēju elpceļu kolapsu šo elpceļu lūmena forma ir mainīga. Turklāt šo lūmenu aizvēršanās tajos ir skaidri redzama pat ar nepiespiedu elpošanu (7. attēls).

Visiem suņiem, kam tiek veikta bronhoskopija, ir jābūt bronhoalveolāra skalošana(BUMBA). To iegūst, izmantojot bronhoskopu, un nosūta pārbaudei, lai noteiktu infekciju ar baktērijām vai mikoilāzēm, kā arī iekaisuma pazīmes. Pamatojoties uz iegūtā BAL šķidruma bakterioloģiskās un histoloģiskās izmeklēšanas rezultātiem, dzīvniekam var nozīmēt atbilstošu antibiotiku terapiju un/vai pretiekaisuma ārstēšanu (9). Lai iegūtu BAL, bronhoskopu uzmanīgi ievieto mazajos bronhos un caur tā biopsijas kanālu ievada 10-20 ml sterila fizioloģiskā šķīduma. Ievadītā šķidruma atsūkšanu var veikt manuāli, īpaši uzmanīgi vai izmantojot mehānisku sūkšanu ar parauga slazdu. Parasti ir iespējams izsūkt 40-60% no ievadītā šķidruma tilpuma. Parasti BAL satur apmēram 300 leikocītu uz ml, no kuriem 70-80% ir alveolārie makrofāgi, 5-6% ir limfocīti. 5-6% - neitrofiliem un 5-6% - eozinofiliem. Pierakstīties iekaisuma reakcija kalpo kā ievērojams neitrofilu skaita pieaugums. Infekcijas faktu var noteikt, pamatojoties uz septisko neitrofilu noteikšanu un fagocitētu baktēriju klātbūtni šūnās.

5. attēls. II-III grādiem. Lai nodrošinātu skābekļa piegādi bronhoskopijas laikā, tika izmantots sterils gumijas katetrs. Skrimšļveida gredzeni ir saplacināti, kā rezultātā tiek izstiepta trahejas muguras daļa (zem atzīmes attēlā).
Fotoattēlu sniedza JeffD. Beja, DVM. MS, Misūri universitāte, Kolumbija. ASV
Bronhoskopija suņiem ar trahejas kolapsu ir riskanta procedūra. Komplikāciju risks ir īpaši augsts suņiem ar aptaukošanos, kas atšķiras paaugstināta jutība traheja. Lai samazinātu komplikāciju risku, dzīvnieks no anestēzijas jāizved lēnām, nodrošinot ar skābekli bagātinātu vidi. IN distālā daļa traheja pirms bronhoskopa noņemšanas varat injicēt 1 ml 1% lidokaīna šķīduma. Tas vājinās klepus refleksu.
Narkotiku ārstēšana
Ja sunim ir smags elpas trūkums, kas saistīts ar elpceļu obstrukciju, stresu diagnostiskā pārbaude jāsamazina līdz minimumam. Šādos gadījumos, lai izņemtu dzīvnieku no bīstams stāvoklis jums ir nepieciešams ievietot viņu skābekļa kamerā un lietot vieglus sedatīvus līdzekļus. Piemēram, subkutāna butofanola (0,05-1 mg/kg) un acepromazīna (0,01-0,1 mg/kg) ievadīšana ik pēc 4-6 stundām var ne tikai nomierināt suni, bet arī apturēt tā klepus uzbrukumu. Jāatzīmē, ka šo izmantošana zāles kombinācijā prasa zināmu piesardzību, jo tas var izraisīt straujš kritums asinsspiediens. Lietošanas sākumā jālieto minimālā deva zāles lai noteiktu konkrētā dzīvnieka jutību pret tiem. Ja nevēlamas sekas nenotiek, nākotnē, ja nepieciešams, devu var palielināt. Ja jūsu sunim ir smags trahejas iekaisums vai balsenes pietūkums, viņam jāievada vienreizēja īslaicīgas darbības kortikosteroīda deva, kam ir pretiekaisuma iedarbība.
Trahejas kolapsa ilgstošai terapijai suņiem jābūt vērstai uz to faktoru vājināšanu, kas var izraisīt slimības klīnisko simptomu pastiprināšanos. Diemžēl nav specifisku metožu vielmaiņas traucējumu ārstēšanai trahejas gredzenu skrimšļa audos, tāpēc slimības saasināšanās risks slimam sunim saglabājas visu mūžu. Ja tiek atklāta elpceļu infekcija, jānosaka antibiotiku terapija. Antibiotiku izvēle tiek veikta, pamatojoties uz pacienta inokulētās mikrofloras jutības noteikšanu pret tām. Ja tiek atklāta mikoplazmas infekcija, jālieto antibiotikas, kas ir efektīvas pret mikroorganismiem, kuriem nav šūnu sienas. Visefektīvākie šajā gadījumā ir doksiciklīns, hloramfenikols un enrofloksacīns. Lai sterilizētu elpceļus, parasti pietiek ar 7-10 dienu ilgu antibiotiku kursu, bet pneimonijas klātbūtnē antibiotiku terapijas ilgums var būt no 3 līdz 6 nedēļām.
Smaga traheīta gadījumā tas ir nepieciešams īsa ārstēšana kortikosteroīdu zāles. Parasti pacientam tiek ievadīts prednizons vai prednizolons 0,5 mg/kg/dienā 3-7 dienas. Ja sunim uz fona ir trahejas sabrukums hronisks bronhīts tiek noteikts ilgāks kortikosteroīdu terapijas kurss. Zāles lieto lielās devās. Pēc iekaisuma mazināšanas un infekcijas likvidēšanas tiek nozīmēti klepus medikamenti. Tās nomākšana ir nepieciešama, lai pārtrauktu atkārtotu elpceļu bojājumu ciklu. Klepus nomākšanai suņiem ar trahejas kolapsu parasti ir jāizmanto narkotiskās vielas. Klepu var efektīvi nomākt ar hidrokolonu (0,22 mg/kg 2-3 reizes dienā) vai butorfanolu (0,55-1,1 mg/kg, ja nepieciešams). per os(10). Kursa sākumā šo medikamentu devu izvēlas katram sunim individuāli tā, lai panāktu maksimālu klepus nomākšanu.Noreptori nav bronhodilatatori, taču tie izraisa mazo elpceļu paplašināšanos un veicina gaisa apmaiņu tajos laikā. izelpa. Tā rezultātā tiek samazināta krūšu kurvja trahejas sabrukuma iespējamība. Īpaši farmakokinētikas pētījumi dažādas formas teofilīns parādīja, ka divi dažādu firmu ražoti ilgstošas darbības teofilīna preparāti nodrošina pietiekami augstas zāļu koncentrācijas uzturēšanu suņu asinīs ilgstoši. Arī parastās teofilīna formas var būt efektīvas, taču to efektivitāte ir daudz zemāka nekā minētajiem ilgstošas darbības preparātiem. Trahejas kolapsam suņiem izmanto arī beta adrenerģisko receptoru agonistus: terbutalīnu (1,25-5 mg/kg<гол- 2-3 раза вдень) и альбутерол (50 мкг/кг 3 раза в день). Следует помнить, что применение бронхорасширяющих средств любого типа может привести к побочным эффектам, например, повышенной нервозности и возбудимости животных, тахикардии, желудочно-кишечным расстройствам.
Visiem suņiem ar trahejas kolapsu nepieciešama uztura terapija. Samazinot ķermeņa svaru, piemēram, ievērojami samazinās slodze uz elpošanas sistēmu. Lai sasniegtu šo mērķi, dzīvniekus parasti pāriet uz gatavām mazkaloriju diētām, kas nodrošina aptuveni 60% no veseliem suņiem nepieciešamās enerģijas. Ideāls svara zaudēšanas ātrums (2-3% no ķermeņa svara nedēļā) ļauj saimniekam ātri normalizēt suņa svaru. Lietderīgi arī pamazām palielināt dzīvnieka fizisko slodzi – tādējādi vieglāk un ātrāk sasniegt normālu ķermeņa svaru. Jāņem vērā, ka karstā un mitrā laikā fiziskās aktivitātes labāk samazināt līdz minimumam, bet apkakli nomainīt pret uzkabi. Tas ļaus izvairīties no pēkšņas slimības saasināšanās.
Ķirurģija
Dzemdes kakla trahejas sabrukšanas gadījumā efektīva ir skarto skrimšļa gredzenu protezēšana. Ķirurģiska iejaukšanās ir indicēta gadījumos, kad terapeitiskā ārstēšana ir neefektīva vai kad dzīvnieki izjūt novājinātus kondicionētus refleksus un ģīboni elpošanas traucējumu dēļ. Ķirurģiska iejaukšanās ievērojami vājina klīniskos simptomus: klepus pazūd, elpošana kļūst brīvāka. Viens pētījums atklāja, ka suņu īpašnieki kopumā bija apmierināti ar operācijas iznākumu, pat ja pēcoperācijas balsenes paralīzei bija nepieciešama traheostomija.
Suņiem ar augšējo elpceļu obstrukciju ir nepieciešama obstrukcijas cēloņa ķirurģiska noņemšana. Piemēram, ir pierādīts, ka mīksto aukslēju saīsināšana un balsenes aritenoidālā skrimšļa atbrīvošana mazina trahejas kolapsa klīniskos simptomus.
Trahejas sabrukums ir izplatīts mazu šķirņu suņiem, un tam nepieciešama ilgstoša ārstēšana. Slimiem dzīvniekiem ieteicams samazināt ķermeņa svaru un lietot pretklepus medikamentus. Katrā konkrētā gadījumā svarīgi ir arī identificēt un likvidēt vienlaicīgas augšējo un apakšējo elpceļu slimības, kas sarežģī trahejas kolapsa gaitu.
Bronhoalveolārā skalošana ir medicīniska procedūra, ko izmanto diagnostikas un terapeitiskos nolūkos pacientiem ar bronhopulmonālās sistēmas patoloģijām. Šīs manipulācijas veikšanas tehnika sastāv no bronhu koka mazgāšanas ar īpašu šķīdumu un pēc tam to izņemšanu. Ja procedūra tiek veikta diagnostikas nolūkos, tad tiek veikts noņemtā mazgāšanas ūdens laboratoriskais pētījums.
Indikācijas
Bronhoalveolārā skalošana tiek nozīmēta kā papildu pētījums, lai noskaidrotu elpošanas sistēmas patoloģijas būtību un cēloni.
Pētījums ir indicēts diagnozei:
- izplatīti procesi plaušās (sarkoidoze, tuberkuloze, azbestoze, fibrozējošais alveolīts);
- ļaundabīgi audzēji (ieskaitot metastātiskus bojājumus);
- nezināmas etioloģijas fokālie patoloģiskie procesi (ilgstoša un recidivējoša pneimonija, ko nevar ārstēt ar medikamentiem);
- hroniski iekaisuma procesi bronhos (hronisks bronhīts, bronhiālā astma).
Procedūra ir kontrindicēta pacientiem ar pavadošām slimībām dekompensācijas stadijā.
Diagnostikas vērtība
Mazgājumus, kas iegūti no bronhu un alveolu virsmas, izmanto mikrobioloģiskiem, bioķīmiskiem, imunoloģiskiem un citoloģiskiem pētījumiem. Dažos gadījumos skalojamā ūdens citoloģiskā izmeklēšana var pat aizstāt biopsiju. Visinformatīvākie ir visaptveroši laboratorijas testi.
Dažos gadījumos nav iespējams noteikt pareizu diagnozi bez bronhoalveolārās skalošanas pētījuma. Tas ļauj droši apstiprināt sarkoidozes videnes formas diagnozi. Šajā patoloģijā nav radioloģisko izmaiņu skarto limfmezglu specifiskās atrašanās vietas dēļ.
Sagatavošana
Sagatavošanas pasākumi:
- Pacientam ir jāveic visi noteiktie izmeklējumi, lai ārstējošajam ārstam būtu pilnīgs priekšstats par pacienta veselības stāvokli un viņš varētu noteikt blakusslimības.
- 10-12 stundas pirms skalošanas vajadzētu ieturēt vieglas vakariņas (lai novērstu kuņģa satura aspirāciju).
- Pārbaudes dienā ir stingri aizliegts smēķēt (tas var izraisīt izkropļotus rezultātus).
- Nomierinošus līdzekļus lieto 2-3 stundas pirms testa.
- Tieši pirms procedūras sākšanas jums ir jāiztukšo urīnpūslis un zarnas.
Pacientiem, kas cieš no bronhiālās astmas, līdzi jābūt bronhodilatatoram, jo šī procedūra var izraisīt bronhu spazmas lēkmi.
Ārsts individuāli lemj par pacienta pastāvīgi lietoto medikamentu pagaidu atcelšanu.
Tehnika
Bronhoalveolārā skalošana tiek veikta bronhoskopijas laikā. Izmeklēšanu var veikt, izmantojot stingru bronhoskopu (vispārējā anestēzijā) un elastīgu optisko šķiedru bronhoskopu (vietējā anestēzijā).
Otrā metode ir labāka, jo tai nav nepieciešama vispārēja anestēzija un pacienti to labāk panes.
Tehnika sastāv no šādām darbībām:

- Tiek nodrošināta atbilstoša sāpju mazināšana. Ja izmeklēšanu plānots veikt ar cieto bronhoskopu, tad anesteziologs veiks vispārējo anestēziju. Ja tiek izmantots elastīgs optiskās šķiedras bronhoskops, lokālos anestēzijas līdzekļus izsmidzina uz mutes un rīkles gļotādām. Vietējā anestēzija ļauj izvairīties no sāpīga diskomforta izmeklējuma laikā, kā arī palīdz nomākt rīstīšanās un klepus refleksus, kas var sarežģīt procedūru.
- Pārbaude tiek veikta sēdus vai guļus stāvoklī uz dīvāna. Pēc tam, kad subjekts ir ieņēmis vajadzīgo pozīciju, speciālists lēnām ievada bronhoskopu elpceļos caur deguna vai mutes dobumu. Ar pareizu anestēziju pacientam nav diskomforta vai sāpju.
- Izmantojot video aparatūru, tiek izmeklētas elpceļu gļotādas un konstatētas novirzes no normas.
- Caur speciālu katetru izvēlētajā bronhā ievada līdz cilvēka ķermeņa temperatūrai (37-39 °C) uzsildītu izotonisku šķīdumu. Pēc tam ievadītais šķidrums tiek aspirēts, izmantojot vakuuma elektrisko ekstraktoru. Kopējais izmantotā šķīduma tilpums ir 150-300 mililitri (atkarībā no tā, cik daudz materiāla nepieciešams laboratorijas pētījumiem). Sāls šķīdums tiek injicēts nelielās porcijās (10-30 mililitri), savukārt iepriekš ievadītais šķidrums tiek pilnībā aspirēts.
- Izņemto mazgāšanas ūdeni ievieto sterilā traukā un nosūta uz laboratoriju. Iegūtie tamponi jāuzglabā temperatūrā, kas zemāka par 5 °C, ne ilgāk kā 2 stundas no savākšanas brīža. Stikla traukus nedrīkst izmantot materiālu uzglabāšanai un transportēšanai, jo šādos apstākļos daži šūnu elementi tiek iznīcināti.
- Laboratorijā pēta no bronhu un alveolāro telpu gļotādām iegūtā materiāla šūnu sastāvu. Tiek aprēķināts kopējais šūnu skaits, dažādu šūnu elementu procentuālais daudzums un tiek identificētas netipiskas šūnas.
- Veicot mikrobioloģisko izmeklēšanu, tiek identificētas dažādas baktērijas (mycobacterium tuberculosis, pneimokoki, Pseudomonas aeruginosa un citas).
- Mazgāšanas ūdens bioķīmiskā izpēte nosaka dažādu ķīmisko vielu kvalitatīvo un kvantitatīvo saturu, kā arī fermentu un bioloģiski aktīvo vielu klātbūtni un funkcionālo aktivitāti.
Rezultātu atšifrēšana
Pacientiem ar akūtu strutojošu bronhu vai plaušu parenhīmas iekaisumu citoloģiskā izmeklēšana atklās būtisku neitrofilu skaita pieaugumu.
Par procesa tuberkulozo etioloģiju liecinās mērens limfocītu skaita pieaugums ar vienlaicīgu alveolāro makrofāgu skaita samazināšanos.
 Bronhiālās astmas gadījumā tiks konstatētas alerģiskajam procesam raksturīgas izmaiņas (eozinofilu skaita pieaugums 10-15 reizes).
Bronhiālās astmas gadījumā tiks konstatētas alerģiskajam procesam raksturīgas izmaiņas (eozinofilu skaita pieaugums 10-15 reizes).
Netipisku šūnu elementu noteikšana testa materiālā norāda uz ļaundabīga audzēja klātbūtni vai metastātisku plaušu bojājumu.
Ar hemosiderozi tiks konstatēti specifiski hemosiderofāgi.
Ar azbestozi būs redzamas mikroskopiskas azbesta putekļu daļiņas, ko sauc par azbesta ķermeņiem.
Bakterioloģiskās izmeklēšanas laikā iegūtais materiāls tiek novietots uz īpašām uzturvielu barotnēm. Patogēnu klātbūtnē krēpās tiks iegūta mikrobu koloniju augšana. Papildus tam tiek noteikta kultivētās baktēriju floras jutība pret antibiotikām, kas palīdz ārstam katram pacientam izvēlēties piemērotāko ārstēšanas shēmu.
Paaugstināta elastāzes enzīma aktivitāte, kas atklāta mazgāšanas ūdens bioķīmiskās analīzes laikā, liecina par emfizēmas vai pneimosklerozes attīstību. Šie dati ir īpaši vērtīgi patoloģiskā procesa attīstības sākumposmā, jo citas metodes vēl nevar noteikt izmaiņas. Proteāzes aktivitātes rādītāji daudzās slimībās atšķiras un ir vērtīgi tikai tad, ja tos novērtē kopā ar citiem datiem.
Bronhoalveolārā skalošana ir vērtīga metode bronhopulmonārās sistēmas patoloģiju diagnosticēšanai. Manipulāciju labi panes visi pacienti, un tai ir zems komplikāciju risks. Metodes priekšrocība ir tā, ka tā ļauj identificēt daudzas patoloģijas agrīnās attīstības stadijās.
Bronhoalveolārās skalošanas diagnostikas iespējas
M.V. Samsonova
Optiskās šķiedru bronhoskopijas un bronhoalveolārās skalošanas (BAL) tehnikas ieviešana klīniskajā praksē, kas ļauj iegūt bronhu skalošanu (BS) un bronhoalveolāro skalošanu (BAS), ir būtiski paplašinājusi diagnostikas iespējas pulmonoloģijā. Pateicoties BAL tehnikai, ir kļuvis iespējams izmantot veselu virkni citoloģisko, bakterioloģisko, imunoloģisko, bioķīmisko un biofizikālo metožu. Šie pētījumi palīdz pareizi diagnosticēt vēzi un diseminētos procesus plaušās, kā arī ļauj novērtēt iekaisuma procesa aktivitāti bronhoalveolārajā telpā.
BAL tehnika
BAL veic fibrobronhoskopijas laikā vietējā vai vispārējā anestēzijā. Bronhoskopu ievieto lobāra bronhā (parasti labās plaušas vidējā daivā), un bronhu koku mazgā ar lielu daudzumu fizioloģiskā šķīduma, kas uzkarsēts līdz 37°C. Pēc mazgāšanas šķīdums tiek pilnībā aspirēts no bronhu koka.
Bronhoskops tiek ievietots segmentālā bronha mutē, to noslēdzot. Caur bronhoskopa biopsijas kanālu tiek izvadīts polietilēna katetrs un segmentālā bronha lūmenā tiek ievadīts 50 ml fizioloģiskā šķīduma, kas pēc tam tiek pilnībā aspirēts. Iegūtā šķidruma daļa ir bronhu mazgāšana. Pēc tam katetru virza 6-7 cm dziļi segmentā.
Marija Viktorovna Samsonova -
doc. medus. zinātnes, vad lab. Rošdravas patoloģiskās anatomijas Pulmonoloģijas pētniecības institūts.
bronhu un 4 porcijas 50 ml fizioloģiskā šķīduma injicē frakcijās, kuras katru reizi tiek pilnībā aspirētas. Šīs jauktās daļas veido bronhoalveolāro skalošanu.
BS un ALS izpētes metodes
Galvenās BS un ALS izpētes metodes ietver supernatanta bioķīmiskos un imunoloģiskos pētījumus, kā arī šūnu nogulumu izpēti. Vienlaikus tiek aprēķināta BS un ALS šūnu dzīvotspēja, citogramma, veikti šūnu citoķīmiskie pētījumi, kā arī citobakterioskopiskais novērtējums. Nesen tika izstrādāta metode ALS makrofāgu formulas aprēķināšanai dažādām bronhopulmonārās sistēmas slimībām. BAL pētījums ļauj novērtēt arī plaušu virsmaktīvās sistēmas stāvokli, mērot virsmas spraigumu un pētot virsmaktīvās vielas fosfolipīdu sastāvu.
Kvalitatīvu un kvantitatīvu mikrobioloģisko pētījumu veikšanai izmanto BAL šķidruma bronhu daļu. Turklāt izmaiņas BS šūnu sastāvā var noteikt iekaisuma reakcijas smagumu bronhu kokā.
bronhu epitēlijs 5-20%
ieskaitot
kolonnveida epitēlijs 4-15% plakanšūnu epitēlijs 1-5%
alveolu makrofāgi 64-88% neitrofīli 5-11%
limfocīti 2-4%
tuklo šūnas 0-0,5%
eozinofīli 0-0,5%
Normāla BAL alveolārās daļas citogramma (1. att.) ir parādīta tabulā. 1.
BS un ALS izpētes diagnostiskā vērtība
BS un ALS pētījumam ir vislielākā diagnostiskā nozīme, lai novērtētu iekaisuma pakāpi traheobronhiālajā kokā, plaušu audzējos un alveolārās proteinozes gadījumā.
ALS citoloģiskajai izmeklēšanai ir augsta diagnostiskā vērtība tikai dažām plaušu slimībām. Pie šādām nozoloģijām pieder histiocitoze X, kurā parādās Langer-Hans šūnas (to citoplazmā elektronu mikroskopijā nosaka raksturīgos X-ķermeņus; pēc imūnfenotipa tās ir CD1+ šūnas). Ar BAS palīdzību iespējams apstiprināt plaušu asiņošanas esamību. ALS izpēte ir norādīta arī alveolārās proteinozes pārbaudē, ko raksturo ekstracelulāras vielas klātbūtne (2. att.), kas labi noteikta, izmantojot gaismu (PIR reakcija) un elektronu mikroskopiju. Šajā slimībā BAL kalpo ne tikai kā diagnostiska, bet arī kā terapeitiska procedūra.
Rīsi. 1. ALS normāls šūnu sastāvs. Krāsošana pēc Romanovska teiktā. x400.
Pneimokoniozes gadījumā, izmantojot BAS pētījumu, ir iespējams tikai apstiprināt putekļu aģenta iedarbību. Specifisku berilija slimības diagnozi var veikt, pētot ALS šūnu funkcionālo proliferatīvo aktivitāti, reaģējot uz berilija sāļu darbību. Ar azbestozi BAS azbesta ķermeņus var noteikt (3. att.) raksturīgu šķiedru veidā - gan ārpusšūnu, gan intracelulāri. Šie ķermeņi ir azbesta šķiedras, uz kurām ir agregēts hemosiderīns, feritīns un glikoproteīns, tāpēc tie labi iekrāsojas, veicot PAS reakciju un Perla krāsošanu. Personām, kurām ir bijis neprofesionāls kontakts ar azbestu, azbesta ķermeņi tiek konstatēti ārkārtīgi reti, un šādu daļiņu koncentrācija BAS nepārsniedz 0,5 uz 1 ml. Pseidoazbesta ķermeņus var atrast arī ALS - pneimokoniozes gadījumā, kas saistīta ar ogļu, alumīnija, stikla šķiedru u.c. putekļu iedarbību.
Pacientiem ar imūndeficīta stāvokļiem (jo īpaši HIV infekciju) BAL ir izvēles metode infekciozo plaušu bojājumu patogēnu noteikšanai. BAL šķidruma jutīgums Pneumocystis infekcijas diagnostikā (4. att.), pēc dažiem datiem, pārsniedz 95%.
Citu slimību gadījumā BAS pētījums nav īpaši specifisks, bet var sniegt papildu informāciju, kas tiek novērtēta kopā ar klīniskiem, radioloģiskiem, funkcionāliem un laboratoriskiem datiem.
Ar difūzu alveolāru asiņošanu (DAH), kas rodas dažādu slimību gadījumā, ALS var atrast brīvus un fagocitētus eritrocītus un siderofāgus (5. att.). BAS ir efektīva metode BAV noteikšanai pat bez hemoptīzes, kad šī stāvokļa diagnostika ir ārkārtīgi sarežģīta. BAV ir jānošķir no akūta respiratorā distresa sindroma (ARDS),
kurā BAS parādās arī siderofāgi.
Idiopātiskā fibrozējošā alveolīta (IFA) diferenciāldiagnozes ietvaros ALS citoloģiskā izmeklēšana ļauj izslēgt citas intersticiālas plaušu slimības. Tādējādi mērens neitrofilu un eozinofilu īpatsvara pieaugums ALS gadījumā nav pretrunā ar ELISA diagnozi. Būtisks limfocītu un eozinofilu procentuālais pieaugums ELISA nav raksturīgs, un šajos gadījumos jādomā par citu alveolītu (eksogēnu alerģisku, medicīnisku vai arodslimību).
ALS citoloģiskā izmeklēšana kalpo kā jutīga metode eksogēnā alerģiskā alveolīta (EAA) diagnostikā. Liels limfocītu procentuālais daudzums, plazmas un tuklo šūnu, kā arī “putekļu” makrofāgu klātbūtne kopā ar anamnēzes un laboratorijas datiem ļauj diagnosticēt EAA. Iespējama eozīta parādīšanās
1. tabula. Normāla ALS citogramma
Šūnu sastāvs ALS Nesmēķētājiem Smēķētājiem
Citoze, šūnu skaits x106/ml 0,1-0,3 >0,3
Alveolārie makrofāgi, % 82-98 94
Limfocīti, % 7-12 5
Neitrofīli,% 1-2 0.8
Eozinofīli, %<1 0,6
Mast šūnas, %<1 <1
Rīsi. 2. Ārpusšūnu viela ALS ar alveolāru proteīnu. Krāsošana pēc Romanovska teiktā. x400.
nofils jeb milzu daudzkodolu šūnas (6. att.). Limfocītu vidū dominē šūnas ar imūnfenotipu C03+/C08+/C057+/C016-. Jāatceras, ka vairākus mēnešus pēc slimības sākuma līdz ar T-slāpētājiem sāk pieaugt arī T-palīgu skaits. Papildu izpētes metodes ļauj izslēgt citas slimības, kurās ir palielināts limfocītu īpatsvars ALS - difūzās saistaudu slimības, zāļu izraisīts alveolīts (LA), obliterējošs bronhiolīts ar organizējošu pneimoniju (OBOP), silikoze.
Sarkoidozes gadījumā BAS palielinās arī limfocītu īpatsvars, un sarkoidozei raksturīgi ko-
Rīsi. 4. Pneumocystis jiroveci ALS gadījumā. Krāsošana pēc Romanovska teiktā. x400.
Rīsi. 5. Siderofāgi ALS gadījumā. Perls krāsošana. x100.
www.atmosphere-ph.ru
Rīsi. 6. EAA: palielināts eozinofilu, neitrofilu, limfocītu īpatsvars ALS, daudzkodolu milzu šūna. Krāsošana pēc Romanovska teiktā. x200.
Rīsi. 7. “Amiodarona plaušas” (LA): makrofāgi ar putojošu citoplazmu ALS gadījumā. Krāsošana pēc Romanovska teiktā. x1000, eļļas iegremdēšana.
Rīsi. 8. ALS citogrammas limfocītu tips. Krāsošana pēc Romanovska teiktā. x1000, eļļas iegremdēšana.
T-palīgu un T-supresoru (CO4+/CD8+) attiecība ir virs 3,5 (šīs zīmes jutība ir 55-95%, specifiskums līdz 88%). Daudzkodolu milzu šūnas (svešķermeņa šūnu veids) var atrast arī ALS pacientiem ar sarkoidozi.
Rīsi. 9. ALS citogrammas neitrofīlais tips. Krāsošana pēc Romanovska teiktā. x1000, eļļas iegremdēšana.
Ar ārstnieciskām alveolām
Tādējādi morfoloģiskās izmaiņas plaušās var būt dažādas, bieži tiek novērots alveolārais hemorāģiskais sindroms jeb ABOP. ALS citogrammā var atzīmēt eozinofilu un neitrofilu īpatsvara pieaugumu, bet visbiežāk ar LA opi-
2. tabula. ALS citoloģiskās analīzes izmantošanas piemēri diferenciāldiagnozei (saskaņā ar OgeP M. et al., 2000)
Citogrammas indikatori
ALS un to novērtējums
ALS citogrammas klīniskie piemēri
Citoze, x104/ml 29 110 100 20 64
Makrofāgi, % 65,8 18,2 19,6 65,7 41,0
Limfocīti, % 33,2 61,6 51,0 14,8 12,2
Neitrofīli, % 0,6 12,8 22,2 12,4 4,2
Eozinofīli, % 0,2 6,2 7,0 6,8 42,2
Mastu šūnas, % 0,2 1,0 0,2 0,3 0,4
Plazmocīti, % 0 0,2 0 0 0
CO4+/CO8+ attiecība 3,6 1,8 1,9 2,8 0,8
Baktēriju kultūra - - - - -
Visticamākā diagnoze ir sarkoidoze EAA LA ELISA OEP
Pareizas diagnozes varbūtība*, % 99,9 99,6 98,1 94,3 Nav aprēķināts
*Aprēķināts, izmantojot matemātisko modeli. Apzīmējumi: AEP - akūta eozinofīlā pneimonija.
norāda uz limfocītu procentuālā daudzuma palielināšanos, starp kuriem, kā likums, dominē CD8+ šūnas. Ļoti augsts neitrofilu saturs BAS rodas, lietojot antidepresantu nomifensīnu (neitrofilu īpatsvars var sasniegt 80%, kam seko sekojošs limfocītu skaita samazinājums un vienlaicīga palielināšanās). Lietojot amiodaronu LA (“amiodarona plaušas”), rodas specifiskas BAS izmaiņas, kas izpaužas kā liels skaits “putojošu” makrofāgu (7. att.). Tā ir ļoti jutīga, bet mazspecifiska pazīme: tos pašus makrofāgus var konstatēt arī pie citām slimībām (EAA, OBOP), kā arī pacientiem, kuri lieto amiodaronu, ja nav alveolīta (amiodarons palielina fosfolipīdu saturu, īpaši fagocītos). ).
Citos gadījumos, kad BAL neatklāj īpaši specifiskas slimības pazīmes, šī metode ļauj ierobežot diferenciāldiagnostikas meklēšanu (2. un 3. tabula) ar noteiktu nosoloģisko vienību grupu ar vienu vai otru alveolīta veidu:
Limfocīti (palielināts limfocītu īpatsvars, 8. att.): sarkoidoze, paaugstinātas jutības pneimonīts, pēcradiācijas pneimonija, ELISA, hronisks infekcijas process plaušās, AIDS, silikoze, Sjogrena sindroms, Krona slimība, karcinomatoze, zāļu izraisīta pneimopātija;
Neitrofīli (palielināts neitrofilu īpatsvars, 9. att.): sklerodermija, dermatomiozīts, akūts infekciozs process plaušās, sarkoidoze ļaundabīgā gaitā, azbestoze, zāļu izraisīts alveolīts;
Eozinofīls (palielināts eozinofilu īpatsvars, 10. att.): Šerja-Štrausa angiīts, eozinofīlā pneimonija, zāļu izraisīts alveolīts;
Jaukti (11. att.): tuberkuloze. histiocitoze.
Diagnosticējot plaušu vēzi, BAL metodei ir priekšrocība
3. tabula. ALS citoloģiskie rādītāji ir normāli un to izmaiņas dažādu patoloģiju gadījumā (saskaņā ar OgeP M. et al., 2000)
Alveolārie makrofāgi Limfocīti Neitrofīli Eozinofīli Plazmocīti Tuklo šūnas CD4+/CD8+ attiecība
Normālās vērtības
Nesmēķētāji 9,5-10,5* 0,7-1,5* 0,05-0,25* 0,02-0,08* 0* 0,01-0,02* 2,2-2,8
85-95% 7,5-12,5% 1,0-2,0% 0,2-0,5% 0% 0,02-0,09%
Smēķētāji 25-42* 0,8-1,8* 0,25-0,95* 0,10-0,35* 0* 0,10-0,35* 0,7-1,8
90-95% 3,5-7,5% 1,0-2,5% 0,3-0,8% 0% 0,02-1,0%
Neinfekcijas slimības
Sarkoidoze T = =/T - =/T T/=/4
EAA “Putu” MF TT T =/T +/- TT 4/=
Zāļu “Putu” MF TT T T +/- TT 4/=
alveolīts
ELISA T T/TT T - T =
OBOP “putojošs” MF T T T -/+ =/T 4
Eozinofīls T = TT +/- =/T 4
pneimonija
Alveolārais “putotais” MF T = = - N.d. T/=
proteīnoze
Locītavu slimības - T =/T =/T - =/T T/=/4
ķermeņa audums
Pneimokonioze VKV (daļiņas) T T =/T - =/T T/=/4
Difūzā alveo- Krāsa =/T T =/T - N.d. =
asiņošana uz Fe: +++
ARDS krāsviela Fe: + T TT T - =/T 4/=
Ļaundabīgi audzēji
Adenokarcinoma = = = - = =
Vēža limfangīts T T/= T/= -/+ T/= 4/=
Hemoblastoze T T T -/+ T 4/=
Un infekcijas
Baktēriju BCV (baktērijas) = TT T - N.d. =
Vīrusu VKV T T T - N.d. T/=
Tuberkuloze BCV (mikobaktērijas) T = T - T =
HIV VKV T T T/= - N.d. 4
Apzīmējumi: MF - makrofāgi, VKV - intracelulāri ieslēgumi; indikators: T - palielināts; TT - ievērojami palielināts; 4 - samazināts; =/T - nav mainīts, retāk palielināts; T/=/4 - var palielināt, samazināt vai nemainīt; T/TT - palielināts, retāk būtiski palielināts; T/= - palielināts, retāk nemainīgs; 4/= - samazinājies, retāk nemainīts; = - nav mainīts; - Nē; -/+ - reti; +/- rodas; N.d. - nav datu.
* Dati ir uzrādīti absolūtos skaitļos x104ml-1.
pirms krēpu pārbaudes, lai noteiktu audzēja šūnas, jo materiāls var būt
iegūts no daivas vai segmenta, kurā audzējs ir lokalizēts. BAL padara to ticamāku
diagnosticēt perifēros audzējus, tostarp bronhioloalveolāro vēzi (12. att.).
Rīsi. 10. ALS citogrammas eozinofīlais tips, Char-co-Leiden kristāli. Krāsošana pēc Romanovska teiktā. x200.
Rīsi. 11. Jaukta tipa ALS citogramma: palielināts limfocītu, neitrofilu, eozinofilu īpatsvars. Krāsošana pēc Romanovska teiktā. x1000, eļļas iegremdēšana.
Rīsi. 13. ALS hroniska bronhīta gadījumā: cilindrisku skropstu šūnu, neitrofilu klātbūtne, koku floras uzkrāšanās. Krāsošana pēc Romanovska teiktā. x1000, eļļas iegremdēšana.
Rīsi. 14. Mycobacterium tuberculosis ALS gadījumā. Ziehl-Neelsen krāsošana. x1000, eļļas iegremdēšana.
Rīsi. 15. Candida albicans sēnītes pseidomicēlija ALS gadījumā. Krāsošana pēc Romanovska teiktā. x200.
Citobakterioskopiskā metode ļauj identificēt un daļēji kvantitatīvi novērtēt baktēriju (13. att.), mikobaktēriju (14. att.) un sēnīšu (15. att.) saturu BAS. Šie rezultāti (baktērijas var atšķirt pēc grama) kalpo par pamatu atbilstošas antibakteriālās terapijas nozīmēšanai līdz bakterioloģiskās izmeklēšanas rezultātu iegūšanai. Kazuistiski
Rīsi. 16. Ievērojams neitrofilu skaita pieaugums ALS, daudzu vienšūņu, piemēram, amēbu, skaita pieaugums. Krāsošana pēc Romanovska teiktā. x200.
BAS izpēte ļauj novērtēt infekcijas slimību iekaisuma procesa aktivitātes pakāpi un terapijas efektivitāti. Zemai iekaisuma aktivitātes pakāpei raksturīgs neitrofilu īpatsvara pieaugums BAS 10% robežās.
vidējs - līdz 11-30%, augsts - vairāk nekā 30%.
Histoķīmisko metožu izmantošana BAL šūnu pētīšanai ir iespējama, ja to dzīvotspēja ir augsta (vairāk nekā 80%).
Secinājums
Novērtējot BS un BAS konstatētās izmaiņas, jums jāievēro noteikti noteikumi un jāatceras:
Konstatētās izmaiņas ir raksturīgas tikai pētāmajam segmentam, tāpēc pret tām jāizturas piesardzīgi, ja procesam nav difūza rakstura;
Identificētās izmaiņas ir raksturīgas konkrētam laika punktam;
Tā kā plaušas vienlaikus ir pakļautas daudziem faktoriem (smēķēšana, piesārņotāji utt.), vienmēr ir jāizslēdz iespēja, ka šie faktori varētu ietekmēt plaušu patoloģijas attīstību.
Čerņajevs A.L., Samsonova M.V. Plaušu patoloģiskā anatomija: Atlas / Red. Čučaļina A.G. M., 2004. gads.
Šapiro N.A. Plaušu slimību citoloģiskā diagnostika: Krāsu atlants. T. 2. M., 2005. gads.
Baughman R.P Bronhoalveolārais skalošana. Sv. Luiss, 1992. gads.
Costabel U. Bronhoalveolārā skalošanas atlants. L., 1998. gads.
Drent M. et al. //Eiro. Resp. Monogrāfija. V 5. Pirmd. 14. Hadersfīlda, 2000. 63. lpp.
Grāmatas no izdevniecības “ATMOSPĒJA”
Amelīna E.L. uc Mukoaktīvā terapija /
Ed. A.G. Čučaļina, A.S. Beļevskis
Monogrāfijā apkopoti mūsdienu priekšstati par mukociliārā klīrensa uzbūvi un funkcionēšanu, tā traucējumiem dažādu elpceļu slimību gadījumā, pētījumu metodēm; Aplūkotas galvenās ārstnieciskās un nemedicīniskās metodes mukociliārā klīrensa koriģēšanai bronhopulmonārās patoloģijas gadījumā. 128 lpp., ill.
Ģimenes ārstiem, terapeitiem, pulmonologiem, medicīnas studentiem.
Ideja par bronhu skalošanu, lai iztukšotu saturu, pieder Klinam un Vinternicam (1915), kuri veica BAL eksperimentālās pneimonijas gadījumā. Klīnikā Jēls 1922. gadā pirmo reizi veica bronhoalveolāro skalošanu kā terapeitisku procedūru, proti, lai ārstētu saindēšanos ar fosgēnu, lai izvadītu bagātīgus sekrētus. Vincente Garcia 1929. gadā izmantoja no 500 ml līdz 2 litriem šķidruma bronhektāzēm, plaušu gangrēnai un svešķermeņiem elpceļos. Galmay 1958. gadā izmantoja masīvu skalošanu pēcoperācijas atelektāzei, kuņģa satura aspirācijai un asiņu klātbūtnei elpceļos. Broom 1960. gadā veica bronhu skalošanu caur endotraheālo caurulīti. Tad viņi sāka izmantot dubultlūmena caurules.
1961. gadā Q.N. Myrvik et al. Eksperimentā alveolāro makrofāgu iegūšanai tika izmantota elpceļu skalošana, ko var uzskatīt par svarīgas diagnostikas metodes - bronhoalveolārās skalošanas - dzimšanu. Pirmo reizi skalošanas šķidruma izpēti, kas iegūta, izmantojot stingru bronhoskopu, veica R.I. Keimowitz (1964) par imūnglobulīnu noteikšanu. T.N. Finlijs et al. (1967) izmantoja Metra balonkatetru, lai iegūtu sekrēcijas un pētītu tās pacientiem ar hronisku obstruktīvu plaušu slimību. 1974. gadā H.J. Reinolds un H.H. Ņūbols pirmo reizi saņēma šķidrumu pētījumam šķiedru bronhoskopijas laikā, kas tika veikta vietējā anestēzijā.
Bronhoalveolārā skalošana ir papildu pārbaude, lai noteiktu plaušu slimības raksturu. Bronhoalveolārā skalošana ir procedūra, kurā elpceļu bronhoalveolārais rajons tiek mazgāts ar izotonisku nātrija hlorīda šķīdumu. Šī ir šūnu un šķidruma iegūšanas metode no dziļām plaušu audu daļām. Bronhoalveolārā skalošana ir nepieciešama gan fundamentālajiem pētījumiem, gan klīniskiem nolūkiem.
Pēdējos gados ievērojami pieaudzis patoloģisko procesu biežums, kura galvenais simptoms ir pieaugošs elpas trūkums.
Diagnostiskā bronhoalveolārā skalošana ir indicēta pacientiem, kuriem krūškurvja rentgenogrammā atklājas neskaidras izmaiņas plaušās, kā arī difūzas izmaiņas. Difūzās intersticiālās plaušu slimības ir vislielākais izaicinājums ārstiem, jo to etioloģija bieži nav zināma.
Bronhoalveolāras skalošanas indikācijas ir gan intersticiāla infiltrācija (sarkoidoze, alerģisks alveolīts, idiopātiska fibroze, histiocitoze X, pneimokonioze, kolagenoze, karcinomatozs limfangīts), gan alveolāra infiltrācija (pneimonija, alveolāra asiņošana, bronhi obstruktīvs arproteolīts, alveolārais terafīts).
Neskaidras izmaiņas var būt infekciozas, neinfekciozas vai ļaundabīgas etioloģijas. Pat gadījumos, kad skalošana nav diagnostiska, tās rezultāti var likt domāt par diagnozi, un tad ārsta uzmanība tiks vērsta uz nepieciešamajiem turpmākajiem pētījumiem. Piemēram, pat parastā skalošanas šķidrumā pastāv liela varbūtība atklāt dažādas novirzes. Nākotnē bronhoalveolārā skalošana tiek potenciāli izmantota slimības aktivitātes pakāpes noteikšanai, prognozes un nepieciešamās terapijas noteikšanai.
Ar katru gadu bronhoalveolārā skalošana arvien vairāk tiek izmantota dažādu plaušu slimību, piemēram, cistofibrozes, alveolārās mikrolitiāzes, alveolārās proteinozes, lipoīdu pneimonijas ārstēšanā.
Pēc visu bronhu pārbaudes bronhoskops tiek ievietots segmentālajā vai subsegmentālajā bronhā. Ja process ir lokalizēts, tad attiecīgie segmenti tiek mazgāti; difūzām slimībām šķidrums tiek ievadīts vidējās daivas vai lingulāro segmentu bronhos. Šo sekciju skalošanas rezultātā iegūtais kopējais šūnu skaits ir lielāks nekā apakšējās daivas skalošanas rezultātā.
Procedūra tiek veikta šādi. Bronhoskops tiek nogādāts subsegmentālā bronha mutē. Kā skalošanas šķidrumu izmanto sterilu izotonisku nātrija hlorīda šķīdumu, kas uzkarsēts līdz 36-37°C temperatūrai. Šķidrumu ievieto caur īsu katetru, kas ievietots caur bronhoskopa biopsijas kanālu, un nekavējoties tiek aspirēts silikonizētā traukā. Nav ieteicams lietot parasto stikla kausu, jo alveolārie makrofāgi pielīp pie tā sieniņām.
Parasti atkārtoti ievada 20-60 ml šķidruma, kopā 100-300 ml. Iegūtā skalošanas tilpums ir 70-80% no ievadītā fizioloģiskā šķīduma tilpuma. Iegūto bronhoalveolāro skalošanu nekavējoties nosūta uz laboratoriju, kur to 10 minūtes centrifugē ar ātrumu 1500 apgr./min. No nogulsnēm sagatavo uztriepes, kuras pēc žāvēšanas fiksē ar metilspirtu vai Ņikiforova maisījumu un pēc tam nokrāso pēc Romanovska. Gaismas mikroskopā, izmantojot eļļas tehnoloģiju, tiek saskaitītas vismaz 500-600 šūnas, diferencējot alveolāros makrofāgus, limfocītus, neitrofilus, eozinofilus un citas šūnas.
Bronhoalveolārā skalošana, kas ņemta no iznīcināšanas vietas, nav piemērota slimības patoģenētisko mehānismu izpētei, jo tā satur šūnu detrītu, lielu skaitu neitrofilu, intracelulāros enzīmus un citus audu sabrukšanas elementus. Tāpēc, lai izpētītu ALS šūnu sastāvu, ir jāņem tamponi no plaušu segmentiem, kas atrodas blakus iznīcināšanai.
BAS, kas satur vairāk nekā 5% bronhu epitēlija un/vai 0,05 x 10 šūnas uz 1 ml, netiek analizēts, jo saskaņā ar W. Eschenbacher et al. (1992), šie rādītāji ir raksturīgi mazgāšanai, kas iegūta no bronhiem, nevis no bronhoalveolārās telpas.
Bronhoalveolārā skalošana ir vienkāršs, neinvazīvs un labi panesams tests. Presē ir bijis tikai viens ziņojums par pacientu, kurš miris no akūtas plaušu tūskas un septiskā šoka bronhoalveolārās skalošanas dēļ. Autori izvirza hipotēzi, ka šī pacienta stāvokļa straujā pasliktināšanās ir saistīta ar masveida iekaisuma mediatoru izdalīšanos, kā rezultātā rodas plaušu tūska un vairāku orgānu mazspēja.
Lielākā daļa ziņojumu par bronhoalveolārās skalošanas komplikācijām ir saistītas ar komplikācijām bronhoskopijas laikā vai ir atkarīgas no ievadītā šķidruma tilpuma un temperatūras. Ar BAL saistītās komplikācijas ir klepus procedūras laikā un pārejošs drudzis dažas stundas pēc pārbaudes. Kopējais bronhoalveolārās skalošanas komplikāciju biežums nepārsniedz 3%, palielinās līdz 7%, veicot transbronhiālo biopsiju un sasniedz 13% gadījumos, kad tiek veikta atvērta plaušu biopsija.
Bronhoalveolārā diagnostikas skalošana ir pētījumu metode, kas nodrošina šūnu elementu, olbaltumvielu un citu vielu ekstrakciju no mazāko bronhu un alveolu virsmas, aizpildot plaušu apakšsegmentu ar izotonisku šķīdumu, kam seko aspirācija. Diagnostiskā subsegmentālā bronhoalveolārā skalošana parasti tiek veikta bronhofibroskopijas laikā vietējā anestēzijā pēc bronhofibroskopa nogādāšanas subsegmentālā bronha mutē. Caur bronhofiberskopa kanālu subsegmentālajā bronhā tiek iepilināts 50-60 ml izotoniska šķīduma. Šķidrums, kas nāk no bronhu lūmena, kas ir bronhu-alveolārais skalošana, tiek aspirēts caur bronhofiberskopa kanālu plastmasas glāzē. Instilāciju un aspirāciju atkārto 2-3 reizes. Aspirētajā šķidrumā, kas attīrīts no gļotām, filtrējot caur marli, tiek pētīts šūnu un olbaltumvielu sastāvs un alveolāro makrofāgu funkcionālā aktivitāte. Lai izpētītu šūnu sastāvu, bronhoalveolāro skalošanu centrifugē. Uztriepes sagatavo no nogulsnēm un krāso ar hematoksilīna-eozīnu vai Romanovski. Plaušu diseminēto procesu aktivitātes noteikšanai biežāk izmanto diagnostisko bronhoalveolāro skalošanu. Augstas idiopātiskā fibrozējošā alveolīta aktivitātes pazīme ir ievērojams neitrofilu skaita pieaugums bronhoalveolārajā skalā, bet sarkoidozes un eksogēnā alerģiskā alveolīta gadījumā - limfocītu skaita palielināšanās.
BRONHALVEOLĀRĀ MEDICĪNISKĀ skalošana
Plaušu slimību ārstēšanas metode, kuras pamatā ir liela daudzuma izotoniska šķīduma endobronhiāla ievadīšana un gļotu, olbaltumvielu un cita mazo bronhu un alveolu satura izskalošana. Terapeitisko bronhoalveolāro skalošanu var veikt caur bronhoskopu vai dubultlūmena endotraheālo cauruli. Procedūra parasti tiek veikta anestēzijā. Plaušu mākslīgā ventilācija tiek veikta, izmantojot injekcijas metodi. Izotonisks šķīdums tiek secīgi iepilināts katrā lobārajā vai segmentālajā bronhā caur kontrolētu katetru un nekavējoties tiek aspirēts kopā ar izskaloto viskozu sekrēciju un gļotu recekļiem. Bronhoskopisko metodi biežāk izmanto pacientiem ar bronhiālo astmu astmas stāvoklī. Bronhu mazgāšanai izmanto 500-1500 ml izotoniskā šķīduma. Parasti ir iespējams aspirēt apmēram 1/3 - 1/2 no ievadītā šķidruma tilpuma. Terapeitiskās bronhoalveolārās skalošanas indikācijas pacientiem ar bronhiālo astmu rodas reti, jo citu terapeitisko pasākumu komplekss parasti palīdz atvieglot astmas stāvokli.
Terapeitiskā bronhoalveolārā skalošana caur dubultlūmena endotraheālo caurulīti tiek veikta ar vienas plaušu mākslīgo ventilāciju. Endotraheālās caurules lūmenā galvenajā bronhā ievieto katetru, caur kuru tiek veikta izotoniskā šķīduma instilācija un aspirācija. Uzreiz plaušās ievada 1000-1500 ml šķīduma, un 90-95% no ievadītā šķidruma tilpuma tiek aspirēti atpakaļ. Procedūru atkārto vairākas reizes. Kopējais ievadītā šķidruma tilpums svārstās no 3-5 līdz 40 litriem. Kopēja bronhoalveolāra skalošana caur dubultlūmena endotraheālo cauruli ir visefektīvākā idiopātiskās alveolārās proteinozes ārstēšana.
Direktorija pulmonoloģijā / Red. N. V. Putova, G. B. Fedosejeva, A. G. Homenko. - L.: Medicīna