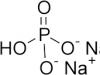
ICD kodi - 10
Dž 13- Dž 18
Lekcijas mērķis ir Pamatojoties uz iegūtajām zināšanām, veikt pneimonijas diagnozi, veikt diferenciāldiagnozi ar citām plaušu slimībām, formulēt diagnozi un izrakstīt personalizētu ārstēšanu konkrētam pneimonijas pacientam.
Lekcijas konspekts
Klīniskais gadījums
Pneimonijas definīcija
Pneimonijas epidemioloģija
Sabiedrībā iegūtās pneimonijas etioloģija, patoģenēze, patomorfoloģija
Nozokomiālās pneimonijas etioloģija, patoģenēze, patomorfoloģija
Pneimonijas klīnika
Pneimonijas komplikācijas
Pneimonijas diferenciāldiagnoze
Pneimonijas klasifikācija
Pneimonijas ārstēšana
Prognoze, pneimonijas profilakse
Pacients P., 64 gadus vecs,
sūdzējās par klepu ar nelielu dzeltenīgi zaļu krēpu daudzumu, ķermeņa temperatūras paaugstināšanos līdz 38,3ºC, sāpēm krūškurvja labajā pusē, kas rodas klepojot un dziļi ieelpojot, vispārēju nespēku, elpas trūkumu ar mērenu fizisko slodzi aktivitāte, svīšana un galvassāpes. Es saslimu akūti pirms 3 dienām, pēc hipotermijas. Apmeklējot vietējo klīniku, ārsts izrakstīja gentamicīnu 80 mg IM 2 reizes dienā, mukaltīnu 3 tabletes dienā un aspirīnu. Ārstēšanas laikā netika novērota nozīmīga pozitīva dinamika.
Pacients ir bijušais militārists, šobrīd pensijā, strādā par sargu. Viņš 22 gadus izsmēķē 1,5 – 2 cigarešu paciņas dienā. Periodiski (2-3 reizes gadā) pēc hipotermijas vai akūtas elpceļu vīrusu infekcijas viņš pamana klepus parādīšanos ar dzelteni zaļu krēpu izdalīšanos; pēdējos 2 gados ir parādījies elpas trūkums ar mērenu fizisko slodzi.
Pārbaudē: stāvoklis ir vidēji smags, āda ir tīra, mērens mitrums, tiek atzīmēta sejas ādas hiperēmija. Ķermeņa temperatūra - 39,1ºС. Zemādas tauku slānis ir vidēji attīstīts, nav tūskas, perifērie limfmezgli nav palielināti. RR miera stāvoklī –30/min. Krūtis ir emfizēmas, pārbaudot, uzmanība tiek pievērsta krūškurvja labās puses atpalicībai elpošanas laikā. Sitot plaušas uz kastes skaņas fona, labajā pusē zem lāpstiņas leņķa tiek noteikts truluma laukums, tajā pašā zonā palielinās balss trīce. Auskulācijas laikā ir dzirdami izkliedēti sausi sēkšana, labajā pusē zem lāpstiņas leņķa ir krepita zona. Sirds skaņas ir apslāpētas, nav trokšņu. Sirdsdarbības ātrums – 105 minūtē, asinsspiediens – 110/65 mm Hg. Vēders ir mīksts, nesāpīgs, pieejams palpācijai visās daļās. Aknas un liesa nav palielinātas. Nav dizūrisku traucējumu.
Asins analīze: hemoglobīns – 15,6 g/l; sarkanās asins šūnas – 5,1x10,12; hematokrīts – 43%; leikocīti – 14,4x10,9; p/o – 12%; s/ya – 62%; limfocīti – 18%; eozinofīli – 2%; monocīti – 6%; trombocīti-238x10,9; ESR – 28 mm/h Bioķīmiskā asins analīze: kreatinīna līmenis serumā 112 µmol/l, aknu bioķīmiskie rādītāji bez novirzēm no normas. Pulsa oksimetrija atklāja asins skābekļa piesātinājuma samazināšanos:Sao2 94%. Krēpu analīze: pēc būtības mukopurulents, leikocīti blīvi pārklāj redzes lauku; eozinofīli, Kurshman spirāles, Charcot-Leyden kristāli, BC – nav; Tiek noteikti grampozitīvi diplokoki. Spirometrija atklāja FEV1 samazināšanos līdz 65% no normālās vērtības (bronhu obstrukcijas pazīme). Krūškurvja orgānu rentgenogrāfija divās projekcijās: plaušu audu aptumšošanas (infiltrācijas) zona labās plaušas apakšējā daivā (6,9,10 segmenti), plaušu emfizēma, palielināts plaušu modelis, ko izraisa tiek noteikts intersticiālais komponents.
Tādējādi pacientam ir akūtas apakšējo elpceļu slimības simptomi un anamnēzē ir recidivējoši elpceļu sindromi (klepus un elpas trūkums). Jārisina šādi uzdevumi: diagnostiskā - noteikt galvenās un blakusslimības nozoloģisko formu un terapeitisko - noteikt ārstēšanu atbilstoši noteiktajai diagnozei.
Pneimonijas definīcija
Pneimonija - akūtu infekcijas slimību grupa (galvenokārt bakteriāla) ar atšķirīgu etioloģiju, patoģenēzi un morfoloģiskām īpašībām, kam raksturīgi plaušu elpceļu daļu fokālie bojājumi ar obligātu intraalveolāru eksudāciju; iekaisuma reakcijas attīstība plaušu audos ir makroorganisma aizsargmehānismu pārkāpuma sekas uz masveida mikroorganismu ar paaugstinātu virulenci iedarbību fona.
Kopienā iegūta pneimonija (CAP) - akūta slimība, kas radusies sabiedrībā vai vēlāk nekā 4 nedēļas pēc izrakstīšanās no slimnīcas, vai diagnosticēta pirmo 48 stundu laikā pēc hospitalizācijas, vai attīstījusies pacientam, kurš neatradās pansionātos/ilgstošās medicīniskās aprūpes nodaļās. vairāk nekā 14 dienas, ko pavada apakšējo elpceļu infekcijas simptomi (drudzis, klepus, krēpu izdalīšanās, sāpes krūtīs, elpas trūkums), svaigu fokusa infiltratīvu izmaiņu radioloģiskās pazīmes plaušās, ja nav diagnostikas alternatīvas.
Nozokomiālā pneimonija (NP) (slimnīcā iegūta, nozokomiāla) - slimība, kurai raksturīga "svaiga" fokāli infiltratīva izmaiņu parādīšanās plaušās 48 stundas vai ilgāk pēc hospitalizācijas kopā ar klīniskiem datiem, kas apstiprina infekciozu raksturu (jauns drudža vilnis, strutainas krēpas vai strutaini izdalījumi no traheobronhiālais koks, leikocitoze u.c.), izslēdzot infekcijas, kas bija NP inkubācijas periodā brīdī, kad pacients tika ievietots slimnīcā.
Ar veselības aprūpi saistīta pneimonija
Šajā kategorijā ietilpst pneimonija cilvēkiem, kas dzīvo pansionātos vai citās ilgtermiņa aprūpes iestādēs. Atbilstoši to rašanās apstākļiem tos var klasificēt kā sabiedrībā iegūtus, taču tie, kā likums, atšķiras no pēdējiem ar patogēnu sastāvu un to antibiotiku rezistences profilu.
Pneimonijas epidemioloģija
Saskaņā ar PVO datiem KLP ieņem 4. vietu mirstības cēloņu struktūrā. Saskaņā ar oficiālo statistiku Krievijā 1999.gadā 440 049 (3,9%) KLP gadījumi tika reģistrēti starp cilvēkiem, kas vecāki par 18 gadiem. 2003. gadā visās vecuma grupās saslimstība ar KLP bija 4,1%. Tiek pieņemts, ka šie skaitļi neatspoguļo patieso KLP sastopamību Krievijā, kas tiek lēsta 14–15%, un kopējais pacientu skaits gadā pārsniedz 1,5 miljonus cilvēku. Amerikas Savienotajās Valstīs katru gadu tiek diagnosticēti 5–6 miljoni KLP gadījumu, no kuriem vairāk nekā 1 miljonam ir nepieciešama hospitalizācija. Neskatoties uz progresu pretmikrobu terapijā, mirstības līmenis no pneimonija būtiski nesamazinājās. No pacientiem, kas hospitalizēti KLP dēļ, mirst vairāk nekā 60 tūkstoši cilvēku. Saskaņā ar Krievijas Federācijas Veselības ministrijas datiem, 2003. gadā mūsu valstī no plkst pneimonija Miruši 44 438 cilvēki, kas ir 31 gadījums uz 100 tūkstošiem iedzīvotāju.
NP aizņem 13-18% no visām nozokomiālajām infekcijām un ir visizplatītākā infekcija ICU (vairāk nekā 45%). Ar ventilatoru saistītā pneimonija (VAP) rodas 9–27% intubētu pacientu.
Attiecināmā mirstība (tieši saistīta ar NP) svārstās no 10 līdz 50%.
KLP etioloģija, patoģenēze, patomorfoloģija
KLP etioloģija
Kopienā iegūta pneimonija kā patstāvīga nozoloģiska forma tā ir infekcijas slimība, kuras galvenais morfoloģiskais substrāts ir eksudatīvs iekaisums plaušu respiratorajās daļās bez plaušu audu nekrozes. CAP etioloģija ir tieši saistīta ar normālu mikrofloru, kas kolonizē augšējos elpceļus. No daudzajiem mikroorganismiem tikai dažiem ir pneimotropisms un paaugstināta virulence, un tie spēj izraisīt iekaisuma reakciju, kad tie nonāk apakšējos elpceļos.
Runājot par etioloģiskās nozīmes biežumu starp KLP izraisītājiem, S. pneimonijaie (30-50%); M. Pneimonijas, C. pneumoniae, Legionela tiek noteiktas ar biežumu no 8 līdz 30%, retāk sastopami patogēni (H. gripa, S. aureUns, Klebsiellaun citas enterobaktērijas ir sastopami 3-5%. Mikroorganismi, kas mīt augšējos elpceļos un nav KLP cēloņi, ir: Streptokoks viridans, Stafilokoks epidermidis, Enterokoku, Neisseria, Candida. Bieži vien pieaugušiem pacientiem, kuriem tiek veikta KLP, tiek konstatēta jaukta vai vienlaicīga infekcija, piemēram, slimības pneimokoku etioloģijas kombinācija un vienlaikus aktīvas mikoplazmas vai hlamīdiju infekciju seroloģisko pazīmju noteikšana. Elpceļu vīrusi bieži neizraisa tiešus plaušu elpošanas daļu bojājumus. Vīrusu elpceļu infekcijas, galvenokārt epidēmiskā gripa, tiek uzskatītas par galveno KLP riska faktoru. KLP var būt saistīta ar jauniem, iepriekš nezināmiem patogēniem, kas izraisa slimību uzliesmojumus. Pēdējos gados identificētie KLP izraisītāji ir Ar SARS saistītais koronavīruss, putnu gripas vīruss (H5N1), cūku gripas vīruss (H1N1) un metapneumovīruss.
Ir jānošķir vīrusu izraisītas patoloģiskas intersticiālas izmaiņas plaušu audos no pašas bakteriālās pneimonijas, jo pieeja šo divu stāvokļu ārstēšanai būtiski atšķiras. KLP etioloģiskā struktūra var atšķirties atkarībā no pacientu vecuma, slimības smaguma pakāpes un blakusslimību klātbūtnes. No praktiskā viedokļa ir ieteicams identificēt pacientu grupas ar KLP un iespējamiem patogēniem
Nesmaga KLP personām bez blakusslimībām, kuras pēdējo 3 mēnešu laikā nav lietojušas pretmikrobu zāles.
Iespējamie patogēni : S pneumoniae, M. Pneimonijas, C. pneumoniae, H. Gripas.
Nesmaga KLP personām ar blakusslimībām ( HOPS, cukura diabēts, sastrēguma sirds mazspēja, cerebrovaskulāras slimības, difūzās aknu slimības, nieru darbības traucējumi, hronisks alkoholisms u.c.) un/vai pēdējo 3 mēnešu laikā esat lietojis pretmikrobu zāles.
Iespējamie patogēni : S. pneumoniae, H. gripa, C. pneumoniae, S. aureus, Enterobacteriaceae. Ir iespējama ambulatorā ārstēšana (no medicīniskā viedokļa).
Nesmagas plūsmas VP, lārstēšana slimnīcās (vispārējā nodaļa).
Iespējamie patogēni : S. pneumoniae, H. Gripas, C. pneumoniae, M. Rneumonijas, S. aureus, Enterobacteriaceae.
Smags VP,ārstēšana slimnīcā (ICU).
Iespējamie patogēni : S. pneumoniae, Legionella, S. aureus, Enterobacteriaceae.
KLP riska faktori:
saskare ar gaisa kondicionēšanas sistēmām;
gripas epidēmijas;
neattīrīts mutes dobums;
uzliesmojums slēgtā grupā;
atkarība.
hipotermija;
intoksikācija;
gāze vai putekļi, kas kairina elpceļus;
|
Zināmas etioloģijas KLP attīstības epidemioloģija un riska faktori |
|
|
Notikuma apstākļi |
Iespējamie patogēni |
|
Alkoholisms |
S. pneumoniae, anaerobi, Klebsiella pneumoniae, Acinetobacter, Micobacterium tuberculosis. |
|
HOPS/smēķēšana |
Haemophilus influenzae, Pseudomonas aerugenosa, Legionella sugas, Moraxella catarrhalis, Chlamidophila pneumoniae, S. pneumoniae |
|
Tiekšanās |
Gramnegatīvās enterobaktērijas, anaerobi. |
|
Kopienā iegūti MRSA celmi, Micobacterium tuberculosis, anaerobi, sēnīšu pneimonija, netipiskas mikobaktērijas. |
|
|
Sazināties ar gaisa kondicionieriem, gaisa mitrinātājiem, ūdens dzesēšanas sistēmām |
Legionellu sugas |
|
Gripas epidēmija |
S. pneumoniae, Staphylococcus aureus, Haemophilus influenzae |
|
KLP attīstība uz bronhektāzes, cistiskās fibrozes fona |
Pseudomonas aerugenosa, Burkhoideriacepacipa, S/aureus, |
|
Intravenozās narkomāni |
S. aureus, Micobacterium tuberculosis, S. Pneumoniae. |
|
Vietējā bronhu obstrukcija (bronhu audzējs) |
S. pneumoniae, Haemophilus influenzae, S. aureus. |
|
Bioterorisms |
Sibīrijas mēris, mēris, tularēmija. |
Pacients A.
simptomi, kas bija apmeklējuma iemesls, akūti attīstījās kopienas vidē. Pastāv pneimonijas riska faktori - ilgstoša smēķēšanas vēsture ar smēķētāju indeksu aptuveni 20 gadi, patoloģijas pazīmes, kas predisponē pneimonijas attīstību - atkārtotas klepus un elpas trūkuma epizodes, tieksme uz “saaukstēšanos”.
KLP patoģenēze
70% veselu cilvēku orofarneksā kolonizē mikroorganismi. Tie ir pneimokoki, gripas bacilis un Staphylococcus aureus. Orofaringeālo sekrēciju mikroaspirācija fizioloģiskos apstākļos tiek novērota arī veseliem indivīdiem, galvenokārt miega laikā. Apakšējo elpceļu pretinfekcijas aizsardzību veic ar aizsargmehānismiem: mehāniskiem (aerodinamiskā filtrācija, bronhu anatomiskā atzarošanās, epiglottis, klepus, šķaudīšana, cilindriskā epitēlija skropstu vibrācija), specifiskas un nespecifiskas imunitātes mehānismi. Pateicoties šīm sistēmām, tiek nodrošināta inficēto sekrēciju izvadīšana no apakšējiem elpceļiem un nodrošināta to sterilitāte. Pneimonijas attīstību var veicināt, pirmkārt, makroorganisma aizsargmehānismu efektivitātes samazināšanās, otrkārt, devas masivitāte un/vai patogēna virulence.
Galvenie patoģenētiskie mehānismi Austrumu partnerības attīstība ir:
nazofaringeāla sekrēta aspirācija, kas satur iespējamos pneimonijas patogēnus;
aerosolu saturošu mikroorganismu ieelpošana;
hematogēna un limfogēna infekcijas izplatīšanās no ekstrapulmonāla fokusa (sepse, trikuspidālā vārstuļa endokardīts, tromboflebīts);
tieša infekcijas izplatīšanās no kaimiņu orgāniem (aknu abscess utt.);
infekcija, ko izraisa iekļūstošas krūšu brūces.
Orofaringeālo sekrēciju aspirācija
Kad traheobronhiālā koka “pašattīrīšanās” mehānismi tiek bojāti, piemēram, elpceļu vīrusu infekcijas laikā, kad tiek traucēta skropstu epitēlija funkcija un samazināta alveolāro makrofāgu fagocītiskā aktivitāte, tiek radīti labvēlīgi apstākļi. pneimonijas attīstība .
Aspirācija b Lielu daudzumu satura no orofarneksa un/vai kuņģa var pavadīt trīs sindromu attīstība atkarībā no aspirāta rakstura: ķīmiskais pneimonīts (sālsskābes aspirācija - Mendelsona sindroms), mehāniska obstrukcija, aspirācijas pneimonija, kas attīstās, kad bakteriāla infekcija ir saistīta ar mehānisku obstrukciju un ķīmisku pneimonītu. Faktori, kas veicina aspirāciju: samaņas nomākums, gastroezofageālais reflukss, atkārtota vemšana, nazofarneksa anestēzija, mehāniski aizsargbarjeru pārrāvumi.
Mikroorganismus saturošu aerosolu ieelpošana
Šim pneimonijas attīstības mehānismam ir liela nozīme apakšējo elpceļu inficēšanā ar obligātajiem patogēniem, piemēram, Legionella.
Nosacījums, kas veicina mikrofloras vairošanos apakšējos elpceļos, ir pārmērīga gļotu veidošanās, kas pasargā mikrobus no aizsargfaktoru iedarbības un veicina kolonizāciju. Ja tiek pakļauti riska faktoriem (hipotermija, elpceļu vīrusu infekcija u.c.) un traucēti aizsargmehānismi
tiek pārvarētas aizsargbarjeras ceļā no nazofarneksa uz alveolām, patogēns iekļūst plaušu elpošanas sekcijās un sākas iekaisuma process neliela fokusa veidā.
VP patomorfoloģija
Iekaisuma process attīstās plaušu elpceļu daļās - plaušu anatomisko struktūru komplektā, kas atrodas distāli no gala bronhioliem, kas ir tieši iesaistīti gāzu apmaiņā. Tie ietver elpceļu bronhiolus, alveolu maisiņus, alveolu kanālus un pašus alveolus. Papildus gaisu saturošajām telpām plaušu elpošanas daļa ietver bronhiolu, acini un alveolu sienas, t.i. intersticiālas struktūras, kurās var attīstīties arī infekcijas process. Eksudatīvs iekaisums plaušu respiratorajā daļā nosaka galveno pneimonijas radioloģisko pazīmi - lokālu plaušu audu gaisīguma samazināšanos (“aptumšošana”, “samazināta plaušu lauka caurspīdīgums”, “blīvēšanās”, “infiltrācija”). Pneimonijas fokusa lokalizācija bieži ir vienpusēja, apakšējās daivas vai augšējo daivu paduses apakšsegmentos, infiltrācijas izplatīšanās notiek viena līdz divu bronhopulmonāro segmentu robežās. Šī infiltratīvo izmaiņu lokalizācija atspoguļo galveno KLP attīstības patoģenētisko mehānismu - patogēno patogēnu aspirāciju vai ieelpošanu plaušās ar gaisu caur elpošanas ceļiem. Divpusējas izmaiņas vairāk raksturīgas plaušu tūskai, intersticiālām plaušu slimībām, ļaundabīgo audzēju metastāzēm plaušās, hematogēnai un limfogēnai plaušu infekcijai sepses laikā.
Atkarībā no patogēna KLP pastāv klīniskas un morfoloģiskas atšķirības.
Pneimokoku pneimonija
Par pneimoniju, ko izraisa endotoksīnu veidojošie patogēni(pneimokoks, Haemophilus influenzae, Klebsiella), process parasti sākas ar toksisku alveolu kapilāru membrānas bojājumu, izraisot baktēriju tūsku. I – III tipa pneimokoki var izraisīt gan sporādiskus, gan epidēmiskus saslimšanas gadījumus organizētās grupās baktēriju nesēju infekcijas dēļ. Pneimokoks iekļūst plaušu audos un asinsvadu gultnē, 25% pacientu tas tiek kultivēts no asinīm slimības pirmajās stundās. Pneimokoku pneimonijas I - III tipa patomorfoloģisko ainu raksturo kā lobāra vai pleiropneimonija, kas klasiski notiek trīs posmos: baktēriju tūskas stadijā, hepatizācijas stadijā un izšķirtspējas stadijā. Pirmajā posmā endotoksīna, kas izdalās pneimokoku nāves laikā, un enzīmu (hemolizīnu, hialuronidāzes) ietekmē tiek bojāta alveolārā kapilārā membrāna, palielinās asinsvadu caurlaidība, notiek plazmas svīšana un veidojas liels daudzums tūskas šķidruma, kas izplatās kā eļļas traips, no alveolām uz alveolām caur Kohna porām un gar bronhiem. Pneimokoki atrodas tūskas perifērijā, centrā veidojas no dīgļiem brīva fibrīna un strutojoša eksudāta zona. Atkarībā no ķermeņa reaktivitātes procesa izplatība ir segmentāla, polisegmentāla, lobāra, starpsumma. Otrā stadija parasti sākas 3-4 dienas no slimības sākuma, un tai raksturīga eritrocītu diapedēze, leikocītu infiltrācija un masīvs fibrīna zudums, kā rezultātā eksudāts alveolās no šķidruma pārvēršas blīvā, atgādinot aknas. audu blīvums (hepatizācijas vai hepatizācijas stadija). Šī posma ilgums ir no 5 līdz 7 dienām, dažreiz ilgāk, pēc tam sākas pneimonijas izzušanas stadija. Šajā posmā eksudāts tiek reabsorbēts, piedaloties plaušu fibrinolītiskajai sistēmai un neitrofilu proteolītiskajiem enzīmiem. Pneimokoku pneimonijas obligāta sastāvdaļa ir fibrīns pleirīts. Iespējama strutojoša bronhīta pievienošana.
Citu celmu pneimokoki izraisa attīstību fokusa pneimonija(bronhopneimonija). Iekaisuma process, kas galvenokārt notiek bronhos, izplatās uz plaušu parenhīmu, izplatoties gar bronhiem. Plaušu audos veidojas sarkanas un sarkani pelēkas krāsas perēkļi, histoloģiski atklājas serozs eksudatīvs iekaisums ar plaušu audu pārpilnību un leikocītu infiltrāciju.
Pneimokoku pneimoniju raksturo plaušu audu iznīcināšanas neesamība un gandrīz pilnīga tās struktūras atjaunošana.
Stafilokoku pneimonija
Par pneimoniju, ko izraisa eksotoksīnu veidojošā flora(stafilokoku, streptokoku), process sākas ar fokusa strutojošu iekaisumu attīstību ar plaušu audu strutojošu kušanu tā centrā. Stafilokoku pneimonija parasti attīstās ar A gripu, kas bojā elpceļu aizsargmehānismus. Stafilokoks veido eksotoksīnu un ražo fermentus – lecitināzi, fosfatāzi, hemolizīnus, koagulāzi, kas izraisa strauju plaušu audu iznīcināšanas attīstību. Histoloģiski stafilokoku pneimonijai raksturīgi ierobežoti leikocītu infiltrācijas perēkļi ar obligātu plaušu audu strutojošu kušanu šo perēkļu centrā.
Stafilokoku pneimonijas variants ir hematogēna pneimonija sepses gadījumā.
Streptokoku pneimonija, tāpat kā stafilokoks, attīstās pēc (vai uz to fona) gripas un citām elpceļu vīrusu infekcijām. Bieži sarežģī pleiras izsvīdums un abscesa veidošanās.
Frīdlendera pneimonija
Pneimonija, ko izraisa Friedlandera bacilis (Klebsiela pneumonia), bieži attīstās imūndeficīta stāvokļa fona pacientiem ar cukura diabētu, alkoholismu, gados vecākiem cilvēkiem un pacientiem, kuri lieto imūnsupresantus. Pēc morfoloģiskajiem simptomiem Frīdlandera pneimonija atgādina lobaro pneimoniju, raksturīga hemorāģiskās nekrozes attīstība ar plaušu audu sabrukumu uz saplūstošas bakteriālas tūskas zonu fona. Sabrukšanas cēloņi ir vairākas mazo asinsvadu trombozes iekaisuma zonā.
Mikoplazmas pneimonija.
Mikoplazma, ornitoze, daži vīrusi Pneimonija sākas ar plaušu intersticiālo audu iekaisuma bojājumiem.
Mikoplazmas pneimonija ir ļoti virulenta, un ir iespējami epidēmiski infekcijas uzliesmojumi. Slimības sākumā klīniskā aina ir raksturīga akūtai elpceļu vīrusu infekcijai, plaušās attīstās interstitiuma iekaisuma tūska. Attīstoties pneimonijai, notiek plaušu parenhīmas šūnu infiltrācija, pneimonijas fokuss ir līdzīgs pneimokoku pneimonijai. Pneimonijas atrisināšana ilgst līdz 2-3 nedēļām.
Hemophilus pneimonija
Haemophilus influenzae izraisīta pneimonija pieaugušajiem reti ir patstāvīga slimība, tā bieži attīstās kā sekundāra pneimonija pacientiem ar hronisku bronhītu. Morfoloģiskā aina ir līdzīga fokālajai pneimokoku pneimonijai.
Legionellas pneimonija
Pneimoniju izraisa gramnegatīvs endotoksīnu ražojošais Legionella pneumophila bacilis. Legionellas ātri vairojas siltā un mitrā vidē; iespējamie infekcijas avoti ir gaisa kondicionieri un apkures caurules. Saskaņā ar klīnisko un morfoloģisko ainu Legionella pneimonija atgādina smagu mikoplazmas pneimoniju.
Pneimonija vīrusu slimību dēļ.
Gripas pneimonija Vīrusa citopatogēnās iedarbības dēļ elpceļu epitēlijs sākas ar hemorāģisko traheobronhītu ar strauju slimības progresēšanu, pievienojot baktēriju floru, bieži vien stafilokoku. Elpceļu vīrusu infekcija (A, B gripas vīrusi, adenovīrusu infekcija, sincitiāla elpceļu vīrusu infekcija, paragripas infekcija) tiek uzskatīta par pneimonijas riska faktoru, vīruss ir sava veida bakteriālas infekcijas “vadītājs”. Elpošanas vīrusu loma pneimonijas rašanās gadījumā ir nomākt vietējo imunitāti elpceļos, jo īpaši epitēlija bojājumus, bronhu sekrēcijas traucējumus, neitrofilu un limfocītu aktivitātes nomākšanu ar imūnglobulīnu sintēzes traucējumiem. Šo iemeslu dēļ tiek aktivizēta baktēriju flora, kas nosaka pneimonijas attīstību. Pneimonija ar A un B gripu tiek uzskatīta par gripas infekcijas komplikāciju, tā biežāk attīstās cilvēkiem ar blakusslimībām un grūtniecēm. Vīrusu bojājumus raksturo plaušu audu divpusējas intersticiālas tūskas attīstība bez konsolidācijas pazīmēm; to bieži uzskata par akūtu respiratorā distresa sindromu (ARDS). Viroloģiskais pētījums atklāj augstu gripas vīrusa titru, krēpu bakterioloģiskais pētījums bieži neatklāj patogēnu baktēriju floru. Patomorfoloģisko ainu raksturo hemorāģisks traheobronhīts, hemorāģiska pneimonija, hialīna membrānu veidošanās uz alveolu virsmas un ievērojams leikocītu skaits alveolās. Pēc īslaicīgas (1-4 dienas) stāvokļa uzlabošanās attīstās bakteriāla pneimonija, plaušās tiek konstatēti infiltrācijas perēkļi, krēpās tiek konstatēti pneimokoki, stafilokoki, Haemophilus influenzae. Galvenā atšķirība starp gripas pneimoniju un sekundāro bakteriālo pneimoniju ir antibiotiku terapijas neefektivitāte pirmajā gadījumā un antibiotiku lietošanas ietekme otrajā gadījumā.
Pneumocystis pneimonija
Mikroorganismu grupa, kas apvienota ar nosaukumu Pneumocystis carinii, pieder pie raugam līdzīgām sēnēm. Seroloģisko pētījumu rezultāti liecina, ka lielākajai daļai cilvēku pirmajos dzīves gados ir bijusi asimptomātiska Pneumocystis infekcija, un vairāk nekā 90% pieaugušo ir antivielas pret Pneumocystis. Galvenais infekcijas izplatīšanās veids ir pārnešana no cilvēka uz cilvēku. Cilvēki ar normālu imūnsistēmu nav pastāvīgi Pneumocystis pārnēsātāji; Pneumocystis pneimonija ir imūndeficīta stāvokļa pacientu slimība, kurai raksturīga traucēta šūnu un humorālā imunitāte. Infekcija reti izplatās ārpus plaušām, kas izskaidrojams ar patogēna zemo virulenci. Pneumocystis pneimonijai ir trīs patomorfoloģiskie attīstības posmi. Pirmo posmu raksturo patogēna iekļūšana plaušās un tā piesaiste alveolu sieniņu fibronektīnam. Otrajā posmā notiek alveolu epitēlija deskvamācija un palielinās cistu skaits alveolārajos makrofāgos. Šajā posmā parādās pneimonijas klīniskie simptomi. Trešā (pēdējā) stadija ir alveolīts ar intensīvu alveolocītu deskvamāciju, mono- vai plazmacītisku interstitiuma infiltrāciju, lielu skaitu pneimocistu alveolārajos makrofāgos un alveolu lūmenā. Slimībai progresējot, trofozoīti un detrīts, kas uzkrājas alveolos, noved pie to pilnīgas iznīcināšanas, tiek traucēta virsmaktīvās vielas sintēze, kā rezultātā samazinās alveolu virsmas spraigums, samazinās plaušu elastība un ventilācija. - perfūzijas traucējumi. Klīniskie stāvokļi, kas saistīti ar Pneumocystis pneimoniju: HIV infekcija, imūnsupresīva terapija, vecums utt.
Citomegalovīrusa pneimonija
Citomegalovīruss (CMV) ir herpes vīruss. CMV ir tipisks oportūnistisku infekciju pārstāvis, kas parādās tikai primārā vai sekundārā imūndeficīta gadījumā. 72-94% Krievijas Federācijas pieaugušo iedzīvotāju asinīs tiek konstatētas specifiskas antivielas, kas nozīmē paša vīrusa klātbūtni organismā. Imunokompetentiem indivīdiem primārā CMV infekcija ir asimptomātiska vai ar vieglu mononukleozei līdzīgu sindromu. Tāpat kā visi herpes vīrusi, arī pēc primārās inficēšanās CMV cilvēka organismā paliek latentā stāvoklī, un imunoloģisku traucējumu gadījumā latentā vīrusa aktivācijas vai atkārtotas inficēšanās rezultātā var attīstīties smaga slimība. Riska grupā ietilpst HIV inficēti pacienti, pacienti pēc orgānu transplantācijas, vēža pacienti, grūtnieces, personas, kas saņem imūnsupresīvu terapiju uc CMV reaktivācijas nosacījums ir šūnu imunitātes, galvenokārt CD+4 palīglimfocītu, pārkāpums.
Nozokomiālās pneimonijas etioloģija, patoģenēze, patomorfoloģija
NK etioloģija
Lielākajai daļai NP ir polimikrobiāla etioloģija, un to izraisa gram (-) baktērijas (Klebsiella pneumoniae, Pseudomonas aeruginosa, Acinetobacter spp. un gram (+) cocci (Staphylococcus aureus). Anaerobi, vīrusi un sēnītes ir reti sastopami NP patogēni; pacienti ar NP bez imūndeficīta stāvokļiem tādiem patogēniem kā C. albicans, Streptococcus viridans, Enterococcus spp un koagulāzes negatīviem stafilokokiem nav etioloģiskas nozīmes.
NP riska faktori:
vecāka gadagājuma vecums;
bezsamaņas stāvoklis;
tiekšanās;
avārijas intubācija;
ilgstoša (vairāk nekā 48 stundas) mehāniskā ventilācija;
cauruļu barošana;
horizontāls stāvoklis;
operāciju veikšana, īpaši krūškurvja un vēdera dobuma orgānos, un anestēzija;
akūts respiratorā distresa sindroms;
bronhoskopija personām ar mehānisko ventilāciju
vairāku medikamentu lietošana - sedatīvi līdzekļi, antacīdi, H2 blokatori
NK patoģenēze
Priekšnoteikums NP attīstībai ir apakšējo elpceļu aizsargmehānismu pārvarēšana. Primārais baktēriju iekļūšanas ceļš apakšējos elpceļos ir potenciālos NP patogēnus saturošu orofaringeālu sekrēciju, kā arī mikroorganismus saturošu sekrēciju aspirācija no endotraheālās caurules.
Daudziem veseliem cilvēkiem raksturīga Streptococcus pneumoniae, Haemophilus influenzae, anaerobu kolonizācija orofarneksā. Gluži pretēji, kolonizācija pēc gramu (-) floras ir galvenokārt. Pseudomonas aeruginosa, Acinetobacter parasti ir reta, bet palielinās līdz ar slimnīcas uzturēšanās ilgumu un slimības smagumu. . Aspirācijas biežums palielinās, ja apziņas traucējumi, rīšanas traucējumi, samazināts rīstīšanās reflekss, lēna kuņģa iztukšošanās un kuņģa-zarnu trakta motorikas traucējumi. Retāki patoģenētiskie mehānismi NP attīstībai ir: mikrobu aerosola ieelpošana, patogēna tieša iekļūšana elpošanas traktā, hematogēna mikrobu izplatīšanās no inficētiem vēnu katetriem, nesterila barības vada/vēdera satura pārvietošana.
Normālos apstākļos kuņģis ir sterils, var attīstīties kuņģa kolonizācija ar ahlorhidriju, nepietiekamu uzturu un badošanos, enterālo uzturu un kuņģa sulas skābumu mazinošu medikamentu lietošanu. Mehāniskās ventilācijas laikā endotraheālās caurules klātbūtne elpošanas traktā izjauc aizsargmehānismus: bloķē mukocilāru transportu, izjauc epitēlija integritāti un veicina nozokomiālās mikrofloras kolonizāciju orofarneksā ar sekojošu iekļūšanu plaušās. Uz endotraheālās caurules virsmas var veidoties bioplēve, kam seko emboliju veidošanās elpceļu distālajās daļās. Baktēriju piesārņojuma avots ir paša pacienta āda un personāla rokas. Biofilma uzlabo baktēriju uzkrāšanos un palielina rezistenci pret antimikrobiālo terapiju. Aspirāciju veicina pacienta horizontālais stāvoklis uz muguras un enterālā barošana.
Pneimonijas klīnika
Kopienā iegūta pneimonijas klīnika
Pacienta sūdzības
Aizdomām par pneimoniju ir jābūt, ja pacientam ir drudzis kopā ar sūdzībām par klepu, elpas trūkumu, krēpu izdalīšanos un/vai sāpēm krūtīs. Pneimonijas klīniskā aina ir atkarīga no izraisītāja, tomēr, pamatojoties uz pneimonijas simptomiem, nav iespējams droši runāt par iespējamo etioloģiju. Arī pacienta vecums un vienlaicīgu slimību klātbūtne ietekmē slimības klīniskās izpausmes. Var nebūt tādu raksturīgu pneimonijas simptomu kā akūts slimības sākums ar drudzi, sāpēm krūtīs un klepu, īpaši novājinātiem pacientiem un gados vecākiem cilvēkiem. Vairākiem gados vecākiem pacientiem klīniskie simptomi ir vājums, apziņas traucējumi un dispepsijas simptomi. Bieži vien sabiedrībā iegūta pneimonija “debitē” ar blakusslimību paasinājuma simptomiem, piemēram, sirds mazspēju.
Izskatāmajā klīniskajā gadījumā
un sūdzības Pacients ar drudzi, klepus ar krēpām, elpas trūkumu ir raksturīgi akūtām iekaisīgām (ņemot vērā attīstības smaguma pakāpi, visticamāk infekcijas) apakšējo elpceļu slimību. Smaga intoksikācija, sāpes krūtīs, kas saistītas ar elpošanu, ir raksturīgas plaušu audu bojājumiem un ļauj aizdomām par pneimoniju. Anamnēzes dati (ilgstoša smēķēšana, periodisks klepus ar krēpām, elpas trūkuma parādīšanās) liecina, ka pacientam ir hroniska obstruktīva plaušu slimība (HOPS), kas līdzās pacienta vecumam – 64 gadi var būt riska faktors. pneimonijas attīstība. Šajā gadījumā provocējošais faktors ir hipotermija.
Slimības vēsture
Pneimonijas klīniskā aina sastāv no divām simptomu grupām: plaušu (elpošanas) un ekstrapulmonālās (vispārējās).
Tipiska pneimokoku pneimonija kam raksturīgs akūts febrils stāvoklis (ķermeņa temperatūra virs 38%), klepus ar krēpām, sāpes krūtīs, elpas trūkums.
Krupu iekaisums kuru biežums pēdējos gados atkal ir pieaudzis, un to raksturo vissmagākā gaita.Parasti slimības sākums ir saistīts ar hipotermiju. Pneimokoku pneimoniju tipiskos gadījumos raksturo pakāpeniska gaita. Klīniskie simptomi un fiziskās pazīmes ir dinamiskas un atkarīgas no pneimonijas perioda.
Sākotnējais periods(1-2 dienas) ir akūts raksturs: pēkšņas sāpes krūtīs, kas saistītas ar elpošanu, smagi drebuļi, kam seko temperatūras paaugstināšanās līdz febrila līmenim, sauss klepus (klepus), vispārējs nespēks, nespēks. Nākamo 24 stundu laikā klepus pastiprinās, un izdalās viskozas, rūsas krāsas krēpas. Objektīvie dati: izmeklējot pacienta seja ir nomākta, elpojot bieži ir deguna spārnu pietūkums, herpes uz lūpām, deguna spārni; Skartajā pusē ir aizkavēta krūškurvja elpošana, šķiet, ka pacients to saudzē sāpju dēļ, turot to ar roku.
Palpējot pār skarto zonu, tiek noteikts balss trīces pieaugums. Plaušu sitieni atklāj blāvu bungādiņu, ko izraisa iekaisīga tūska, un alveolās joprojām paliek gaiss. Auskultācija atklāj novājinātu vezikulāro elpošanu, ko izraisa ar iekaisuma eksudātu piesūcināto alveolu elastības samazināšanās, un krepītu (induktīvu induksu), kas rodas ieelpošanas augstumā, kad alveolas, kas salipušas kopā izelpas laikā, atdalās, piepildoties ar gaisu, radot raksturīgu skaņu. Pneimoniju var atpazīt pēc auskulācijas pat pirms plaušu infiltrāta parādīšanās rentgenogrammā. Šis laika posms ir aptuveni 24 stundas.
Augsts periods(1-3 dienas) raksturo pastāvīgs drudzis līdz 39 - 40 grādiem C ar ikdienas svārstībām viena grāda robežās. Temperatūras pazemināšanās notiek adekvātas ārstēšanas ietekmē, parasti 1-3 dienu laikā, ko papildina intoksikācijas simptomu samazināšanās: galvassāpes, nogurums, vājums. Fiziskās apskates laikā kulminācijas periodā skartajā zonā tiek konstatēta blāva skaņa, jo plaušas ir bezgaisa un bronhiālā elpošana .
Izšķiršanas periods ilgst līdz 3-4 nedēļām, kuru laikā normalizējas temperatūra, izzūd intoksikācijas simptomi, samazinās klepus un krēpu izdalīšanās, kas kļūst gļotāda, izzūd sāpes krūtīs. Fiziskās apskates laikāŠajā periodā skartajā zonā atkal tiek konstatēta blāva bungas skaņa, pavājināta vezikulārā elpošana un skanīgs krepīts (redux).
Bronhopneimonija (fokālais) biežāk notiek ārpus slimnīcas apstākļos. Atbilstoši rašanās apstākļiem iespējami divi “scenāriji”: pneimonijas rašanās pēc akūtas elpceļu vīrusu infekcijas vai kā bronhīta komplikācija. Fokālās pneimonijas klīniskajām izpausmēm raksturīgs arī akūts sākums, bet mazāk izteikts drudzis, intoksikācija un slimības cikliskuma trūkums. Pneimonijas smagums, kā arī fiziskās īpašības ir atkarīgas no procesa apjoma. Pārbaudot, var konstatēt krūškurvja elpošanas kavēšanos skartajā pusē. Palpējot, tiek novērota pastiprināta balss trīce un bronhofonija. Perkusijas laikā pār infiltrācijas perēkļiem tiek noteiktas saīsināta perkusijas toņa zonas. Auskultācija atklāj grūtu elpošanu, sausus un mitrus rales. Šo simptomu smagumu nosaka bojājumu atrašanās vieta.
Fiziskās apskates laikā pacientam A, 64 gadi
tiek atklāts plaušu audu sablīvēšanās sindroms: puses krūškurvja atpalicība elpošanas laikā, pastiprināta balss trīce, perkusijas skaņas saīsināšana. Krepītu izraisa fibrīna eksudāta uzkrāšanās alveolos, un var pieņemt, ka plaušu audu sablīvēšanās ir iekaisuma infiltrācijas sekas. Tādējādi, ja ir raksturīgas sūdzības par klepu, elpas trūkumu un sāpēm krūtīs un pacienta objektīvas izmeklēšanas rezultātiem, ir diezgan iespējama provizoriska pneimonijas diagnoze, kas lokalizēta apakšējā daivā labajā pusē. Ir objektīvas bronhu difūza bojājuma pazīmes - sausa izkliedēta sēkšana sēkšana, plaušu emfizēmas pazīmes. Ilga tabakas smēķēšanas, hroniska klepus un elpas trūkuma vēsture pirms pašreizējās slimības attīstības ļauj aizdomām par pacienta blakusslimību - hronisku obstruktīvu plaušu slimību (HOPS). Šajā gadījumā HOPS kā riska faktors palielina pneimonijas diagnozes iespējamību.
Mikoplazmas etioloģijas KLP klīniskās pazīmes. Drudzis nesasniedz augstu smaguma pakāpi. Raksturīgi ir elpceļu bojājumu simptomi: klepus (visbiežākais simptoms), elpas trūkums (reti sastopams simptoms), faringīta simptomi. Plaušu perkusijas laikā izmaiņas bieži netiek konstatētas; Auskultācija atklāj neizteiktu sēkšanu – sausu vai mitru, smalki burbuļojošu. Mikoplazmas infekcijas ekstrapulmonāras izpausmes: bungādiņas iekaisums (auss sāpes), asimptomātisks sinusīts, hemolīze ar paaugstinātu aukstā aglutinīna titru, katarāls pankreatīts, katarāls meningīts, meningoencefalīts, neiropātija, smadzeņu ataksija; makulopapulāri ādas bojājumi, multiformā eritēma, miokardīts (retāk), glomerulonefrīts (retāk), mialģija, artralģija (bez patiesa artrīta attēla). Plaušu rentgena dati: palielināts plaušu modelis,
fokālie infiltrāti, diskoīda atelektāze, palielināti plaušu sakņu limfmezgli, pleirīts. Laboratorijas dati: hemolītiskā anēmija ar retikulocitozi, trombocitoze kā reakcija uz anēmiju, konstatēta cerebrospinālajā šķidrumā l impocitoze ar palielinātu olbaltumvielu daudzumu. Etioloģiskā diagnoze: anti-mikoplazmas antivielu IgM, IgG noteikšana asins serumā, kuras tiek noteiktas ar imunoloģisko metodi) no 7.-9. slimības dienas titrā virs 1:32 vai ar 4-kārtīgu dinamikas pieaugumu. . un antigēnu noteikšana - Mikoplazmas DNS vienas nedēļas laikā no slimības sākuma.
Hlamīdiju etioloģijas CAP klīniskās pazīmes
Plaušu simptomi: sauss klepus vai ar vieglu krēpu izdalīšanos, sāpes krūtīs, mērena sausa sēkšana vai mitras raļļi.
Ekstrapulmonālie simptomi: dažāda smaguma intoksikācija, aizsmakums, bieži iekaisis kakls, meningoencefalīts, Guillain-Barre sindroms, reaktīvs artrīts, miokardīts. Plaušu rentgena dati: palielināts plaušu modelis vai lokāla subsegmentāla infiltrācija. Laboratorijas dati: normāla asins analīze. Etioloģiskā diagnoze: antivielu noteikšana, izmantojot RSK, antigēnu noteikšanas metodes ELISA, PCR .
Legionellu etioloģijas KLP klīniskās pazīmes
Plaušu simptomi: klepus (41-92%), elpas trūkums (25-62%), sāpes krūtīs (13-35%). Ārpusplaušu simptomi: drudzis (42 - 97%, temperatūra virs 38,8 grādiem C), galvassāpes, mialģija un artralģija, caureja, slikta dūša/vemšana, neiroloģiski simptomi, apziņas traucējumi, nieru un aknu darbības traucējumi. Rentgena dati: infiltratīvas ēnas ar tendenci saplūst, palielināts plaušu modelis, eksudatīvs pleirīts. Laboratorijas dati: leikocitoze ar nobīdi pa kreisi, palielināts ESR, relatīvā limfopēnija, trombocitopēnija; hematūrija, proteīnūrija, hiponatriēmija, hipofosfatēmija. Etioloģiskā diagnoze: kultivēšana uz selektīvas barotnes, antigēna noteikšana urīnā vai krēpās, antivielu noteikšana asinīs (sākotnējais pieaugums 2 reizes vai 4 reizes līdz 2. slimības nedēļai, vienlaicīga IgM un IgG palielināšanās), polimerāzes ķēdes reakcija, krēpu krāsošana saskaņā ar gramu (neitrofilija un gramnegatīvās nūjiņas). Ārstēšanas iezīme ir beta-laktāmu un aminoglikozīdu iedarbības trūkums.
KLP klīniskās pazīmes, ko izraisa Frīdlandera bacilis(Klebsiella pneumoniae)
Plašs plaušu audu bojājums (lobārs, starpsumma), izdalīto krēpu gļotām līdzīgs raksturs, iespēja attīstīties infarktam līdzīgai plaušu nekrozei, tendence uz strutojošām komplikācijām (abscess, pleiras empiēma).
Pneumocystis pneimonijas klīniskās pazīmes HIV inficētiem pacientiem Oportūnistisku patogēnu izraisītu slimību klātbūtne, plaušu un ārpusplaušu tuberkuloze, Candida albicans izraisīts stomatīts, parastās starpenes čūlas (herpes simplex vīrusa aktivizēšana).
Pneimonijas instrumentālā un laboratoriskā diagnostika
Pneimonijas staru diagnostika
Radiācijas izmeklēšana pacientiem ar aizdomām vai zināmu pneimoniju ir vērsta uz plaušu audu iekaisuma procesa pazīmju un iespējamo komplikāciju noteikšanu un to dinamikas novērtēšanu ārstēšanas ietekmē. Pētījums sākas ar krūškurvja orgānu aptaujas rentgenu priekšējā un sānu projekcijās. Fluoroskopijas izmantošana aprobežojas ar klīniskām situācijām, kurās nepieciešams nošķirt izmaiņas plaušās un šķidruma uzkrāšanos pleiras dobumā. Atsevišķās klīniskās situācijās - diferenciāldiagnoze, ilgstoša pneimonijas gaita utt., Datortomogrāfijas iecelšana ir pamatota. Ultraskaņas izmeklēšana tiek izmantota, lai novērtētu pleiras un pleiras dobuma stāvokli šķidruma uzkrāšanās gadījumā.
Galvenā pneimonijas radioloģiskā pazīme ir lokāla plaušu audu gaisīguma samazināšanās (“ēnojums”, “tumšošana”, “blīvēšanās”, “infiltrācija”). izraisa plaušu elpceļu daļu piepildīšanās ar iekaisuma eksudātu, kā rezultātā plaušu audi kļūst bezgaisa (alveolārais infiltrācijas veids). Retikulāra (tīkla) vai peribronhovaskulāra (stingra) plaušu audu intersticiāla infiltrācija rodas, jo interalveolārās telpas ir piepildītas ar iekaisuma eksudātu. Interalveolāro starpsienu sabiezēšanu pavada alveolu apjoma samazināšanās, saglabājot to gaisīgumu, kas rada radioloģisko caurspīdīguma jeb “matēta stikla” fenomenu. Infiltratīvo izmaiņu lokalizācija atspoguļo galveno pneimonijas attīstības patoģenētisko mehānismu - patogēno patogēnu aspirāciju vai ieelpošanu caur elpceļiem. Infiltrācija visbiežāk izplatās vienā vai divos segmentos, lokalizējas galvenokārt plaušu apakšējās daivas (S IX, S X) un augšējo daivu paduses apakšsegmentos (SII, S ax-II, III), bieži vien ir vienpusējs un labējais. -pusējā lokalizācija. Pleiropneimonijas gadījumā plaušu audu sablīvēšanās zonai ir viendabīga struktūra, ar plašu pamatni atrodas blakus viscerālajai pleirai, tās intensitāte pakāpeniski samazinās saknes virzienā, starplobārā pleira ir ieliekta pret sablīvēto zonu, daiva nav mainīta vai samazināta, infiltrācijas zonā redzamas lielo bronhu gaisa spraugas (gaisa bronhogrāfijas simptoms). Plaušu modeļa izmaiņas bez plaušu audu infiltrācijas rodas citu slimību gadījumā, biežāk plaušu cirkulācijas traucējumu rezultātā, reaģējot uz intoksikāciju un ekstravaskulārā šķidruma līdzsvara traucējumiem plaušās, bet pašas par sevi nav pneimonijas pazīmes, t.sk. intersticiāla pneimonija. Bronhopneimoniju raksturo neviendabīgas struktūras infiltrācijas zonas klātbūtne plaušās, kas sastāv no daudziem polimorfiem centrilobulāriem perēkļiem ar neskaidrām kontūrām, kas bieži saplūst viens ar otru. Šāda veida infiltrācija ir balstīta uz iekaisuma procesa pāreju no maziem intralobulāriem bronhiem uz plaušu audiem. Pneimonisko bojājumu izmērs var būt no miliāriem (1-3 mm) līdz lieliem (8-10 mm). Dažos perēkļos var izsekot bronhu lūmeniem, citos struktūra ir viendabīgāka, jo mazos bronhus aizsprosto iekaisuma eksudāts. Fokālās infiltrācijas zona sniedzas līdz vienam vai vairākiem segmentiem, daivai vai vairākiem blakus esošo daivu segmentiem. Ja pneimonijas klīniskā gaita ir labvēlīga, divas nedēļas pēc ārstēšanas sākuma vēlams veikt kontroles rentgena izmeklēšanu, kuras pamatā rentgena izmeklēšanai šajos gadījumos ir identificēt centrālo vēzi un aizsegā sastopamu tuberkulozi. pneimonijas gadījumā. Iekaisuma apgrieztā attīstība ir saistīta ar eksudāta sašķidrināšanu un izvadīšanu caur elpošanas ceļiem un limfātiskajiem asinsvadiem. Šajā gadījumā tiek novērota infiltrācijas ēnas intensitātes samazināšanās līdz tās pilnīgai izzušanai. Pneimonijas atrisināšanas process var nebūt pilnībā pabeigts, savukārt alveolās un plaušu interstitijā veidojas karnifikācijas zonas, jo tiek organizēts iekaisuma eksudāts, vai pneimosklerozes zonas pārmērīgas saistaudu elementu proliferācijas dēļ.
64 gadus veca pacienta A krūšu dobuma rentgena dati
Pneimonijas diagnozi apstiprina krūškurvja rentgenogrāfija.

Iekaisuma infiltrācijas perēkļi ir lokalizēti labās plaušas apakšējā daivā un tiek apvienoti ar plaušu saknes paplašināšanos un plaušu modeļa palielināšanos.
Piemērs. Plaušu rentgenogrāfija pacientam ar masīvu (totālu) pneimoniju.

Kreisajā plaušu laukā, kas pēc būtības ir neviendabīgs, ir manāma pilnīga tumšāka. Skartās krūškurvja puses izmēri nemainās, videnes pārvietošanās nav.
Negatīvi krūškurvja rentgena rezultāti nevar pilnībā izslēgt KLP diagnozi, ja tās klīniskā iespējamība ir augsta. Dažos gadījumos KLP diagnozes laikā pneimonijas infiltrācijas fokuss netiek vizualizēts.
Laboratoriskā pneimonijas diagnostika
Klīniskā asins analīze
Par lielu bakteriālas infekcijas iespējamību liecina leikocitoze (>10x109/l) un/vai joslu nobīde (>10%); leikopēnija (<3х10.9) или лейкоцитоз >25x10,9 ir nelabvēlīgas prognozes rādītāji.
Bioķīmiskās asins analīzes
Palielināts C-reaktīvā proteīna līmenis> 50 mg/l atspoguļo iekaisuma procesa sistēmisko raksturu, kas novērots pacientiem ar smagu pneimokoku vai legionellas izraisītu pneimoniju. Līmenis prokalcitonīns korelē ar pneimonijas smagumu, un tam var būt prognostiska vērtība sliktam iznākumam. Aknu, nieru funkcionālie pētījumi var liecināt par šo orgānu iesaistīšanos, kam ir prognostiska nozīme un kas ietekmē arī antibakteriālās terapijas izvēli un režīmu.
Arteriālo asiņu gāzu noteikšana
Pacientiem ar plašu pneimoniju infiltrāciju, komplikāciju klātbūtnē pneimonijas attīstība uz HOPS fona un ar skābekļa piesātinājumu mazāku par 90%, indicēta arteriālo asins gāzu noteikšana. Hipoksēmija ar pO2 zem 69 mm Hg. ir indikācija skābekļa terapijai.
Pneimonijas etioloģiskā diagnoze
Mikrobioloģiskā diagnostika. Pneimonijas izraisītāja identificēšana ir optimāls nosacījums adekvātas antibiotiku terapijas izrakstīšanai. Tomēr, ņemot vērā mikrobioloģisko pētījumu sarežģītību un ilgumu, no vienas puses, un nepieciešamību nekavējoties uzsākt ārstēšanu, no otras puses, antibakteriālā terapija tiek nozīmēta empīriski, pamatojoties uz klīniskajām un patoģenētiskajām īpašībām katrā konkrētajā gadījumā. Pieejama un ātra izpētes metode ir bakterioskopija ar krēpu uztriepes Grama krāsošanu. Liela skaita grampozitīvu vai gramnegatīvu mikroorganismu identificēšana var kalpot kā ceļvedis antibakteriālās terapijas izvēlē. Mikrobioloģisko pētījumu veikšanas pamatojums ir:
ICU uzņemšana;
iepriekšēja neveiksmīga šīs slimības antibiotiku terapija;
komplikāciju klātbūtne: plaušu audu iznīcināšana vai abscesi, pleiras izsvīdums;
blakusslimību fona klātbūtne: HOPS, CHF, hroniska alkohola intoksikācija utt.
Pacientiem ar smagu pneimoniju nepieciešama seroloģiskā pārbaude. diagnostika“netipisku” patogēnu izraisītas infekcijas, kā arī L. pneumophila un Streptococcus pneumoniae antigēnu noteikšana urīnā. Intubētiem pacientiem ir nepieciešama endotraheālā aspirāta savākšana. Pacientiem ar smagu pneimoniju pirms antibiotiku terapijas uzsākšanas jāsaņem venozo asiņu paraugi kultūrai (2 paraugi no divām dažādām vēnām).
Molekulāri bioloģiskās metodes Pneimonijas patogēni - Mikoplazma pneumoniae, Hlamidofīla. pneumoniae, Legionellas pneimofila grūti diagnosticēt, izmantojot tradicionālās metodes. To identificēšanai tiek izmantotas molekulāri bioloģiskās metodes, no visām šobrīd esošajām ātrās diagnostikas metodēm vispieņemamākā ir polimerāzes ķēdes reakcija (PCR). Indikācijas tās ieviešanai pneimonijas gadījumā var būt smaga slimība, sākotnējās antibiotiku terapijas neefektivitāte vai epidemioloģiskā situācija.
Pleiras šķidruma pārbaude
Pleiras izsvīduma klātbūtnē indicēta pleiras šķidruma izpēte ar leikocītu skaitīšanu un leikocītu formulu, pH, LDH aktivitātes, proteīna satura noteikšanu, uztriepes bakterioskopiju un kultūras izmeklēšanu.
Invazīvās diagnostikas metodes.
Diagnostiskā fibrobronhoskopija ar bronhu satura mikrobioloģisko, citoloģisku izmeklēšanu, biopsiju, bronhoalveolāru skalošanu indicēta, ja nepieciešama diferenciāldiagnoze ar tuberkulozi, bronhogēnu vēzi un citām slimībām.
Pacienta ar VP instrumentālās un laboratoriskās izmeklēšanas apjoms tiek izlemts individuāli.
Diagnostiskā minimālā izmeklēšana ambulatorajiem pacientiem papildus vēsturei un fiziskajai pārbaudei jāiekļauj pētījumi, lai noteiktu ārstēšanas smagumu un nepieciešamību pēc hospitalizācijas. Tie ietver krūškurvja rentgenu un pilnīgu asins analīzi. Regulāra KLP mikrobioloģiskā diagnostika ambulatorā stāvoklī būtiski neietekmē antibakteriālo zāļu izvēli.
Diagnostiskā minimālā izmeklēšana hospitalizētiem pacientiem jāiekļauj pētījumi, lai noteiktu KLP diagnozi, smagumu un lemtu par ārstēšanas vietu (terapeitiskā nodaļa vai ICU). Tie ietver:
krūškurvja orgānu rentgenogrāfija;
Vispārēja asins analīze;
Bioķīmiskā asins analīze (glikoze, kreatinīns, elektrolīti, aknu enzīmi);
Mikrobioloģiskā diagnostika: krēpu uztriepes mikroskopija, iekrāsošana ar gramu, krēpu bakterioloģiskā izmeklēšana ar patogēna izolēšanu un jutības noteikšana pret antibiotikām, asins bakterioloģiskā izmeklēšana.
Papildu metodes smagi slimiem pacientiem: pulsa oksimetrija, asins gāzu pētījumi, pleiras šķidruma citoloģiskie, bioķīmiskie un mikrobioloģiskie pētījumi pleirīta klātbūtnē.
64 gadus veca pacienta A laboratorisko pārbaužu dati,
apstiprina akūtu iekaisumu (leikocitoze ar nobīdi pa kreisi, palielināts ESR, gļoturulentas krēpas ar augstu leikocītu un koku saturu). Grampozitīvu diplokoku noteikšana krēpās liecina par slimības pneimokoku etioloģiju. Bioķīmiskajiem parametriem nav novirzes no normālām vērtībām. Pulsa oksimetrija atklāja skābekļa piesātinājuma samazināšanos līdz 95%, kas norāda uz 1. pakāpes elpošanas mazspēju. Spirogrāfija atklāja bronhu obstrukcijas pazīmes – FEV1 samazināšanos līdz 65% no normālās vērtības.
Pneimonijas diagnostikas kritēriji
Galvenais uzdevums, ko ārsts risina, pacientam ierodoties pie viņa ar apakšējo elpceļu infekcijas simptomiem, ir apstiprināt vai izslēgt pneimoniju kā slimību, kuras iznākums ir atkarīgs no pareizas un savlaicīgas ārstēšanas. . Zelta standarts pneimonijas diagnosticēšanai būtu identificēt iespējamo patogēnu no infekcijas avota. Taču praksē šāda diagnostikas pieeja, kas ietver invazīvas manipulācijas, nav iespējama. Šajā sakarā alternatīva ir kombinēta diagnostikas pieeja, tostarp ņemot vērā klīniskos simptomus, radioloģiskās, mikrobioloģiskās un laboratoriskās pazīmes, kā arī antibakteriālās terapijas efektivitāti.
Ir aizdomas par pneimoniju, ja pacientam ir šādi sindromi:
vispārējs iekaisuma sindroms: akūts sākums ar temperatūras paaugstināšanos līdz febrila līmenim, drebuļi, stipra svīšana naktī, vājums, apetītes zudums, galvassāpes un muskuļu sāpes; akūtās fāzes asins parametri (paaugstināts PSA);
apakšējo elpceļu sindroms: klepus ar krēpām, elpas trūkums, sāpes krūtīs;
plaušu sindroms: pār skarto plaušu zonu ir lokāls balss trīces un bronhofonijas palielināšanās, perkusiju skaņas saīsināšanās, krepita fokuss (indux, redux) vai skanīgi smalku burbuļu raļļi, bronhu elpošana.
plaušu infiltrācijas sindroms, iepriekš nenoteikts., ar rentgena izmeklējumu; Nozoloģiskā diagnoze tiek apstiprināta, identificējot patogēnu.
Noteikti KLP diagnoze ir, ja pacientam ir:
Rentgenā apstiprināta plaušu audu fokusa infiltrācija un
Vismaz divas klīniskās pazīmes no sekojošām:
a) akūts drudzis slimības sākumā (temperatūra > 38,0 °C; b) klepus ar krēpām;
c) fiziskas pazīmes: krepita fokuss un/vai smalki burbuļojoši raļļi, grūta, bronhiāla elpošana, perkusiju skaņas saīsināšana;
d) leikocitoze >10,9/l un/vai joslu nobīde vairāk nekā 10%.
Neprecīzs/neskaidrs KLP diagnozi var veikt, ja nav radioloģiskā apstiprinājuma fokālās infiltrācijas plaušās vai nav pieejams. Šajā gadījumā diagnoze balstās uz epidemioloģiskās vēstures, sūdzību un atbilstošo vietējo simptomu ņemšanu vērā.
CAP diagnoze ir maz ticama jāapsver, ja, izmeklējot pacientu ar drudzi, sūdzībām par klepu, elpas trūkumu, krēpu izdalīšanos un/vai sāpēm krūtīs, nav pieejama rentgena izmeklēšana un nav lokālu simptomu.
Pneimonijas diagnoze kļūst nosoloģisks pēc slimības izraisītāja noteikšanas. Etioloģijas noskaidrošanai tiek veikta ar gramu krāsotu krēpu uztriepes bakterioskopija un krēpu kultūras izmeklējums, šāds pētījums ir obligāts stacionārā un pēc izvēles ambulatorā stāvoklī.
KLP diagnostikas kritēriji
|
Diagnoze |
Kritēriji |
||||
|
Rentgens. zīmes |
Fiziskās pazīmes |
Akūts Sākt, 38 gr. AR |
Klepus ar krēpas |
Leikocitoze:> 10 X10 9 /; p-i> 10% |
|
|
Noteikti |
+ |
Jebkuri divi kritēriji | |||
|
Neprecīzi /neskaidrs |
- |
+ |
+ |
+ |
+/- |
|
Maz ticams |
- |
- |
+ |
+ |
+/- |
Klīniskā diagnozepacients A. 64 gadi
formulēts, pamatojoties uz diagnostikas kritērijiem: klīniski akūts drudzis slimības sākumā > 38,0 grādi C; klepus ar flegmu; lokālas plaušu audu iekaisuma fizikālās pazīmes - pastiprināti balss trīce, perkusijas skaņas saīsināšanās, krepīta fokuss zemlāpstiņas rajonā pa labi), radioloģiskās (fokāla plaušu audu infiltrācija apakšējā daivā pa labi unS8,9,10); laboratorija (leikocitoze ar joslu sedāciju un paātrinātu ESR).
Slimības rašanās mājās liecina par sabiedrībā iegūto pneimoniju.
Veicot krēpu kultivēšanu, tika izolēts pneimokoks ar diagnostisko titru 10,7 grādi, kas nosaka nozoloģisko diagnozi.
Vienlaicīgas slimības - HOPS diagnozi var noteikt, pamatojoties uz raksturīgiem kritērijiem: riska faktors (tabakas smēķēšana), klīniskie simptomi - ilgstošs klepus ar krēpām, papildus elpas trūkums, objektīvas bronhu obstrukcijas un emfizēmas pazīmes. (sausas, izkliedētas rales, rūgta skaņa uz plaušu perkusijām). HOPS diagnozi apstiprina emfizēmas radioloģiskās pazīmes un obstruktīvu ventilācijas traucējumu klātbūtne (FEV1 samazināšanās līdz 65% no normālās vērtības). Paasinājumu skaits, kas pārsniedz 2 gadā, un vidējā ventilācijas traucējumu pakāpe ļauj klasificēt pacientu augsta riska grupā C.
KLP komplikācijas
Smagos pneimonijas gadījumos var attīstīties komplikācijas - plaušu un ekstrapulmonālas.
Pneimonijas komplikācijas
Plaušu:
pleirīts
akūta strutojoša plaušu audu iznīcināšana.
Ārpusplaušu:
infekciozi toksisks šoks;
akūta elpošanas mazspēja;
akūts cor pulmonale;
sekundārā bakterēmija;
akūts respiratorā distresa sindroms;
citu orgānu infekciozi toksiski bojājumi: perikardīts, miokardīts, nefrīts utt.
sepse
Akūta strutojoša plaušu iznīcināšana
Plaušu akūtu strutojošu procesu cēlonis 92% gadījumu ir pneimonija. Akūtas strutainas plaušu iznīcināšanas klīniskās un morfoloģiskās formas ir akūts abscess, fokusa strutaini-nekrotiska plaušu destrukcija un plaušu gangrēna.
Akūts abscess - strutojošs-nekrotisks plaušu bojājums ar bakteriālu un/vai autolītisko nekrozes proteolīzi, jo tas veidojas, veidojot vienu (vai vairāku) sabrukšanas dobumu (dobumus) ar robežu no dzīvotspējīgiem plaušu audiem. Abscesa pneimonija - akūts strutojošs process, kura galvenā iezīme ir nelielu strutojošu perēkļu parādīšanās iekaisuma vietās.
Plaušu fokusa strutaini-nekrotiska iznīcināšana ko raksturo vairāku strutojošu-nekrotisku baktēriju vai autolītiskas proteolīzes perēkļu veidošanās bez skaidras robežas no dzīvotspējīgiem plaušu audiem.
Plaušu gangrēna - strauji progresējoša strutojoša-pūšanas plaušu nekroze bez norobežojumiem.
Akūti strutojoši-destruktīvi plaušu procesi var būt sarežģīti ar piopneimotoraksu, pleiras empiēmu, asiņošanu, krūškurvja sienas flegmonu, kā arī ekstrapulmonālām komplikācijām: sepsi, diseminētas intravaskulāras koagulācijas sindromu u.c.
Faktori, kas predisponē strutojošu destruktīvu procesu: elpceļu vīrusu infekcija, alkoholisms, imūndeficīta stāvokļi, traumatisks smadzeņu bojājums uc Etioloģiskie faktori plaušu strutainas iznīcināšanas attīstībā var būt stafilokoki, streptokoki, Pseudomonas aeruginosa, Klebsiella, enterobaktērijas, sēnītes (aspergillus), mikoplazmas. Akūtas infekciozas plaušu destrukcijas etioloģijā ir konstatēta sporas neveidojošo anaerobu loma: bakterioīdi, fusobaktērijas un anaerobie koki, kas parasti saprofītējas mutes dobumā, īpaši cilvēkiem ar zobu kariesu, pulpītu, periodontītu, uc Jautājumi par akūtu strutojošu-destruktīvu procesu attīstību plaušās nav pilnībā izpētīti. Ar pneimokoku pneimoniju attīstās strutojošs-destruktīvs process sekundāras oportūnistisku mikroorganismu invāzijas rezultātā tūskas un plaušu audu infiltrācijas zonā.Vīrusu bojājumi apakšējo elpceļu eitēlijam rada apstākļus invāzijai plaušās. audi ar oportūnistisku floru, kas atrodas elpošanas traktā. Aspirācijas, bronhu caurules aizsprostojuma gadījumā ar audzēju vai svešķermeni var pievienoties anaerobā flora, kas izraisa pūšanas procesus plaušās. Mikrobu aģentu iekļūšanas ceļi plaušās ir dažādi: endobronhiāli, hematogēni, traumatiski.
Strutaino-destruktīvo procesu patoģenēze plaušās.
Reaģējot uz mikroorganismu invāziju un audu bojājumiem ap iekaisuma un iznīcināšanas perēkļiem, rodas mikrocirkulācijas diseminētās blokādes parādība (izkliedētas intravaskulāras koagulācijas lokālais vai orgānu sindroms - DIC - sindroms). Mikrocirkulācijas bloķēšana ap bojājumu ir dabiska un agri notiekoša aizsargreakcija, kas nodrošina atdalīšanos no veseliem audiem un novērš baktēriju floras, toksīnu, pro-iekaisuma mediatoru un audu iznīcināšanas produktu izplatīšanos visā organismā. Masīva asinsvadu mikrotromboze ar fibrīna recekļiem un asins šūnu agregātiem, veidojoties dūņām, ietekmē plaušu audu zonas, kas atrodas tālu no bojājuma vietas, un to pavada traucēta mikrocirkulācija, kas izraisa neefektīvu elpošanu, hipoksiju un atjaunošanās procesu traucējumus. plaušu audi. Mikrocirkulācijas bloķēšana ap bojājumu un plaušu audu iznīcināšana novērš zāļu, jo īpaši antibiotiku, iekļūšanu bojājumā, kas veicina antibiotiku rezistences veidošanos. Plaši izplatīta mikrotrombotiska reakcija ar nelabvēlīgu gaitu bieži ietver ne tikai zonas, kas atrodas blakus iekaisuma perēkļiem, bet izplatās uz attāliem audiem un orgāniem. Šajā gadījumā attīstās mikrocirkulācijas traucējumi, kas izraisa daudzu orgānu darbības traucējumus: centrālās nervu sistēmas, nieru, aknu un kuņģa-zarnu trakta. Zarnu gļotādas barjerfunkcijas samazināšanās dēļ tā kļūst caurlaidīga zarnu mikroflorai, kas izraisa sekundāras endogēnas sepses attīstību, veidojot infekcijas perēkļus dažādos audos un orgānos.

DIFERENCIĀLDIAGNOSTIKA PNEUMONIJAI
Pneimonija- akūta plaušu lokāla infekciozi-iekaisuma slimība, kas patoloģiskajā procesā ietver elpošanas sekcijas (alveolas, bronhiolus), kas rodas ar iekaisuma šūnu infiltrāciju un intraalveolāru eksudāciju.
Klasifikācija
Pēc etioloģijas:
ü bakteriāls (norādot konkrētu patogēnu),
ü vīrusu,
ü sēnīte
ü nenorādot patogēnu.
Epidemioloģiskā:
ü ārpus slimnīcas,
ü slimnīca,
ü tiekšanās,
uz imūndeficīta fona.
Pēc smaguma pakāpes:
ü nav smags,
ü smags.
Pēc lokalizācijas: norādot segmentu vai vairākus segmentus.
Atkarībā no plūsmas veida:
ü ilgstoša (slimības ilgums vairāk nekā 1 mēnesis).
Komplikācijas:
ü plaušu
§ parapneimonisks pleirīts,
§ pleiras empiēma,
§ plaušu abscess un gangrēna,
§ plaušu iznīcināšana,
§ bronhu obstrukcija,
§ akūta elpošanas mazspēja (distresa sindroms).
ü ārpusplaušu
§ infekciozi toksisks šoks,
§ akūts cor pulmonale,
§ DIC sindroms,
§ sepse,
§ miokardīts,
§ endokardīts,
§ perikardīts,
§ meningīts,
§ encefalīts,
§ akūta psihoze.
Diagnozes piemērs:
1. Kopienā iegūta pneimonija, kas lokalizēta labās plaušas S 8-9, gaita nav smaga. DN I.
2. Kopienā iegūta apakšējās daivas kreisās puses pneimonija, smaga, komplicēta ar eksudatīvu pleirītu. DN II.
Kopienā iegūta pneimonija (CAP)- akūta slimība, kas radusies sabiedrībā (ārpus slimnīcas vai diagnosticēta pirmajās 48 stundās pēc hospitalizācijas).
Etioloģija
CAP etioloģija ir tieši saistīta ar normālu mikrofloru, kas kolonizē augšējos elpceļus. Visbiežāk sastopamie patogēni:
ü Streptokoku pneimonijae (30-50% gadījumu),
ü Haemophilus influenzae (pirms tam 10%) .
Netipiskiem mikroorganismiem (kurus nevar identificēt ar bakterioskopiju vai kultivēšanu uz parastajām barotnēm) ir nozīmīga loma KLP etioloģijā; 8-30% slimības gadījumu:
ü Hlamidofīla pneumoniae, Mikoplazma pneimonija(kopā līdz 25%),
ü Legionella pneumophila.
Reti (3-5%) KLP patogēni ir:
ü Staphylococcus aureus,
ü Klebsiella pneumoniae
ü enterobaktērijas.
Ļoti retos gadījumos KLP var izraisīt Pseudomonas aeruginosa(pacientiem ar cistisko fibrozi, bronhektāzes klātbūtnē).
No praktiskā viedokļa ir vēlams nošķirt KLP pacientu grupas, ņemot vērā vecumu, pavadošo patoloģiju un slimības smagumu (1. tabula).
1. tabula
Pacientu grupas ar KLP un iespējamiem patogēniem
Nozokomiālā (slimnīca, nozokomiālā) pneimonija (NP) - slimība, kas attīstās 48 stundas vai ilgāk pēc hospitalizācijas, izņemot infekcijas, kas bija inkubācijas periodā brīdī, kad pacients tika ievietots slimnīcā.
Riska faktori:
ü slimnīcas uzturēšanās ilgums,
ü iepriekšēja antibakteriālā terapija,
ü hronisku pamatslimību klātbūtne,
ü ārstniecības iestādes specifika.
Izcelt agrīna hospitalizācija pneimonija, kas rodas laika posmā no 2 līdz 5 hospitalizācijas dienām, kam raksturīgi patogēni, kas pārsvarā ir jutīgi pret tradicionāli lietotām pretmikrobu zālēm ( S. Pneumonijas, Enterobacteriaceae, H. Influenzae) un tam ir labvēlīga prognoze.
Vēla uzturēšanās slimnīcā pneimonija attīstās pēc 5. hospitalizācijas dienas, un to raksturo augsts multirezistentu patogēnu risks (P. aeruginosa, Escherichia coli, Klebsiella pneumoniae un Acinetobacter spp.) un mazāk labvēlīga prognoze.
Arī izceļas ar ventilatoru saistīta pneimonija (VAP) - pneimonija cilvēkiem ar mehānisko ventilāciju.
Aspirācijas pneimonija (AP) var būt gan ārpus slimnīcas, gan slimnīcas iekšienē. AP apgrūtina pacienta pārtikas, vemšanas, asiņu, toksisko un citu vielu aspirāciju apakšējos elpceļos, ko pavada patogēnas floras iekļūšana kopā ar aspirātu. Aspirācija parasti attīstās cilvēkiem ar dažāda dziļuma apziņas traucējumiem šādu iemeslu dēļ:
ü smaga alkohola intoksikācija,
ü insults,
ü anestēzija,
ü dažādu etioloģiju koma,
ü saindēšanās ar miegazālēm,
ü konvulsīvi apstākļi.
Aspirācija var notikt ar kardiospazmu vai traheo-barības vada fistulu klātbūtni.
Anaerobi izraisa AP attīstību:
ü Bacteroides melaninogēns,
ü Fuzobaktērija kodols,
ü Peptosstreptokoksun utt.,
kā arī daži aerobi:
ü Escherichia coli
ü Stafilokoksaureus,
ü Pseidomonas aerugenosa.
Pneimonija cilvēkiem ar imūndeficītu.
Galvenie imūndeficīta cēloņi ir:
ü HIV infekcija,
ü leikēmija;
ü ilgstoša (> 3 nedēļas) citostatisko līdzekļu vai sistēmisko glikokortikoīdu lietošana audzēju, sistēmisku slimību ārstēšanai, pacientiem pēc orgānu transplantācijas.
Vispārējā asins analīzē imūndeficīts izpaužas kā ilgstoša neitropēnija (< 500 клеток в 1 мкл крови) в период диагностики или в предыдущие 60 дней.
Visticamākā pneimonijas etioloģija cilvēkiem ar novājinātu imunitāti ir:
ü S. aureus,
ü Pseudomonas aeruginosa,
ü S. pneimonija,
ü H. Gripa
ü E. coli.
Īpašs pneimonijas izraisītājs imūndeficīta fona apstākļos ir Pneumocystis carinii. Vairāk nekā 3/4 Pneumocystis pneimonijas ir saistītas ar HIV . Pārējie gadījumi rodas pacientiem ar primāru vai sekundāru imūndeficītu, tostarp jatrogēnu imūnsupresiju.
Diagnostikas standarts pneimonijas pacienta izmeklēšanai
Klīniskie kritēriji:
ü Akūts febrils drudzis, intoksikācija,
ü Klepus ir sauss vai ar krēpām,
ü Sāpes krūtīs, kas saistītas ar elpošanu,
ü Vietējais sitaminstrumentu skaņas blāvums,
ü Lokāli dzirdama bronhu elpošana, skanīgu smalku rēguļu un/vai kreptu zona, pleiras berzes troksnis.
Objektīvie kritēriji:
ü leikocitoze > 10 G/l ar joslu nobīdi > 10%, palielināts ESR;
ü infiltratīva aptumšošanās krūškurvja orgānu vienkāršā rentgenogrammā;
ü mikroorganismu identificēšana krēpās bakterioskopijas laikā ar uztriepes Grama krāsošanu, kā arī mikroorganisma pārbaude un tā jutīguma noteikšana pret antibiotikām bakterioloģiskās izmeklēšanas laikā;
ü asins piesātinājums ar skābekli< 90% по данным пульсоксиметрии (является критерием тяжелой пневмонии и показанием для проведения кислородотерапии).
Uzskaitīti kritēriji pietiekams pneimonijas diagnostikai un ārstēšanai ambulatori, kā arī nekomplicētas slimības gaitas laikā stacionārā.
Papildu pētījumu metodes:
ü datortomogrāfija(ar augšējo daivu, videnes limfmezglu bojājumiem, daivas tilpuma samazināšanos, aizdomām par abscesa veidošanos, ar antibakteriālās terapijas neefektivitāti, ar acīmredzamu pneimonijas klīnisko ainu, izmaiņu rentgenogrammā nav vai ir netieša rakstura, atkārtota pneimonija ar tādu pašu lokalizāciju, ilgstoša pneimonija).
ü Seroloģiskais pētījums ar netipisku pneimonijas gaitu riska grupā cilvēkiem, kuri pārmērīgi lieto alkoholu, narkotikas, gados vecākiem un seniliem cilvēkiem, ar imūndeficītu.
ü Mikrobioloģiskā izmeklēšana pleiras šķidrums.
ü Bioķīmiskā asins analīze smagos pneimonijas gadījumos ar nieru un aknu mazspējas izpausmēm, pacientiem ar hroniskām slimībām, cukura diabēta dekompensāciju.
ü Cito- un histoloģiskā izmeklēšana plaušu vēža risks smēķētājiem, kas vecāki par 40 gadiem, ar hronisku bronhītu un vēža ģimenes anamnēzē.
ü Bronholoģiskā izmeklēšana: diagnostiskā bronhoskopija, ja nav efekta no adekvātas pneimonijas terapijas, ja ir aizdomas par plaušu vēzi, svešķermenis, biopsija. Ārstnieciskā bronhoskopija abscesa veidošanai, lai nodrošinātu drenāžu.
ü Ultrasonogrāfija sirds un vēdera dobuma orgāni, ja ir aizdomas par sepsi vai infekciozu endokardītu.
ü Izotopu skenēšana plaušas (plaušu angiogrāfija, ja norādīts), ja ir aizdomas par PE.
Pneimonijas netipiskās gaitas cēloņi un raksturs.
Pieejamība smagas somatiskas slimības, smags imūndeficīts, vecums un citi faktori var mainīt pneimonijas gaitu. Iespējams:
ü plaušu iekaisuma fizisko pazīmju neesamība vai zema smaguma pakāpe;
ü drudža neesamība;
ü ekstrapulmonālo simptomu pārsvars (centrālās nervu sistēmas traucējumi u.c.);
ü tipisku izmaiņu trūkums perifērajās asinīs;
ü tipisku radioloģisko izmaiņu trūkums, kas var būt saistīts ne tikai ar pneimonijas variantu, bet arī ar pētījuma vietu un laiku.
Pneimonijas gaitas pazīmes atkarībā no etioloģijas vai varianta.
Priekš pneimokoku KLP raksturīgs akūts sākums, augsts drudzis (39-40°C), sāpes krūtīs, smaga gaita, arteriāla hipotensija, liels infiltrāts, laba reakcija uz penicilīniem.
Stafilokoku pneimonija bieži rodas pēc vīrusu infekcijas, un to raksturo akūts sākums, smaga gaita, mazs infiltrāta izmērs (fokuss, fokuss), tendence uz abscesu veidošanos, bullozas izmaiņas plaušās un rezistence pret penicilīniem.
Haemophilus influenzae izraisa pneimoniju cilvēkiem, kuri slimo ar hronisku bronhītu, alkoholismu un citām hroniskām slimībām, krēpas ir viskozas, viskozas, bieži vien ar asinīm svītrainas, raksturīga smaga klīniska gaita, lieli (polisegmentāli, lobāri) infiltrāti, tendence uz abscesu veidošanos.
Mikoplazma Pneimonija parasti rodas cilvēkiem, kas jaunāki par 35 gadiem, ir ļoti lipīga, tāpēc var rasties epidēmijas uzliesmojumu veidā grupās. Raksturīgs akūts sākums, augsts drudzis ar drebuļiem, augšējo elpceļu infekcijas simptomi (faringīts, laringotraheīts), muskuļu sāpes un galvassāpes, pastiprinošs klepus ar nelielu krēpu daudzumu, gaita parasti nav smaga.
Priekš legionellas Pneimoniju raksturo arī epidēmijas uzliesmojumi cilvēkiem, kuri strādā vai apmeklē mitras, gaisa kondicionētas telpas, smaga klīniskā gaita, caureja, neiroloģiski simptomi un aknu darbības traucējumi.
Rašanās tiekšanās Pirms pneimonijas parasti parādās sāpīgs reflekss klepus, ko bieži pavada spēcīga siekalošanās. Iekaisuma perēkļi bieži ir vairāki, dažāda lieluma, un tiem bieži ir tendence apvienoties. Infiltrācija, kā likums, ir lokalizēta labajā apakšējā daivā, kas ir saistīta ar galveno bronhu sazarojuma raksturu, bet tā var būt arī divpusēja. Aspirācijas pneimoniju raksturo:
ü dokumentēta aspirācija vai aspirācijas attīstībai predisponējošu faktoru klātbūtne;
ü krēpas ar pūšanas smaku;
ü labās plaušas apakšējās daivas pneimonija;
ü nekrotizējoša pneimonija vai abscesa veidošanās, pleiras empiēma;
ü nav mikroorganismu vairošanās aerobos apstākļos.
Pneimonija pacientiem ar novājinātu imunitāti raksturīgs akūts sākums, smaga gaita, drebuļi ar augstu intoksikāciju, tendence uz septisku stāvokli, plaušu un citu iekšējo orgānu abscesa veidošanās. Radioloģiski raksturīgi lobāri un segmentāli infiltrāti ar pleiras izsvīdumu.
Priekš Pneimocistis pneimoniju raksturo plaušu audu intersticiāla iekaisuma klīniskā aina: neproduktīvs klepus vairākas nedēļas, smags elpas trūkums (100% pacientu) un pieaugošas elpošanas mazspējas simptomi, kā arī fizisko izpausmju un pazīmju trūkums. radioloģiskām izmaiņām. Rentgena izpausmes slimības sākumā var nebūt, tad tiek atklāta plaušu audu pneimatizācijas samazināšanās un intersticiāla rakstura palielināšanās. Vairāk nekā pusē gadījumu tiek konstatēti abpusēji mākoņiem līdzīgi infiltrāti ("tauriņa" simptoms), un slimības augstumā tiek konstatētas bagātīgas fokālās ēnas ("kokvilnas" plaušas), kam nepieciešama diferenciāldiagnoze ar diseminētu. tuberkuloze. Līdz 20% Pneumocystis pneimonijas var rasties bez skaidra rentgena attēla. Raksturīga ir neatbilstība starp smagu elpošanas mazspēju un mērenām radioloģiskajām izmaiņām.
Sēnīšu pneimoniju izraisa sēnītes (mikromicīti), bieži vien oportūnistiskas: Aspergillus spp., Criptococcus neoformans, Candida spp. uc Sēnīšu pneimonijas klīniskās izpausmes ir nespecifiskas, nav iespējams noteikt diagnozi, pamatojoties tikai uz klīniskām pazīmēm. Visbiežāk sastopamie simptomi ir drudzis, kas nav izturīgs pret plaša spektra antibiotikām (t > 38°C), kas ilgst vairāk nekā 96 stundas, neproduktīvs klepus, sāpes krūtīs, hemoptīze un elpošanas mazspēja. Sēnīšu pneimonija attīstās ļoti ātri, un to pavada augsta mirstība. Obligātās diagnostikas metodes kopā ar rentgenogrammām ir: augstas izšķirtspējas CT, elpceļu substrātu (krēpu, BAL šķidruma utt.) Mikroskopiskā izmeklēšana ar obligātu kultūru uz uzturvielu barotnēm. Jāņem vērā, ka sēnīšu noteikšana parasti nesterilos biosubstrātos (arī krēpās) notiek kolonizācijas rezultātā, kam nav nepieciešama specifiska apstrāde.
Pneimonijas terapijas principi
ü Adekvāta antibakteriālā terapija.
ü Detoksikācija.
ü Pretiekaisuma terapija.
ü Bronhu drenāžas uzlabošana.
ü Mikrocirkulācijas traucējumu korekcija.
ü Simptomātiska ārstēšana.
Indikācijas hospitalizācijai:
1. Smaga pneimonija*.
ü BH ³ 30 / min.
ü Ķermeņa temperatūra< 35,0 0 С или ³ 40,0 0 С.
ü asinsspiediens< 90/60 мм рт.ст.
ü Pulss > 125/min.
ü Apziņas traucējumi.
ü Leikocitoze > 20,0 G/l vai leikopēnija< 4,0 Г/л
ü Hemoglobīns< 90 г/л
ü Hematokrīts< 30%
ü Kreatinīns > 176,7 µmol/l
ü SaO 2< 90% (по данным пульсоксиметрии)
ü PaO 2< 60 мм рт.ст. и/или PaCO 2 >50 mmHg elpojot telpas gaisu
ü Pneimoniskā infiltrācija ir lokalizēta vairāk nekā vienā daivā
ü Komplikāciju klātbūtne: sabrukšanas dobums(-i), pleiras izsvīdums, ITS.
* Ja ir vismaz viens kritērijs, sabiedrībā iegūta pneimonija tiek uzskatīta par smagu
2. Sākotnējās antibiotiku terapijas neefektivitāte ambulatorā stāvoklī 48-72 stundas.
3. Sociālās indikācijas (nespēja organizēt adekvātu pneimonijas ārstēšanu mājas apstākļos).
Relatīvās indikācijas hospitalizācijai:
ü vecums virs 60 gadiem,
ü smagas blakusslimības (HOPS, ļaundabīgi audzēji, cukura diabēts, hroniska nieru mazspēja, sirds mazspēja, alkoholisms, narkomānija, izsīkums),
ü pacienta un/vai viņa ģimenes locekļu vēlmes.
Lai ātri orientētos konkrēta pacienta vadības taktikā, varat izmantot angļu valodas CRB-65 skalu.
Pneimonijas ārstēšana
Režīms: drudža un intoksikācijas periodam - gulta vai pusgulta, ar sekojošu paplašināšanos.
Diēta: pilnvērtīgs, bagātināts ar vitamīniem, tostarp viegli sagremojamu pārtiku, ar siltuma taupīšanu un palielinātu patērētā šķidruma daudzumu.
Antibakteriālā terapija
Pneimonijas diagnozes noteikšana ir absolūta indikācija antibakteriālās terapijas izrakstīšanai. Pirmā antibiotikas deva jāievada pirmo 4 stundu laikā pēc diagnozes noteikšanas!
Izšķir pneimonijas (ar nezināmu etioloģiju) empīrisko terapiju un noteiktas etioloģijas pneimonijas terapiju.
Zināmas etioloģijas pneimonijas antibakteriālā terapija
S. pneimonija. Izvēles zāles pneimonijas ārstēšanai ir aminopenicilīni(amoksicilīns - iekšķīgi, ampicilīns - parenterāli), t.sk. ar inhibitoriem aizsargāts (amoksicilīns/klavulanāts) un cefalosporīni III paaudze (cefotaksīms, ceftriaksons). Makrolīds Antibiotikas ir alternatīva b-laktāma alerģijām. Viņiem ir augsta aktivitāte elpceļu fluorhinoloni(levofloksacīns, moksifloksacīns), vankomicīns Un linezolīds.
H. gripa. Atlases rīki ir aminopenicilīni(amoksicilīns - iekšķīgi, ampicilīns - parenterāli), t.sk. aizsargāts pret inhibitoriem (amoksicilīns/klavulanāts), cefalosporīni III paaudze (cefotaksīms, ceftriaksons) fluorhinoloni
M. pneimonija, C. pneimonija. Viņiem ir vislielākā aktivitāte pret “netipiskiem” patogēniem makrolīdi, tetraciklīni(doksiciklīns), elpceļu fluorhinoloni.
S. aureus. MSSA izraisītas pneimonijas izvēles zāles ir oksacilīns, alternatīva var būt aizsargāti aminopenicilīni, cefalosporīnies- IIpaaudzes, linkozamīdi. Ja tiek konstatēta MRSA, glikopeptīdu antibiotikas (vankomicīns) vai linezolīds, un pēdējam būtu jādod priekšroka tā farmakokinētisko īpašību dēļ.
Legionellasspp. Leģionāru pneimonijas ārstēšanā, makrolīdi. Arī ļoti efektīva fluorhinoloni(ciprofloksacīns, ofloksacīns, levofloksacīns, moksifloksacīns).
Enterobacteriaceae. Trešās paaudzes cefalosporīniem ir visplašākais darbības spektrs. Slimnīcā iegūtas pneimonijas ārstēšanai nepieciešams iepriekš noteikt jutību pret antibiotikām.
P. aeruginosa. Ceftazidīma un tobramicīna kombinācija tiek uzskatīta par vienu no visizplatītākajām pseudomonas pneimonijas ārstēšanas shēmām. Šī patogēna augstās iegūtās rezistences pret antibiotikām biežums prasa iepriekšēju jutības novērtējumu katrā konkrētajā gadījumā.
Empīriskā ārstēšanas plānošana balstās uz iespējamo slimības etioloģiju (2. tabula).
2. tabula.
Empīriskā antibakteriālā terapija sabiedrībā iegūtas pneimonijas gadījumā ambulatori pacientiem
| Visbiežāk patogēni | Narkotikas pēc izvēles |
|
| Nesmaga CAP pacientiem bez blakus slimībām, kuri pēdējo 3 mēnešu laikā nav lietojuši AMP ≥ 2 dienas | S. pneumoniae M. pneumoniae C. pneumoniae H. influenzae | Amoksicilīns iekšķīgi vai makrolīds iekšķīgi 1 |
| Nesmaga CAP pacientiem ar vienlaicīgām slimībām un/vai kuri pēdējo 3 mēnešu laikā ir lietojuši pretmikrobu medikamentus ≥2 dienas | S. pneumoniae H. influenzae C. pneumoniae S. aureus Enterobacteriaceae | amoksicilīns/klavulanāts, amoksicilīns/sulbaktāms iekšķīgi ± makrolīds iekšķīgi Elpošanas fluorhinolons (levofloksacīns, moksifloksacīns, gemifloksacīns) iekšķīgi |
Piezīme: 1 Makrolīdi ir izvēles zāles, ja ir aizdomas par “netipisku” KLP etioloģiju ( C. pneumoniae, M. pneumoniae). Priekšroka jādod visvairāk pētītajiem CAP makrolīdiem ar uzlabotām farmakokinētiskajām īpašībām (azitromicīns, klaritromicīns) vai labvēlīgu drošības profilu un minimālu zāļu mijiedarbības biežumu (josamicīns, spiramicīns).
3. tabula.
Empīriskā antibakteriālā terapija sabiedrībā iegūtas pneimonijas gadījumā
plkst hospitalizēts pacientiem
| Visbiežāk sastopamie patogēni | ||
| Pneimonija nav smaga strāvas 1 | S. pneumoniae H. influenzae C. pneumoniae S. aureus Enterobacteriaceae | Benzilpenicilīns IV, IM ± makrolīds iekšķīgi 2 Amoksicilīns/klavulanāts IV ± makrolīds iekšķīgi 2 Amoksicilīns/sulbaktāms IV, IM ± makrolīds 2 Cefotaksīms IV, IM ± makrolīds iekšķīgi 2 Ceftriaksons IV, IM ± makrolīds iekšķīgi 2 Ertapenēms IV, IM ± makrolīds iekšķīgi 2 Elpceļu fluorhinolons (levofloksacīns, moksifloksacīns) IV |
| Pneimonija smags kurss 3 | S. pneumoniae Legionellas spp. S. aureus Enterobacteriaceae | Amoksicilīns/klavulanāts IV + makrolīds IV Cefotaksīms IV + makrolīds IV Ceftriaksons IV + makrolīds IV Ertapenēms IV + makrolīds IV Elpošanas fluorhinolons (levofloksacīns, moksifloksacīns) IV + cefotaksīms, ceftriaksons IV |
Piezīme:
1 Priekšroka tiek dota pakāpeniskajai terapijai. Ja pacienta stāvoklis ir stabils, zāļu perorāla ievadīšana ir atļauta nekavējoties.
2 Priekšroka jādod visvairāk pētītajiem CAP makrolīdiem ar uzlabotām farmakokinētiskajām īpašībām (azitromicīns, klaritromicīns) un/vai labvēlīgu drošības profilu un minimālu zāļu mijiedarbības biežumu (josamicīns, spiramicīns).
3 Ja ir riska faktori P. aeruginosa- infekcijas (bronhektāzes , sistēmisko glikokortikoīdu lietošana, plaša spektra antibiotiku terapija ilgāk par 7 dienām pēdējā mēneša laikā, izsīkums) izvēlētās zāles ir ceftazidīms, cefepīms, cefoperazons/sulbaktāms, tikarcilīns/klavulanāts, piperacilīns/tazobaktāms, karbapenēmi (meropenēms, imipenēms), ciprofloksacīns. Visas iepriekš minētās zāles var lietot monoterapijā vai kombinācijā ar II-III paaudzes aminoglikozīdiem. Ja ir aizdomas par aspirāciju, ieteicams lietot amoksicilīnu/klavulanātu, cefoperazonu/sulbaktāmu, tikarcilīnu/klavulanātu, piperacilīnu/tazobaktāmu, karbapenēmus (meropenēmu, imipenēmu).
Sākotnējais efektivitātes novērtējums terapija jāveic pirmajās 48-72 stundās. Galvenie efektivitātes kritēriji ir:
ü ķermeņa temperatūras normalizēšana vai tās pazemināšanās< 37,5°С,
ü intoksikācijas simptomu mazināšana,
ü elpas trūkuma un citu elpošanas mazspējas izpausmju mazināšana.
Ja sākotnēji izvēlētā antibiotika ir neefektīva, vispirms ir jāsavāc biomateriāls bakterioloģiskai izmeklēšanai (krēpas, skalošanas šķidrums), ja tas sākotnēji netika izdarīts, un pēc tam jāmaina antibakteriālais līdzeklis (4. tabula). Ambulatorajiem pacientiem jābūt hospitalizētiem.
4. tabula.
ambulatori pacientiem
| Narkotikas 1. ārstēšanas stadijā | Narkotikas 2. ārstēšanas stadijā | komentāri |
| Amoksicilīns | Makrolīdi | pneumoniae, M. pneumoniae) |
| Amoksicilīns/klavulanāts | Makrolīdi Elpošanas fluorhinoloni | (AR.pneumoniae, M. pneumoniae) |
| Makrolīdi | Amoksicilīns Amoksicilīns/klavulanāts Elpošanas fluorhinoloni | Iespējamais makrolīdu neefektivitātes iemesls ir rezistenti pneimokoki vai gram(-) baktērijas |
5. tabula.
Antibakteriālo zāļu izvēle, ja sākotnējā ārstēšanas shēma ir neefektīva hospitalizēts pacientiem
| Narkotikas 1. ārstēšanas stadijā | Narkotikas priekš Ārstēšanas 2. posms | komentāri |
| Amoksicilīns iekšķīgi Ampicilīns IM | Makrolīdi (aizstāt vai pievienot) III paaudzes cefalosporīni Amoksicilīns/klavulanāts Makrolīds | Iespējamie “netipiski” mikroorganismi (C. pneumoniae, M. pneumoniae, Legionellas spp.), Gram(-) enterobaktērijas, S. aureus |
| Amoksicilīns/klavulanāts Amoksicilīns/sulbaktāms | Makrolīdi (pievienot). Elpošanas fluorhinoloni | Iespējamie “netipiski” mikroorganismi (AR.pneumoniae, M. pneumoniae, Legionellas spp.) |
| Cefalosporīni III paaudze | Makrolīds (pievienot) Elpošanas fluorhinoloni | Iespējamie “netipiski” mikroorganismi (C. pneumoniae, M. pneumoniae, Legionella spp.) |
| Makrolīdi | Amoksicilīns/klavulanāts. Elpošanas fluorhinoloni | Iespējamais makrolīdu neefektivitātes iemesls ir rezistenti pneimokoki vai gram(-) baktērijas |
Pakāpeniska antibakteriāla terapija pneimonijai
Pakāpeniskā antibakteriālā terapija ietver antibakteriālo zāļu divpakāpju lietošanu ar pāreju no parenterālas uz neparenterālu (parasti perorālu) ievadīšanas veidu pēc iespējas īsākā laikā, ņemot vērā pacienta klīnisko stāvokli. Pakāpju terapijas galvenā ideja ir samazināt antibiotikas parenterālās ievadīšanas ilgumu, kas nodrošina ievērojamu ārstēšanas izmaksu samazinājumu un slimnīcas uzturēšanās laiku, vienlaikus saglabājot augstu terapijas klīnisko efektivitāti. Optimālais pakāpju terapijas variants ir vienas un tās pašas antibiotikas divu zāļu formu secīga lietošana, kas nodrošina ārstēšanas nepārtrauktību. Ir iespējams secīgi lietot antibakteriālas zāles, kas ir līdzīgas pēc to mikrobioloģiskajām īpašībām.
Kritēriji pārejai uz perorālu lietošanu kā daļu no pakāpeniskas antibakteriālās terapijas KLP
ü normāla (vai tuvu normālai) ķermeņa temperatūra (mazāka par 37,5°C) ar diviem mērījumiem ar 8 stundu intervālu,
ü elpas trūkuma mazināšana,
ü nav apziņas traucējumu,
ü citu slimības simptomu pozitīva dinamika,
ü uzsūkšanās traucējumu neesamība kuņģa-zarnu traktā,
ü pacientu piekrišana (tieksme) orālai ārstēšanai.
| Injicējamās zāles | Perorālas zāles | Deva, g | Uzņemšanas biežums |
| PENICILĪNI un CEFALOSPORĪNI |
|||
| Benzilpenicilīns 2 miljoni vienību IV (IM) 4 reizes dienā vai Ampicilīns 1-2 g IV (IM) 4 reizes dienā | Amoksicilīns | ||
| Amoksicilīns/klavulanāts, IV 1,2 g 3-4 reizes dienā | Amoksicilīns/klavulanāts | ||
| Cefotaksīms IV (IM) 1,0-2,0 g 2-3 reizes dienā vai Ceftriaksons IV (IM) 1,0-2,0 g 1 reizi dienā | Amoksicilīns/klavulanāts | ||
| MAKROLĪDI |
|||
| Klaritromicīns IV 0,5 g 2 reizes dienā | Klaritromicīns Klaritromicīna pagarinātā izdalīšanās | ||
| Azitromicīns IV 0,5 g vienu reizi dienā | Azitromicīns | ||
| ELPOŠANAS FLUOROHINOLONI |
|||
| Levofloksacīns IV 0,5 g vienu reizi dienā | Levofloksacīns | ||
| Moksifloksacīns IV 0,4 g vienu reizi dienā | Moksifloksacīns | ||
Empīriskā terapija slimnīcā iegūtai pneimonijai
Tā kā slimnīcā iegūtai pneimonijai ir raksturīga ievērojama etioloģijas dažādība, kas apgrūtina empīriskās terapijas plānošanu, pēc klīniskās diagnozes noteikšanas jāveic pēc iespējas ātrāka mikrobioloģiskā diagnostika:
ü krēpu mikrobioloģiskā izmeklēšana (var būt indicēta materiāla iegūšana bronhoskopijas laikā),
ü asins kultūras asins kultūrai.
Plkst pneimonija, kas attīstījās pacientiem vispārējās nodaļās bez riska faktoriem, empīriskās terapijas izvēles līdzekļi pirms etioloģiskās diagnozes noteikšanas var būt parenterālie cefalosporīniIIIpaaudzes maksimālās devās. Tiek apsvērtas alternatīvas fluorhinoloni. Ja ir pierādījumi par labu pseidomonas pneimonijas etioloģiju, ieteicams izrakstīt antipseudomonas kombināciju cefalosporīniIII- IVpaaudzes (ceftazidīms, cefepīms) ar aminoglikozīdiem (tobramicīns, amikacīns).
Plkst pneimonija pacientiem vispārējās nodaļās ar riska faktoriem pastāv liela pseidomonas un citu “neraudzējošo” mikroorganismu etioloģiskās lomas iespējamība. Iespējamās antibiotiku izvēles iespējas:
ü karbapinēmi (imipenēms, meropenēms),
ü III-IV paaudzes antipseudomonālie cefalosporīni kombinācijā ar aminoglikozīdiem,
ü antipseudomonālie penicilīni (azlocilīns, tikarcilīns, piperacilīns) kombinācijā ar aminoglikozīdiem,
ü aztreonāms kombinācijā ar aminoglikozīdiem,
ü fluorhinoloni,
ü glikopeptīdi (vankomicīns).
Empīriska pneimonijas ārstēšana, kas attīstās uz neitropēnijas fona.
Ņemot vērā specifisko etioloģiju, empīriskā terapija ietver glikopeptīdus, kotrimoksazolu un pretsēnīšu zāles.
Aspirācijas pneimonija
Aspirācijas pneimonijas empīriskās terapijas pamatā ir nepieciešamība lietot antibakteriālas zāles ar izteiktu antianaerobo aktivitāti (aizsargāti b-laktāmi, karbapenēmi, metronidazols).
KLP pretmikrobu terapijas pietiekamības kritēriji
ü Ķermeņa temperatūra mazāka par 37,5°C vismaz trīs dienas pēc kārtas
ü Nav reibuma
ü Elpošanas mazspējas trūkums (RR mazāks par 20 minūtē)
ü Strutojošu krēpu trūkums
ü Leikocītu skaits asinīs ir mazāks par 10 G/l, neitrofīli< 80%, юных форм < 6%
ü Negatīvās dinamikas trūkums rentgenogrammā
7. tabula.
Klīniskās pazīmes un apstākļi, kas netiek uzskatīti par indikācijām
lai turpinātu antibiotiku terapiju
| Klīniskās pazīmes | Paskaidrojumi |
| Pastāvīgs zemas pakāpes drudzis (ķermeņa temperatūra | Ja nav citu bakteriālas infekcijas pazīmju, tas var būt neinfekcioza iekaisuma, pēcinfekcijas astēnijas (autonomās disfunkcijas), zāļu drudža izpausme. |
| Atlikušo izmaiņu noturība rentgenogrammā (infiltrācija, palielināts plaušu modelis) | Var novērot 1-2 mēnešus pēc KLP |
| Sausais klepus | Var novērot 1-2 mēnešus pēc CAP, īpaši smēķētājiem un pacientiem ar HOPS |
| Sēkšanas noturība | Sausa sēkšana var tikt novērota 3-4 nedēļas vai ilgāk pēc CAP un atspoguļo slimības dabisko gaitu (lokālā pneimoskleroze iekaisuma fokusa vietā) |
| ESR palielināšanās | Nespecifisks indikators, nevis bakteriālas infekcijas pazīme |
| Pastāvīgs vājums, svīšana | Pēcinfekcijas astēnijas izpausmes |
Aptuvenais antibakteriālās terapijas laiks zināmām etioloģijām:
ü pneimokoku pneimonijas gadījumā - vismaz 5 dienas,
ü pneimonijai, ko izraisa enterobaktērijas un Pseudomonas aeruginosa - 14 dienas,
ü stafilokoku izraisītas pneimonijas gadījumā - 10 dienas,
ü pneimonijas izraisītas pneimonijas gadījumā - 14-21 diena,
ü Legionella izraisītas pneimonijas gadījumā - 21 diena,
ü ar abscesa veidošanos sarežģītu pneimoniju – vairāk nekā 30 dienas
Gadījumos, kad uz klīniskās ainas uzlabošanās fona līdz 4. nedēļas beigām no slimības sākuma nav iespējams panākt pilnīgu fokālo infiltratīvo izmaiņu radioloģisko izzušanu plaušās, jārunā par ilgstošām. KLP.
Šādā klīniskā situācijā, pirmkārt, ir jānosaka iespējamie riska faktori ilgstošai slimības gaitai:
ü vecums virs 55 gadiem;
ü alkoholisms;
ü vienlaicīgu iekšējo orgānu invaliditātes slimību klātbūtne (HOPS, sastrēguma sirds mazspēja, nieru mazspēja, ļaundabīgi audzēji, cukura diabēts utt.);
ü smaga pneimonija;
ü multilobar infiltrācija;
ļoti virulenti patogēni ( L. pneimofila, S. aureus, gramnegatīvās enterobaktērijas);
ü smēķēšana;
ü sākotnējās terapijas klīniskā neefektivitāte (pastāvīga leikocitoze un drudzis);
ü sekundāra bakterēmija;
ü patogēnu sekundārā rezistence pret antibiotikām (vecums > 65 gadi, β-laktāma terapija pēdējo 3 mēnešu laikā, imūndeficīta slimības/stāvokļi).
 Darbības algoritms lēnām pneimonijas atrisināšanai
Darbības algoritms lēnām pneimonijas atrisināšanai
Ja klīniskais uzlabojums netiek novērots un pacientam nav riska faktoru lēnai CAP izzušanai, tad diferenciāldiagnoze ar tādām slimībām kā:
ü lokāla bronhu obstrukcija (audzējs);
ü tuberkuloze;
ü sastrēguma sirds mazspēja;
ü narkotiku drudzis utt.
Detoksikācijas terapija
ü sāls šķīdumi (fizioloģiskie, Ringera uc) 1000-3000 ml,
ü glikoze 5% - 400-800 ml/dienā,
ü hemodez 400 ml/dienā.
Šķīdumus ievada centrālā venozā spiediena un diurēzes kontrolē.
Skābekļa terapija- caur masku, katetriem, mehānisko ventilāciju, atkarībā no elpošanas mazspējas pakāpes.
Pretiekaisuma terapija
NPL (aspirīns, ibuprofēns, diklofenaks u.c.) iekšķīgi vai parenterāli.
Bronhu drenāžas uzlabošana
ü Atrovent, Berodual caur smidzinātāju 4 reizes dienā,
ü mukoregulatori (ambroksols, acetilcisteīns iekšķīgi vai inhalējams)
Mikrocirkulācijas traucējumu korekcija
ü heparīns 20 000 vienības dienā,
ü reopoliglucīns 400 ml/dienā.
Imūnaizstājterapija
ü Gabriglobīns (Gabreglobīns) 1 deva – 2,5 g, ārstēšanas kurss 2,5-10 g 1 reizi dienā 3-10 dienas
Vispārējā terapeitisko pasākumu kompleksā jāiekļauj ārstnieciskā vingrošana. Elpošanas vingrinājumi ne tikai uzlabo ventilāciju un asinsriti, bet ir arī komplikāciju (hipostāzes, atelektāzes, pleiras saaugumi u.c.) profilakses līdzeklis. Nekomplicētas pneimonijas gadījumā rehabilitācijas ārstēšanas programma var sākties un beigties slimnīcas apstākļos. Smagos slimības gadījumos pēc ārstēšanās slimnīcā pacientus var nosūtīt uz specializētām sanatorijām un rehabilitācijas nodaļām. Kompleksās atjaunojošās ārstēšanas izmantošana vairumā gadījumu noved pie pacienta atveseļošanās un darbspēju atjaunošanas.
Fizioterapija plkstpneimonija ir vērsta uz iekaisuma likvidēšanu, ātrākas iekaisuma fokusa rezorbcijas panākšanu, ārējās elpošanas funkcijas, bronhopulmonārās sistēmas limfas un asinsrites uzlabošanu, imūnsistēmas traucējumu atjaunošanu un hiposensibilizējošu efektu.
Kontrindikācijas: smaga intoksikācija, ķermeņa temperatūra virs 38°, II-III pakāpes sirds mazspēja, plaušu asiņošana un hemoptīze, trombembolija, infarkts-pneimonija, pneimotorakss, aizdomas par audzēju.
Pirmajās slimības dienās noteikt elektriskā lauka iedarbību UHF uz krūtīm nepārtrauktā (jauda 40-100 W) vai impulsa (4,5-6 W) režīmā. UHF elektriskajam laukam piemīt pretiekaisuma, asinsriti uzlabojoša, pretsāpju, nervu sistēmas darbību uzlabojoša un desensibilizējoša iedarbība. UHF nedrīkst ordinēt destruktīvas pneimonijas gadījumā. Ieteicams arī ieelpošana fitoncīdi, bronhodilatatori, sārmu šķīdumi, augu novārījumi ar atkrēpošanu, eritēma ultravioletais starojums krūtīs (parasti atsevišķos laukos), kas atbilst skartajai plaušu daivai, viens lauks dienā. Labu efektu infiltrācijas stadijā panāk, lietojot cinkošana krūškurvī uz antibiotiku terapijas fona 20-40 minūtes, ko veic ar intravenozu pilienu ievadīšanu pēc 1/2 - 2/3 šķīduma tilpuma izdzeršanas, un ar intramuskulāru ievadīšanu - 1-1,5 stundas pēc injekcijas. Tas palielina zāļu koncentrāciju iekaisuma fokusā.
Atļaujas darbības laikā tiek noteikts iekaisuma fokuss Mikroviļņu terapija bojājuma zonā vai plaušu apakšējās daivas. Atšķirībā no UHF mikroviļņu elektriskais lauks iedarbojas nevis uz visu ķermeni, bet gan lokāli, uz iekaisuma zonu. Tas pats princips tiek izmantots induktotermija(apstrāde ar augstfrekvences mainīgu magnētisko lauku), izmantojot zemas termiskās un termiskās devas. Induktotermijai ir sedatīvs, spazmolītisks, pretsāpju efekts, samazinās audu muskuļu tonuss, paplašinās asinsvadi, atveras neaktīvie kapilāri, palielinās asins plūsma, palielinās fagocitozes un nespecifiskās imunitātes aktivitāte un intensitāte, uzlabojas simpatoadrenālās sistēmas darbība.
Tajā pašā periodā slimība tiek veikta magnētiskā terapija izmantojot zemfrekvences (50 Hz) magnētisko lauku nepārtrauktos vai intermitējošos režīmos, kas labvēlīgi ietekmē sirds un asinsvadu sistēmas funkcijas, izraisot šīs metodes priekšrocību pacientu ar vienlaicīgu sirds un asinsvadu patoloģiju ārstēšanā. Magnētiskās terapijas kontrindikācijas ir pacienta vispārējais nopietnais stāvoklis, ķermeņa temperatūra virs 38 o C, smaga hipotensija, III stadijas hipertensija, asiņošana vai tendence uz asiņošanu, sistēmiskas asins slimības, kaheksija, recidivējošais tromboflebīts, ādas defekti apvidū. ārstēšana
Lai uzlabotu iekaisuma fokusa rezorbciju un novērstu bronhu spazmas, sāpes un apgrūtinātu krēpu izdalīšanos, izmantojiet elektroforēze kalcijs, magnijs, heparīns, aminofilīns, alvejas ekstrakts, askorbīnskābe, lizocīms. Šajā gadījumā viens elektrods (100-150 cm 2) tiek novietots starplāpstiņu rajonā, otrais - ņemot vērā iekaisuma avota lokalizāciju.
Iekaisuma fokusa izzušanas periodā izmantojiet ieelpošana ar atkrēpošanas līdzekļiem, mukolītiskajiem līdzekļiem, atjaunojošiem medikamentiem, kā arī termoterapija– ozokerīta, parafīna, dūņu un kūdras dūņu aplikācijas. 2-3.nedēļā var nozīmēt klimatoterapeitiskās procedūras (dienas uzturēšanās verandā, gaisa vannas).
Visas metodes ir apvienotas ar vingrošanas terapiju un masāžu. Fizikālā terapija ir indicēta 2-3 dienā no brīža, kad ķermeņa temperatūra normalizējas. Izmantojiet vingrinājumus, kas palīdz palielināt krūškurvja sienas elpošanas mobilitāti, stiept pleiras saaugumus, stiprina elpošanas muskuļus un vēdera muskuļus.
Ārstēšanas laikā ilgstoša pneimonija Nozīmīgākas kļūst rūdīšanas metodes (ūdens beršana, dušas), klimata terapija (sanatorijā vai rehabilitācijas nodaļā), vispārējā UV apstarošana, aerosola terapija ar atkrēpošanas līdzekļiem, mukolītiskajiem un atjaunojošiem medikamentiem.
Klīniskā izmeklēšana.
Dispanseru novērošana tiek veikta 6 mēnešus ar vietējā terapeita apmeklējumiem 1, 3 un 6 mēnešus pēc izrakstīšanas. Vispārējo asins analīzi, krēpu testu, fluorogrammu, spirogrammu veic divas reizes, pēc 1 un 6 mēnešiem, bioķīmisko asins analīzi - vienu reizi pēc 6 mēnešiem. Ja nepieciešams, tiek veiktas LOR ārsta, zobārsta un pulmonologa konsultācijas. Labsajūtas aktivitātes: vitamīnu terapija, vingrošanas terapija, pirts, infekcijas perēkļu sanācija, akūtu elpceļu vīrusu infekciju un gripas profilakse, smēķēšanas atmešana, nosūtīšana uz specializētām sanatorijām.
Testa jautājumi par tēmu.
1. Pneimonijas definīcija.
2. Pneimonijas klasifikācija.
3. Pneimonijas klīniskās un instrumentālās pazīmes.
4. Galvenie pneimonijas izraisītāji.
5. Pneimonijas gaitas pazīmes atkarībā no patogēna.
6. Pneimonijas terapijas principi.
7. Empīriskā antibiotikas izvēle.
8. Pakāpju terapija.
9. Efektivitātes un antibiotiku atcelšanas kritēriji.
10. Pneimonijas kompleksā terapija.
11. Ilgstoša pneimonijas gaita: cēloņi un taktika.
12. Pneimonijas fizioterapija.
13. Klīniskā novērošana pēc pneimonijas.
Diagnostikas algoritms sabiedrībā iegūtai pneimonijai


Nozokomiālās pneimonijas diagnostikas meklēšanas algoritms
Kopienā iegūta pneimonija: diagnostika un diferenciāldiagnoze
A.I. Sinopaļņikovs
Kolektīvo terminu "pneimonija" parasti lieto, lai apzīmētu akūtu infekciozu (galvenokārt bakteriālu) plaušu elpceļu daļu bojājumu grupu, kas atšķiras pēc etioloģijas, patoģenēzes un morfoloģiskajām īpašībām ar intraalveolāru eksudāciju, kas izpaužas. ar drudžainu reakciju, intoksikāciju, kas izteikta dažādās pakāpēs un konstatēta fiziskās un rentgenoloģiskās pārbaudēs.
Visizplatītākā klasifikācija ir tāda, kurā ņemti vērā apstākļi, kādos slimība attīstījās, plaušu audu infekcijas pazīmes, kā arī organisma imunoloģiskā reaktivitāte. Pareiza šo faktoru apsvēršana ļauj ar ievērojamu varbūtības pakāpi prognozēt slimības etioloģiju un galu galā izvēlēties atbilstošu empīriskās pretmikrobu ķīmijterapijas virzienu. Saskaņā ar šo klasifikāciju izšķir šādus pneimonijas veidus:
a) sabiedrībā iegūta (iegūta ārpus medicīnas iestādes) pneimonija (sinonīmi: mājas, ambulatorā);
b) nozokomiālā (iegūta ārstniecības iestādē) pneimonija (sinonīmi: slimnīca, nozokomiāla);
Aleksandrs Igorevičs Sinopaļņikovs - profesors, pulmonoloģijas katedras vadītājs ar ftizioloģijas kursu Krievijas Federācijas Aizsardzības ministrijas Valsts ārstu padziļinātās apmācības institūtā.
c) aspirācijas pneimonija;
d) pneimonija personām ar smagiem imūndeficītiem (iedzimts imūndeficīts, HIV infekcija, jatrogēna imūnsupresija).
Praktiski nozīmīgākā ir pneimonijas iedalījums sabiedrībā iegūtajā un nozokomiālā. Jāuzsver, ka šādam dalījumam nav nekāda sakara ar slimības smagumu, un galvenais un vienīgais diferenciācijas kritērijs ir vide, kurā attīstījās pneimonija.
Termins "sabiedrībā iegūta pneimonija" apzīmē akūtu slimību gadījumus, kas radušies sabiedrībā.
noteiktos apstākļos, ko pavada apakšējo elpceļu infekcijas simptomi (drudzis, klepus ar krēpām, iespējams, strutojošs, sāpes krūtīs, elpas trūkums) un radioloģiskās pazīmes par “svaigām” fokusa-infiltratīvām izmaiņām plaušās, ja nav acīmredzamas diagnostikas. alternatīva.
Diagnostika
Pneimonijas diagnozes noteikšanu sarežģī fakts, ka nav specifisku klīnisku pazīmju vai pazīmju kombinācijas, uz kurām varētu droši paļauties, lai aizdomas par šo diagnozi. Drīzāk nespecifisku simptomu neesamība vai lokālas steto-akustikas trūkums
Šādas izmaiņas plaušās samazina pneimonijas diagnozes iespējamību.
Kopumā sabiedrībā iegūtas pneimonijas (CAP) galvenās klīniskās un radioloģiskās pazīmes var formulēt šādi:
Klīnisko pazīmju un radioloģisko datu analīze dažos gadījumos ļauj izdarīt pieņēmumu par konkrētu patogēnu, taču šai informācijai ir relatīva vērtība;
Streptococcus pneumoniae (bieži vien iespējams izolēt pneimokoku no asinīm), daļēji Legionella spp., retāk citiem patogēniem ir raksturīga pēkšņa parādīšanās, drudzis, drebuļi, pleiras sāpes krūtīs, lobāra infiltrācija. Gluži pretēji, šis attēls nav raksturīgs Mycoplasma pneumoniae un Chlamydophila (Chlamydia) pneumoniae;
"klasiskās" pneimonijas pazīmes (akūts febrils sākums, sāpes krūtīs utt.) var nebūt, īpaši novājinātiem vai gados vecākiem pacientiem;
Apmēram 25% pacientu ar VbP, kas vecāki par 65 gadiem, nav drudža, un leikocitoze tiek reģistrēta tikai 50-70%. Šajā gadījumā simptomus var attēlot vājums, slikta dūša, anoreksija, sāpes vēderā, intelektuālie-mnestiskie traucējumi;
Novēlota diagnostika un novēlota antibakteriālās terapijas uzsākšana noved pie sliktākas prognozes: mirstība pacientiem, kas vecāki par 65 gadiem, sasniedz 10-25%;
Visbiežāk sastopamās pneimonijas radioloģiskās pazīmes ir
Aizdomas par pneimoniju vienmēr vajadzētu rasties, ja pacientam ir drudzis kopā ar sūdzībām par klepu, elpas trūkumu, krēpu izdalīšanos un/vai sāpēm krūtīs.
aklftsA, [ishmtyupya par “ischplssh 3*2003 7
mm. FD-pduu
fokusa ēnas parādās viena vai vairāku segmentu projekcijā;
Lobāras infiltrācijas gadījumos “gaisa bronhogrammas” fenomens tiek vizualizēts 33% pacientu;
Pleiras izsvīdums sarežģī PBP gaitu 10-25% gadījumu, un tam nav īpašas nozīmes slimības etioloģijas prognozēšanā;
Destrukcijas dobumu veidošanās plaušās nav raksturīga pneimokoku, mikoplazmas un hlamīdiju pneimonijai, bet drīzāk liecina par labu stafilokoku infekcijai, zarnu grupas aerobajiem gramnegatīvajiem patogēniem un anaerobiem;
Retikulonodulāra infiltrācija plaušu bazālajās daļās ir raksturīga mikoplazmas pneimonijai (tomēr 20% gadījumu to var pavadīt fokusa konfluenta infiltrācija vairāku segmentu vai pat daivu projekcijā).
Aizdomas par pneimoniju vienmēr vajadzētu rasties, ja pacientam ir drudzis kopā ar sūdzībām par klepu, elpas trūkumu, krēpu izdalīšanos un/vai sāpēm krūtīs. Pacienti, kas cieš no pneimonijas, bieži sūdzas par nemotivētu vājumu, nogurumu un spēcīgu svīšanu naktī.
VBP pacientu fiziskās apskates laikā iegūtā informācija ir atkarīga no daudziem faktoriem, tostarp no slimības smaguma pakāpes, pneimonijas infiltrācijas izplatības, vecuma un blakusslimību klātbūtnes. Klasiskās objektīvās pneimonijas pazīmes ir perkusijas tonusa saīsināšanās (blāvums) skartajā plaušu zonā, lokāli auskultēta bronhu elpošana, skaņu smalku rēguļu vai ieelpas krepita fokuss, pastiprināta bronhofonija un balss trīce. Tomēr dažiem pacientiem objektīvās pneimonijas pazīmes var atšķirties no tipiskām vai vispār nebūt (apmēram 20% pacientu).
Krūškurvja rentgenogrāfija
Šis ir vissvarīgākais diagnostikas tests. Gandrīz vienmēr, lai diagnosticētu VbP, ir jānosaka fokusa infiltratīvas izmaiņas plaušās kombinācijā ar atbilstošiem simptomiem. Un, lai gan pastāv viedoklis, ka fokālās infiltrācijas stetoakustiskās pazīmes parasti sakrīt ar radiogrāfiskiem datiem, daudzi pētījumi ir parādījuši to zemo jutību un specifiskumu pneimonijas diagnostikā.
Ir vairāki iemesli, kas izskaidro viltus negatīvus rentgena rezultātus pacientiem ar pneimoniju. Tie ietver dehidratāciju (tomēr šai teorijai nav pietiekami daudz datu), dziļu neitropēniju
niya, kas neļauj attīstīties lokalizētai akūtai iekaisuma reakcijai plaušu audos, slimības sākuma stadijās (tiek uzskatīts, ka auskultācija var atpazīt pneimoniju pat dienu pirms infiltrācijas parādīšanās rentgenogrammā) un, visbeidzot, gadījumi Pneumocystis carinii izraisīta pneimonija HIV inficētiem pacientiem (10-20% pacientu nav radioloģisko izmaiņu).
Dažreiz rodas diagnostikas problēmas, kas saistītas ar kļūdaini pozitīviem rentgena izmeklēšanas rezultātiem (skatīt zemāk).
Krūškurvja rentgena vērtība ir ne tikai pneimonijas diagnozes pārbaudē (parasti atbilstošu klīnisko pazīmju klātbūtnē), procesa dinamikas un atveseļošanās pilnīguma novērtēšanā. Izmaiņas rentgenogrammā (infiltrācijas izplatība, pleiras izsvīduma esamība vai neesamība, iznīcināšana) atbilst slimības smagumam un kalpo kā sava veida “ceļvedis” antibakteriālās terapijas izvēlē.
Citi pētījumi
Klīniskā asins analīze ir standarta diagnostikas tests. Acīmredzot ne kopējais leikocītu skaits perifērajās asinīs, ne leikocītu formula neļauj mums droši runāt par iespējamo pneimonijas izraisītāju. Tomēr leikocitoze vairāk nekā 10-12 x 109/L norāda uz lielu bakteriālas infekcijas iespējamību, un leikopēnija zem 3 x 109/L vai leikocitoze virs 25 x 109/L ir nelabvēlīgas prognostiskas pazīmes.
Standarta pētījumu metodes pacientiem ar VbP, kuriem nepieciešama hospitalizācija, ietver bioķīmiskās asins analīzes, tostarp aknu un nieru funkcionālos testus, kā arī elektrolītu līmeņa analīzi.
Hospitalizētiem pacientiem ar VbP ir nepieciešams veikt mikrobioloģiskos pētījumus: asins kultūras divas reizes (pirms antibiotiku izrakstīšanas), produktīva klepus klātbūtnē - ar gramu krāsotas krēpu uztriepes un tās kultūras bakterioskopiju (skatīt zemāk).
Pacientiem ar elpošanas mazspējas simptomiem, ko izraisa plaša pneimonija infiltrācija, masīvs pleiras izsvīdums, pneimonijas attīstība uz hroniskas obstruktīvas plaušu slimības fona, nepieciešams noteikt arteriālās asins gāzes. Šajā gadījumā hipoksēmija ar pO2 līmeņa pazemināšanos zem 60 mm Hg. Art. prognostiski nelabvēlīga un norāda uz nepieciešamību ievietot pacientu intensīvās terapijas nodaļā.
Pleiras izsvīduma klātbūtnē un drošas pleiras punkcijas apstākļos (brīvi pārvietota šķidruma laterogrammas vizualizācija ar slāņa biezumu >1,0 cm), pleiras šķidruma izpētē jāiekļauj leikocītu skaitīšana ar leikocītu formulu, pH, laktātdehidrogenāzes noteikšana. aktivitāte, olbaltumvielu saturs, krāsošanās gramu uztriepes un
Fokālās infiltrācijas plaušās radioloģiskā apstiprinājuma neesamība vai neesamība padara pneimonijas diagnozi neprecīzu/nedrošu.
Iespējamie VbP izraisītāji atkarībā no tā rašanās apstākļiem
Rašanās apstākļi Iespējamie patogēni
Alkoholisms Hronisks bronhīts/tabakas smēķēšana Dekompensēts cukura diabēts Uzturēšanās pansionātos Neattīrīts mutes dobums Gripas epidēmija Masīva aspirācija Pneimonijas attīstība bronhektāzes, cistiskās fibrozes dēļ Intravenoza narkotiku atkarība Lokāla bronhu obstrukcija (piemēram, plaušu vēzis, utt.) Kontakts ar gaisa kondicionētājiem . Slimības uzliesmojums sabiedrībā (skolēni, militārpersonas) S. pneumoniae, anaerobi, aerobās enterobaktērijas (Klebsiella pneumoniae u.c.) S. pneumoniae, Haemophilus influenzae, Moraxella catarrhalis, Legionella spp. S. pneumoniae, Staphylococcus aureus S. pneumoniae, Enterobacteriaceae, H. influenzae, S. aureus, Chlamydophila pneumoniae, anaerobi Anaerobes S. pneumoniae, S. aureus, Streptococcus pyogenes, H. influenzae Anaerobes Pseeruciau, S. S. aureus, anaerobi Anaerobi Legionella pneumophila S. pneumoniae, Mycoplasma pneumoniae, Chlamydophila pneumoniae
nē Bartlett J.G. Elpošanas ceļu infekciju vadība. Filadelfija, 1999. Mandell L.A. un citi. // Klin. Inficējiet. Dis. 2000. V. 31. P 383.
skābes izturīgas baktērijas, kultūra aerobiem, anaerobiem un mikobaktērijām.
VbP diagnostika
VbP diagnoze ir noteikta, ja pacientam ir radioloģiski apstiprināta plaušu audu fokāla infiltrācija un vismaz divas klīniskās pazīmes no sekojošām:
a) akūts drudzis slimības sākumā (ķermeņa temperatūra >38,0°C);
b) klepus ar krēpu;
c) fiziskas pazīmes (krepita fokuss un/vai smalkas rales, skarba bronhu elpošana, perkusiju skaņas saīsināšana);
d) leikocitoze >10 x 109/l un/vai joslu nobīde (>10%).
Ja iespējams, jācenšas iegūt VbP diagnozes klīnisku un radioloģisku apstiprinājumu. Šajā gadījumā ir jāņem vērā zināmu sindromam līdzīgu slimību/patoloģisku stāvokļu iespējamība.
Fokālās infiltrācijas plaušās radioloģiskā apstiprinājuma neesamība vai neesamība padara VbP diagnozi neprecīzu/nedrošu. Šajā gadījumā slimības diagnoze balstās uz anamnēzes, sūdzību un atbilstošo vietējo simptomu ņemšanu vērā.
Ja, izmeklējot pacientu ar drudzi, sūdzībām par klepu, elpas trūkumu, krēpu izdalīšanos un/vai sāpēm krūtīs, rentgena izmeklēšana nav pieejama un nav lokālu stetoakustisku simptomu, tad pieņēmums par VbP kļūst maz ticams.
Etioloģiskā diagnoze
Acīmredzami, ka VbP fakta konstatēšana, balstoties uz fizisko un radioloģisko izmeklējumu rezultātiem, ir pielīdzināma tikai sindromiskai diagnozei, bet nosoloģiska tā kļūst pēc patogēna noteikšanas. Beznosacījumu pierādījums mikroorganisma cēloņsakarībai pneimonijas attīstībā ir tā izolēšana no plaušu audiem, bet klīnicistam ir jāuzticas mikroorganismu rezultātiem.
bioloģiskās asins analīzes (pozitīvas 6-10% gadījumu), pleiras šķidrums, krēpas (iespējams bronhu sekrēta piesārņojums, ejot caur orofarneksu) vai imūnseroloģiskie testi, kā arī anamnēzes dati (tabula).
Standarta pētījumu metodes ir bakterioskopija ar Grama krāsošanu un krēpu kultūra, kas iegūta dziļi klepojot. Pirms mikrobioloģiskā pētījuma uzsākšanas nepieciešams nokrāsot uztriepi atbilstoši gramam. Ja uztriepē ir mazāk nekā 25 leikocīti un vairāk nekā 10 epitēlija šūnas, turpmāka izmeklēšana nav ieteicama (visticamāk, materiāls atspoguļo mutes dobuma saturu). Uztriepes noteikšana ievērojamam skaitam grampozitīvu vai gramnegatīvu mikroorganismu ar tipisku morfoloģiju (grampozitīvi lansolāti diplokoki - S. pneumoniae; grampozitīvu koku uzkrājumi kopu veidā - S. aureus, gram- negatīvie kokobacilli – H. influenzae) var kalpot kā ceļvedis
antibakteriālās terapijas recepte. Krēpu izmeklēšanas rezultātu diagnostiskā vērtība ir vērtējama kā augsta, ja potenciālais patogēns ir izolēts koncentrācijā, kas lielāka par 105 KVV/ml (KVV - koloniju veidojošās vienības).
Acīmredzot bakterioskopijas un krēpu kultūras rezultātu interpretācija jāveic, ņemot vērā klīniskos datus.
Smagi slimiem pacientiem, tostarp lielākajai daļai hospitalizēto pacientu, pirms antibiotiku terapijas uzsākšanas jāveic divas venozo asiņu kultūras (asinis ņemtas no dažādām vietām ar vismaz 10 minūšu intervālu).
Savācot krēpu, jāievēro šādi noteikumi:
1. Krēpas tiek savāktas pirms ēšanas, ja iespējams, pirms antibakteriālās terapijas uzsākšanas.
2. Pirms krēpu savākšanas rūpīgi jāizskalo mute ar vārītu ūdeni.
3. Pacientam ir norādīts iegūt apakšējo elpceļu saturu, nevis orofarneksu.
4. Krēpu savākšana jāveic sterilos traukos.
5. Paraugu uzglabāšanas ilgums istabas temperatūrā nedrīkst pārsniegt 2 stundas.
mm. vbpavr «re- phju
Lai gan pirms antibiotiku izrakstīšanas ir svarīgi iegūt laboratorijas materiālu, mikrobioloģiskie izmeklējumi nedrīkst būt par iemeslu, lai atliktu antibakteriālo ārstēšanu. Tas jo īpaši attiecas uz pacientiem ar smagu slimību.
Seroloģiskā diagnoze
infekcijas Mycoplasma pneumoniae, Chlamydophila (Chlamydia) pneumoniae un Legionella nav uzskatāmas par obligātajām pētījumu metodēm, jo, ņemot vērā atkārtotu asins seruma ņemšanu akūtā periodā un atveseļošanās periodā (vairākas nedēļas no slimības sākuma ), tā nav klīniska, bet gan epidemioloģiskā līmeņa diagnostika
Pašlaik ārvalstīs plaši izplatīts ir ar enzīmu saistīts imūnsorbcijas tests, lai noteiktu specifisko šķīstošo Legionella pneumophila antigēnu (1. serotips) urīnā smagas VbP gadījumā. Od-
Taču mūsu valstī šīs dārgās legionellas infekcijas ātrās diagnostikas metodes izmantošana nav izplatījusies tālāk par atsevišķiem klīniskajiem centriem. Streptococcus pneumoniae antigēna noteikšana urīnā tiek uzskatīta par daudzsološu papildu metodi, taču pieejamie dati ir nepietiekami, lai sniegtu skaidrus ieteikumus.
Polimerāzes ķēdes reakcijas (PCR) metode attīstās ļoti ātri un šķiet daudzsološa tādu CAP patogēnu kā C. pneumoniae un M. pneumoniae diagnosticēšanai. Tomēr šo metodi vēl nevar ieteikt plaši izplatītai klīniskai praksei.
Fiberoptiskā bronhoskopija ar iegūtā materiāla mikrobu piesārņojuma kvantitatīvu novērtējumu (“aizsargāta” otas biopsija, bronhoalveolāra skalošana) vai citas invazīvas diagnostikas metodes (transtraheālā aspirācija, transtorakālā
biopsija utt.) ir paredzētas noteiktiem gadījumiem: pneimonija pacientiem ar imūnsupresiju, aizdomas par plaušu tuberkulozi, ja nav produktīva klepus, obstruktīvs pneimonīts plaušu vēža vai svešķermeņa aspirācijas gadījumā utt.
Diemžēl subjektīvo un objektīvo grūtību dēļ: nepareiza materiāla savākšana vai krēpu trūkums, kļūdas mikrobioloģiskajā izmeklēšanā, ierastā prakse, ka pacienti lieto antibakteriālos medikamentus pirms ārsta apmeklējuma (piemēram, pat vienas devas potenciāli efektīvas antibiotikas lietošana liek to darīt). maz ticams, ka pneimokoku kultūra ir izolēta) - daudzos gadījumos pneimonijas izraisītāju nevar noteikt.
Diferenciāldiagnozes jautājumi tiks apspriesti nākamajā žurnāla numurā.
Glikokortikosteroīda un bronhodilatatora kombinācija bromiālās astmas pamatterapijai
BrJLÖKOE GLESTNO0 PRITIYYUSPNPISHPNOV UN BRANZHOPIPINSNIV DARBĪBA.
Valsts pieteikums "■-? inhalācijām
■ Voem^nost devu samazināšana I PKKSKORTI ’■OO BRONLOLYTIKE G pL-
pilnīga kontrole ar bronhiālās astmas simptomiem^ r / luchcinir dzīves kvalitāte ^nn Solnykh brpnkiapg.npi zgtmoi
Uzlabojums 2d un p*d pa ni mania g tatsIvita.
¿Oiikmie Aoimoeti (¡aensnoI teraschi salīdzinājumā ar atsevišķiem pri^i^nyaei inhalatoriem
ĒRTI UN EFEKTĪVI i
T’SliV I JSeuihCJiHLS P[imtchkg L H. KCfin W* \ Imnt^Ki (0&5J SiW-iSiiQ.
PUPMED
ē un es! 11 »-■:+ h s-a vt- ■:-c-:-r uw u -m ktim
10) !M"Sf"rA. PuAKDONTOPN. Šumeli 3*2003
Visu veidu elpošanas sistēmas slimības ir diezgan līdzīgas viena otrai un izraisa gandrīz tādas pašas negatīvas sekas ķermenim, kad rodas iekaisums. Plaušu audu iekaisumu var izraisīt ne tikai elpošanas sistēmas slimības vai patogēni mikroorganismi, kuru vidū ir baktērijas, vīrusi un sēnītes, bet arī visa veida traucējumi citu orgānu darbībā, piemēram, ar insultu, alerģijām vai. problēmas ar centrālo vai perifēro nervu sistēmu.
Starptautiskajā slimību klasifikācijā iekaisuma process plaušu audos tiek saukts par pneimoniju un tautā – pneimoniju, kurai ir sazarota klasifikācija pēc etioloģijas, lokalizācijas un arī norises rakstura.
Šī slimība ir ļoti bīstama cilvēkiem, tā var attīstīties ļoti ātri un dažreiz latenti, atstāt lielu skaitu nopietnu komplikāciju gan plaušu, gan neplaušu rakstura, kā arī tai ir augsts mirstības līmenis.
Pneimonijas ārstēšana ir daudz efektīvāka un vienkāršāka, ja slimība tiek atklāta agrīnās stadijās un nekavējoties tiek uzsākta ārstēšana.
Kāda ir pneimonijas diferenciāldiagnoze
Jebkuras slimības, tai skaitā pneimonijas, noteikšanai tiek izmantotas noteiktas diagnostikas metodes: laboratorijas (visa veida audu, šķidrumu, sekrēciju izmeklējumi), instrumentālie (kas atspoguļo pacienta aparatūras pētījumu: tomogrāfija, rentgens, ultraskaņa), diferenciāldiagnoze un vienkārša pārbaude.
Pneimonijas diferenciāldiagnoze ir izpētes metode, saskaņā ar kuru tiek veikta diagnoze, izslēdzot pacientam slimības ar līdzīgām izpausmēm.
Šo pētījumu metodi izmanto gadījumos, kad precīzs slimības cēlonis nav konkrēti zināms, piemēram, iesnas var būt alerģiskas, vīrusu, bakteriālas vai vispār kādu orgānu darbības traucējumu rezultāts un trešdaļa no vēža. pacienti sākotnēji uzstāda nepareizu diagnozi, mēģinot ārstēt neesošu slimību, kamēr onkoloģija klusi aug.

Lai nekavējoties un precīzi noteiktu jebkuru slimību un noteiktu tās cēloni, ir burtiski rūpīgi jāanalizē slima cilvēka ķermenis un dažreiz arī viņa prāts. Ne viens, ne otrs diemžēl nav iespējams pat ar vismodernākajām iekārtām un zinātniskajām tehnoloģijām, tāpēc ārsti nereti ir spiesti rīkoties nejauši vai ar izslēgšanu.
Šīs izpētes metodes laikā ārsts savāc pēc iespējas vairāk datu par pacientu, viņa dzīvesveidu, visām reakcijām, kas notiek viņa organismā, analizē slimības vēsturi un salīdzina visus iegūtos jaunos datus ar iespējamo diagnožu sarakstu un to īpašībām. Mūsdienu medicīnā dažkārt tiek izmantota pat pneimonijas un citu slimību, arī garīgo, datordiferenciāldiagnostika, kas veic salīdzinājumus, izmantojot datoru.
Pamatojoties uz iegūtajiem rezultātiem, pacientam tiek veikta diferenciāldiagnoze, ko var apstiprināt klīniski.
Diferenciāļa iestatīšana Pneimonijas un citu slimību diagnoze notiek šādi:
- Pirmkārt, tiek pilnībā noteikti simptomi un piemērotāko diagnožu klāsts.
- Pēc tam tiek apkopoti visdetalizētākie slimības raksturojumi un galvenie varianti, kuriem šī slimība var atbilst.
- Trešajā posmā tie tiek salīdzināti.
- Tālāk, pieliekot prāta piepūli un zināmu diagnostista iztēli, tiek izolēts visticamākais variants un noteikta precīza diagnoze.

No pirmā acu uzmetiena šī izpētes metode šķiet ļoti tālu un neuzticama, tomēr vairumā gadījumu tā ir visefektīvākā, ja simptomi rada šaubas, un tai ir ļoti augsts precizitātes procents.
Pneimonijas diferenciāldiagnoze ir vienkārši nepieciešama, ja pacientam ir kādas pavadošas elpošanas sistēmas vai citu orgānu slimības, kas var noslīcināt vai izkropļot simptomus un tos sajaukt. Šī pētījuma metode ļauj šajā gadījumā izolēt pneimoniju no pamatslimības simptomiem un sākt ārstēšanu laikā.
Fokālā pneimonija un plaušu vēzis
Viens no gadījumiem, kad diferenciāldiagnozi vienkārši nevar izvairīties, ir plaušu vēža izraisīta pneimonija, kurai ir vairākas specifiskas pazīmes.
Pirmkārt, uz plaušu audu vēža fona pacientiem vienmēr attīstās akūta pneimonija, kas vēl nesen šādu pacientu dzīvības prasīja ātrāk nekā pats vēzis, līdz tas tika atklāts.
Iekaisuma process sākas tieši audzēja veidošanās zonā, to izraisa liela skaita patogēnu kombinācija un pastiprina tā augšanu, kas, savukārt, stimulē pneimonijas attīstību.
Pneimonijas simptomi uz vēža fona bieži ir praktiski nemanāmi, jo, tiešām, ko gan var nozīmēt veselības pasliktināšanās, nespēks un drudzis uz tik šausmīgas slimības un vēl jo vairāk ķīmijterapijas fona.

Arī ar instrumentālās izpētes metodēm nav iespējams nejauši ieraudzīt iekaisuma sākšanos, jo to fiziski klāj audzējs, kā arī tomogrāfiskās izmeklēšanas laikā tas uzsūc arī visus asinīs ievadītos ķīmiskos marķierus, kas iekrāso audzēju un nereaģē. citām problēmām.
Turklāt plaušu vēzim metastāžu un pneimonijas periodā ir ļoti līdzīgi galvenie simptomi: krēpas, klepus, sāpes krūtīs, apgrūtināta elpošana, elpas trūkums, hemoptīze utt.
Papildus pašam plaušu vēzim līdzīgu efektu rada metastāzes elpošanas sistēmā no galvenā audzēja, kas atrodas citā orgānā. Pirms metastāzes plaušu vēzis ir pilnīgi asimptomātisks.
Tikai nelielas atšķirības var precīzi noteikt, kā pneimonija ir sākusies. Pneimonijas pazīmes:
- Kā slimība sākas: spilgts, akūts sākums.
- Klepus apraksts: sākumā tā var nebūt, var būt dažādas produktivitātes pakāpes un var sniegt vai neapmierināt pacientu.
- Elpas trūkuma apraksts: sākas ar lielu bojājumu vai pietūkumu.
- Kā notiek hemoptīze: reti slimības akūtās stadijās ar smagu formu.
- Sāpju krūtīs raksturojums: visbiežāk saistītas ar elpošanu un kustībām.
- Intoksikācijas smagums: mainās atkarībā no smaguma pakāpes.
- Fiziskie dati: plaušās ir dzirdami mitri raļļi un mainās elpošanas modelis.
- Reakcija uz antibiotikām: pēc vienas līdz pusotras nedēļas ilgas antibiotiku lietošanas process mainās.
- Laboratorisko izmeklējumu rezultāti: ļoti spēcīgs ESR un leikocitozes pieaugums.
- Rentgena starojums: plaušu saknes ir palielinātas (to piestiprināšanas vietas pie galvenajiem bronhiem un asinsvadiem), tiek uzlabots plaušu modelis, pati skartā zona izskatās viendabīga ar izplūdušām malām.

Vēža gadījumā tiek novērotas šādas pazīmes:
- Biežākais pacientu vecums ir virs piecdesmit gadiem, ievērojams smēķētāju pārsvars.
- Visbiežāk sastopamā pacienta dzimums: nav.
- Kā slimība sākas: maigi un nemanāmi, pakāpeniski paaugstinot temperatūru.
- Klepus apraksts: bieži nav.
- Elpas trūkuma apraksts: var nebūt.
- Kā notiek hemoptīze: tā parādās tikai tad, kad metastāzes iekļūst pleiras zonā.
- Sāpju krūtīs raksturojums: dažreiz nav, bet biežāk ir.
- Intoksikācijas smagums: nav izteikts.
- Fiziskie dati: nav izmaiņu elpošanā vai pareizas plaušu darbības skaņas.
- Reakcija uz antibiotikām: vai nu pilnīgi nav, vai arī pacients sāk justies labāk, bet rentgena rezultāti nemainās.
- Laboratorisko izmeklējumu rezultāti: leikocīti ir normāli, ESR ir mēreni paaugstināts.
- Rentgena starojums: audzējam nav skaidru kontūru un “antenu”, un sākotnējos posmos tā ēna ir slikti definēta.
Šie ir galvenie atšķirību punkti starp vienu slimību un citu, pēc kuriem ārstējošais ārsts var aizdomas par vēža rašanos vai, gluži pretēji, pneimoniju uz tā fona. Bet ir slimības, kurām ir vēl mazāk specifisku atšķirību, kuru galvenais robežpunkts var būt tik nenozīmīga pazīme kā pacienta dzimums un vecums, vai arī tas, vai viņš pēc dažiem statistikas datiem pieder pie vairākuma.

Pneimonija un tuberkuloze
Bakteriālajai pneimonijai un tuberkulozei arī ir līdzīgas izpausmes, jo tās abas ir plaušu audu bakteriāla infekcija. Viņiem ir pat vairāk kopīga nekā ar onkoloģiju, un arī tuberkuloze var provocēt pneimonijas kaudzi, ja Koha baciļiem uz to novājinātajiem audiem pievienojas kāds cits patogēns.
Kā saprast, ka jums nav pneimonija, bet tuberkuloze:
- Biežākais pacienta vecums: nav.
- Visbiežāk sastopamais pacienta dzimums: vīrietis.
- Kā slimība sākas: akūta ar klepu, drudzi un nelielu simptomu skaitu.
- Klepus apraksts: sauss, vairāk kā klepus.
- Elpas trūkuma apraksts: ar smagu plaušu iekšējo audu bojājumu.
- Kā notiek hemoptīze: ļoti bieži un jo progresīvāka stadija, jo spēcīgāka.
- Sāpju krūtīs raksturojums: nav vai ļoti reti.
- Intoksikācijas smagums: smaga un pastāvīgi progresējoša.
- Fiziskie dati: nav vai ir nelielas izmaiņas elpošanā.
- Reakcija uz antibiotikām: praktiski nav. Tikai 5% pacientu jūt atvieglojumu, saglabājot rentgena attēlu.
- Laboratorijas izmeklējumu rezultāti: leikocīti un ESR paliek normāli.
- Rentgena starojums: izmaiņas visbiežāk veidojas augšējās daivās, tām ir skaidras kontūras un tās var atrasties pēdu veidā no plaušu saknes vai slimības sākotnējās zonas.

Pneimonija un bronhīts
Pneimonija un progresējošais bronhīts patiešām ir ļoti līdzīgas savās ārējās izpausmēs un pacienta sajūtās, turklāt, ja infekcija izplatās no bronhiem uz alveolām, tad viena slimība tiks pārklasificēta par citu.
Bērniem ir diezgan spēcīga tendence uz šādu slimības deģenerāciju, un provizorisku pneimonijas diferenciāldiagnozi bez instrumentālas izpētes, kas agrīnā stadijā nav pārāk efektīva, var veikt, pamatojoties uz noteiktām pazīmēm: visspilgtākais simptomu modelis: vēl augstāka temperatūra, stāvokļa pasliktināšanās, klepus, krēpu parādīšanās, strutainas gļotas utt.
Pneimonija un plaušu abscess
Plaušu abscess, gluži pretēji, ir pneimonijas sekas un smagāka tās izpausmes forma, kad plaušu audos parādās strutaini dobumi ar atrofētiem audiem. Uz pneimonijas simptomu fona var pazust abscesa veidošanās simptomi, kā arī rentgenā uz vispārēja iekaisuma fona var nebūt redzami, un, izlaižot garām tik svarīgu punktu, ārsts var pat zaudēt pacientu.

Abscess var izpausties kā samazināta elpošana, ārkārtēja intoksikācija, vēl lielāks temperatūras lēciens, kā arī pastiprinātas sāpes skartajā zonā. Pēc abscesa plīsuma pastāv liela sepses vai pleirīta attīstības iespējamība, taču pēc tam pacienta stāvoklis īslaicīgi nedaudz uzlabojas.
Pneimonija un plaušu embolija
PPA ir plaušu embolija, tās fona simptomi var līdzināties pneimonijai, bet tās laikā papildus galvenajiem plaušu audu nospiešanas simptomiem parādās smags elpas trūkums, cianoze (nasolabiālā trīsstūra un audu bālums vai zilums), tahikardija ( paaugstināts sirdsdarbības ātrums), spiediena kritums vairāk nekā 20% no parastā līmeņa.
Pneimonijas vai plaušu embolijas diagnostika balstās uz rūpīgāku izmeklējumu un pacienta iepriekšējo slimību izpēti. Plaušu embolijas gadījumā pneimonija var attīstīties uz vispārēja ķermeņa vājuma un jo īpaši plaušu audu nomākšanas fona. Un plaušu embolija var būt gan operāciju, gan hormonālo zāļu lietošanas sekas, gan ilgstoša gultas režīma rezultāts.

Pneimonija un pleirīts
Pleirīts var būt vai nu pneimonijas sekas, vai neatkarīga slimība un pat tās cēlonis.
Pleirītu ar parastajām metodēm redzēt ir gandrīz neiespējami, un simptomu praktiski nav, bet plaušu rentgenā ir redzami bojājumi, kas ik pa laikam maina atrašanās vietu, kas ar pneimoniju netiek novērots.
Diferenciāldiagnoze ir lieliska metode, kas ļauj gan diagnosticēt pneimoniju agrīnās stadijās, gan identificēt slēptākās kaites. Tomēr no diagnostikas speciālista tas prasa lielu pieredzi vai vismaz viņa plašo zināšanu bāzi un rūpīgu uzmanību uz šķietami nenozīmīgākajām detaļām, kas var likt galīgo, bet pacientam tik svarīgo punktu izmeklējumā.
Dažādas izcelsmes plaušu slimībām ir līdzīgi simptomi. Mikrobioloģisko pētījumu un rentgenu veikšana prasa laiku, kura gan ārstam, gan pacientam diemžēl ir ļoti maz. Apstākļos, kad nepieciešams ātri, pareizi pieņemt lēmumu, priekšplānā izvirzās ārsta spēja noteikt slimības cēloni, pamatojoties uz klīniskajiem un anamnēzes datiem. Šim nolūkam ir izstrādātas diferenciāldiagnostikas metodes.
Pirmkārt, pneimonija tiek atšķirta no:
- tuberkuloze;
- plaušu embolija (PE);
- audzēju bojājumi;
- alerģiskas reakcijas pret zālēm;
- psitakoze;
- alerģisks pneimonīts;
- sarkoidoze;
- kolagenoze.
Veselības aprūpes darbinieks sāk ar pacienta izmeklēšanu un aptauju ar apkārtējiem. Mērķis ir noskaidrot fonu, uz kura slimība attīstījās. Tiek konstatēta blakusslimību (vēzis, tuberkuloze, cukura diabēts, HIV, ārstēšana ar glikokortikosteroīdiem vai citostatiskiem līdzekļiem) klātbūtne, tiek novērtēti dzīves apstākļi, tiek apzināti kontakti ar slimiem cilvēkiem un dzīvniekiem.
Nākamajā posmā ārsts salīdzina saņemto informāciju par ķermeņa temperatūru, drebuļiem, galvassāpēm, apziņas traucējumiem, klepus raksturu, elpas trūkumu, paātrinātu elpošanu, sāpēm, krēpu veidu. Veicot pneimonijas diferenciāldiagnozi, ir svarīgi ņemt vērā pacienta vecumu.
Primārā diagnoze un ārstēšanas recepte ir balstīta uz izmeklējuma rezultātiem, un tikai pēc asins un krēpu analīzes un rentgena izmeklēšanas terapeits izdara galīgo slēdzienu.
Atšķirības starp iekaisumu un citām plaušu slimībām
- Pneimonijas un tuberkulozes diferenciāldiagnoze
Dažu tuberkulozes formu gaita sākotnējā stadijā ir ļoti līdzīga bakteriālās pneimonijas klīniskajam attēlam. Tomēr jāatceras, ka tuberkulozes sākums ir gandrīz asimptomātisks. Pacienti sūdzas par nogurumu, nelielu savārgumu (intoksikācijas rezultātā), klepu un svīšanu. Šajā posmā rentgena izmeklēšana parāda plaušu bojājumus. Pieredzējuši ārsti saka: "Tuberkuloze ir vairāk redzama nekā dzirdēta."
Bakteriālajai pneimonijai raksturīgs izteikts sākums ar drebuļiem un drudzi virs 38,5 grādiem. Šāda pacienta āda ir sausa un karsta, un svīšana tiek novērota tikai krīzes brīžos. Krēpas pneimonijas gadījumā ir ar gaisa burbuļiem, viskozākas nekā tuberkulozes gadījumā.
Tuberkuloze uz rentgena parādās skaidru apaļu polimorfu perēkļu veidā, parasti augšējā daivā. Pneimonijas asins analīze atklāj izteiktu leikocitozi, bet tuberkulozei - limfopēniju un mērenu leikocitozi. Krēpu mikrobioloģiskā izmeklēšana atklāj Mycobacterium tuberculosis.
Tikai 5% tuberkulozes pacientu gūst labumu no ārstēšanas ar plaša spektra antibiotikām. Tāpēc, ja pneimonijas simptomi cilvēkam ilgst vairāk nekā 2 nedēļas, tad diagnoze ir jāprecizē. Visticamāk, tā ir tuberkuloze. Tomēr pneimonijas empīriskajā ārstēšanā nav ieteicams izrakstīt plaša spektra prettuberkulozes zāles.
- Pneimonijas un plaušu vēža diferenciāldiagnoze
Klepus, krēpas, sāpes un hemoptīze var pavadīt metastāžu augšanu pleirā. Līdz šim brīdim plaušu vēzis ir asimptomātisks, bet to var noteikt ar rentgena palīdzību. Šajā gadījumā perifērais vēzis visbiežāk atrodas plaušu priekšējās augšējās daivas, tā kontūras ir starojošas.
Vēža šūnas var pāraugt citos orgānos vai parādīties plaušās kā metastāzes. Sīkāku informāciju par atšķirībām starp akūtu pneimoniju, tuberkulozi un plaušu vēzi skatiet 1. tabulā.
1. tabula. Pneimonijas un tuberkulozes diferenciāldiagnoze.
| Pierakstīties | Fokālā pneimonija | Perifēro plaušu vēzis | Tuberkuloze |
|---|---|---|---|
| Vecums | Jebkurā vecumā, bet biežāk cilvēkiem līdz 50 gadu vecumam | Biežāk cilvēkiem, kas vecāki par 50 gadiem | Jebkurš vecums |
| Stāvs | Vienlīdz bieži vīriešiem un sievietēm | Biežāk smēķētājiem vīriešiem | Biežāk vīriešiem |
| Slimības sākums | Parasti akūta ar drudzi | Var būt nepamanāms vai ar paaugstinātu temperatūru | Akūts, subakūts ar dažiem simptomiem |
| Klepus | Sākumā var nebūt | Bieži prombūtnē | Sausa vai klepus |
| Aizdusa | Ar lielu plaušu audu bojājumu | Var pietrūkt | Ar plašu plaušu audu bojājumu |
| Hemoptīze | Reti | Reti | Bieži |
| Sāpes krūtīs | Rodas, ja ir iesaistīta pleira | Iespējams | Biežāk prombūtnē |
| Reibums | Nav izteikts | Bieži neizpauž | Izteikts, nepārtraukti progresē |
| Fiziskie dati | Izteikts: mainās elpošanas modelis un parādās mitras rales | Trūcīgi vai nav | Trūcīgi vai nav |
| Laboratorijas dati | Leikocitoze, ESR palielināšanās, kas samazinās pēc pneimonijas izzušanas | Mērens ESR pieaugums ar normālu leikocītu skaitu | Parasti ESR un balto asins šūnu skaits nemainās |
| Rentgena dati | Asi izteikta, biežāk tiek skartas apakšējās daivas, fokālās ēnas ir viendabīgas, robežas ir izplūdušas, palielināts plaušu modelis, palielinātas plaušu saknes | Sākotnēji audzēja ēna ir zemas intensitātes ar neskaidrām kontūrām un “antenām” | Lokalizācija bieži ir augšējā daivā, bojājumi ir polimorfi, dažāda vecuma ar skaidrām kontūrām, var būt “ceļš” uz sakni un piesārņojuma perēkļiem. |
| Antibiotiku iedarbība | Izteikta, apgrieztā procesa attīstība pēc 9-12 dienām | Nav vai kļūdaini pozitīva dinamika, bet izmaiņas rentgena izmeklēšanas laikā saglabājas | Nav klāt; Rentgena izmaiņas saglabājas ilgu laiku |
Pneimonijas un plaušu embolijas (PE) diferenciāldiagnoze Ilgstošs gultas režīms pēc operācijas, augšstilba kaula kakliņa lūzumi un priekškambaru fibrilācija var izraisīt apakšējo ekstremitāšu tromboflebītu. Sekas bieži ir plaušu trombembolija. Jaunām sievietēm šī problēma dažkārt rodas pēc perorālo kontracepcijas līdzekļu lietošanas.
TE raksturīgās iezīmes papildus fonam ir:
- cianoze;
- elpas trūkums;
- arteriālā hipotensija;
- tahikardija.
Klausoties, ārsts konstatē pleiras berzes troksni un pavājinātu elpošanu. Rentgena starojums parāda trīsstūrveida ēnu, un radioizotopu perfūzijas skenēšana parāda išēmiskas “aukstās” zonas. Šajā gadījumā ir akūta sirds labās puses pārslodze.
- Pneimonijas un eozinofīlā infiltrāta diferenciāldiagnoze
Ārstējot ar glikokortikosteroīdiem, infiltrāti pazūd pēc 10 dienām.
Esošās pneimonijas raksturs norāda uz tās avotu. Pneimokoku akūtu pneimoniju pavada drebuļi, augsts drudzis un galvassāpes. Ja baktērijas nonāk asinsritē, drebuļi var būt smagi, īpaši bērniem. Šī reakcija nav raksturīga vecākiem cilvēkiem.
Plaušu bakteriālajai infekcijai elpojot ir raksturīgas dedzinošas sāpes krūtīs. Ar vīrusu un mikoplazmas infekcijām šie simptomi netiek novēroti, bet galvassāpes ir smagas un ir iespējami izsitumi.
Krēpu raksturs:
- bakteriāla pneimonija – mukopurulenta, bieza;
- vīrusu un mikoplazmas – neliels daudzums;
- plaušu abscess - strutaina smaka;
- plaušu tūska – bagātīga, putojoša, rozā;
- lobāra pneimonija - sarūsējusi;
- bronhoalveolārais vēzis – siekalu;
- bronhektāzes - bagātīgas, strutainas, ar asinīm.
Baktēriju pneimoniju var pavadīt aknu bojājumi, paaugstināta aknu enzīmu aktivitāte un paaugstināts urīnvielas līmenis asinīs.
Asins analīzē galvenais plaušu infekcijas veida rādītājs ir balto asins šūnu līmenis. Leikocitoze izpaužas pneimonijas bakteriālajās formās (vairāk nekā 15×10 9 /l), mikoplazmas un vīrusu formās indikators paliek gandrīz nemainīgs.
Bērniem
Lai precīzi diagnosticētu bērna plaušu slimību, ir izstrādātas vairākas metodes. Visos no tiem tiek ņemtas vērā pacientu vecuma īpašības, pneimonijas etioloģija, tās attīstību veicinošie faktori un slimības formas (patoģenēze).
Bērna ķermeņa anatomiskās un fizioloģiskās īpašības nosaka tendenci agrīnā vecumā attīstīt pneimoniju, iespēju pāriet hroniskā formā un tās gaitas smagumu. Tikpat svarīgu lomu pneimonijas attīstībā spēlē:
- hipotermija;
- slikta bērnu aprūpe;
- higiēnas noteikumu pārkāpšana;
- mākslīgā barošana;
- antisanitāri dzīves apstākļi, t.sk. mitras telpas;
- iepriekšējās infekcijas slimības.
Visticamākie sabiedrībā iegūtās pneimonijas patogēni bērniem līdz 6 mēnešu vecumam ir vīrusi, stafilokoki un gramnegatīvā flora. Vēlāk - pneimokoku un B tipa H. influenzae. Pusaudža gados pievieno streptokoku. Nozokomiālās infekcijas gadījumā infekcijas avots gan pieaugušajiem, gan bērniem, visticamāk, būs Enterobacteriaceae, Escherichia coli, Staphylococcus, Proteus un Pseudomonas.
Bērnu pneimonijas diferenciāldiagnoze ietver vairākus patoloģiju klasifikācijas veidus:
- Pēc veida tie izšķir fokālo, segmentālo, lobāro un intersticiālo akūtu.
- Pēc lokalizācijas - plaušu daivā, segmentā, vienpusējs un divpusējs.
- Pēc veida: sabiedrībā iegūts un slimnīcā iegūts, perinatāls, ar ventilatoru saistīts, aspirācija, imūndeficīts.
- Pēc smaguma pakāpes: viegla, vidēji smaga un smaga ar komplikācijām. Šajā gadījumā komplikācijas tiek iedalītas plaušu (pleirīts, pneimotorakss) un ekstrapulmonārās (sirds un asinsvadu mazspēja, infekciozi toksisks šoks, diseminētas intravaskulāras koagulācijas sindroms, respiratorā distresa sindroms).
Ar visu veidu pneimoniju bērniem procesā tiek iesaistīti visi orgāna strukturālie elementi, apgrūtinās gāzu apmaiņa, palielinās elpošanas ātrums, samazinās plaušu ventilācija, kad ir ārkārtīgi nepieciešama skābekļa nepieciešamība. Patoloģija var ietekmēt sirdi, kas ir spiesta kompensēt skābekļa trūkumu ar palielinātu kontrakciju intensitāti, kam seko sirds muskuļa distrofija.
Skābekļa trūkums izraisa vielmaiņas traucējumus un asins paskābināšanos. Tālāk tiek novērota hipoksēmija un hipoksija. Skābekļa absorbcijas pārtraukšana ārēji izpaužas zilganā sejas izskatā (hipoksēmija) vai zemes pelēkā krāsā (hipoksija). Sekojoši dziļi vielmaiņas traucējumi var kļūt neatgriezeniski un izraisīt nāvi.
Akūtas pneimonijas diagnosticēšanas kritēriji bērniem ir:
- Plaušu auskultācija atklāj paātrinātu elpošanu un sirdsdarbības ātruma palielināšanos apnojas, stenīgas elpošanas, burbuļu sēkšanas un bronhofonijas fona apstākļos.
- Temperatūras paaugstināšanās par vairāk nekā 38 grādiem vismaz 3 dienas.
- Sauss klepus, elpošanas mazspēja, balss trīce.
- Uz rentgena stariem ir ēnas bojājumu un tumšuma veidā.
- Asins analīze parāda leikocitozi, urīnu un izkārnījumus bez patoloģiskām novirzēm.
Elpošanas mazspējas pazīmes var atrast 2. tabulā.
2. tabula. Elpošanas mazspējas klīniskās un laboratoriskās īpašības bērniem ar akūtu pneimoniju (Saskaņā ar A.F. Tour, A.F. Tarasov, N.P. Shabalov, 1985).
| DN grāds | Klīniskās īpašības | Ārējās elpošanas indikatori | Asins gāzu sastāvs, skābju-bāzes stāvoklis (ABS) |
|---|---|---|---|
| es | Miera stāvoklī elpas trūkuma nav. Periorālā cianoze, periodiska, pasliktinās ar trauksmi. Sejas bālums, asinsspiediens normāls, retāk – mēreni paaugstināts. Ps:RR = 3,5-2,5:1, tahikardija. Uzvedība nemainīga, dažreiz nemierīga | MVR (elpas minūtes tilpums) palielinās, RD (elpošanas rezerve) samazinās. Vital kapacitāte (plaušu vitālā kapacitāte), DE (elpošanas ekvivalents) palielināts OD (elpošanas tilpums) nedaudz samazināts | Asins gāzu sastāvs miera stāvoklī ir nemainīgs vai mēreni samazināts asins piesātinājums ar skābekli (par 10%; pO2 = 8,67-10,00 kPa, bet elpojot skābekli tas tuvojas normai. Hiperkapnija (PCO2 ir augstāka par 4,67 kPa vai PCO2 ir norma). CBS dabiskas izmaiņas nenotiek Oglekļa dioksīda satura palielināšanās asinīs. |
| II | Elpas trūkums miera stāvoklī, elpošana ar palīgmuskuļu piedalīšanos, starpribu telpu un suprasternālās bedres ievilkšana. Ps: RR = 2-1,5:1, tahikardija. Ekstremitāšu periorālā cianoze, pastāvīga, nepazūd, elpojot skābekli, bet skābekļa teltī nav. Ģeneralizēts nagu pamatnes bālums. BP ir paaugstināts. Uzvedība: letarģija, adinamija, samazināts muskuļu tonuss. | MOD palielinājās. Vital kapacitāte ir samazināta par vairāk nekā 25-30%. RD un OD samazināts līdz 50% vai mazāk. DE ir ievērojami palielināts, kas liecina par izteiktu skābekļa izmantošanas samazināšanos plaušās. | Asins skābekļa piesātinājums ir 70-85% (pO2 = 7,33-8,53 kPa. Hiperkapnija (PCO2 augstāka par 6,0 kPa; asiņu pH - 7,34-7,25 (acidoze); bāzes deficīts (BE)). Plazmas bikarbonātu līmeni nosaka acidozes raksturs.ABC ir atkarīgs no hemodinamikas stāvokļa |
| III | Aizdusa ir smaga (elpošanas ātrums ir vairāk nekā 150% no normas), neregulāra elpošana, periodiski bradipnoja, paradoksāla elpošana. Elpas skaņu samazināšanās vai iztrūkums iedvesmas laikā, pazeminās asinsspiediens. Ģeneralizēta cianoze. Ieelpojot skābekli, lūpu un gļotādu cianoze nepazūd. Vispārējs bālums, marmorējums. Uzvedība: letarģija, nomākta apziņa, samazināts skeleta muskuļu tonuss, koma, krampji. | MOD samazināts, VC un OD samazināts par vairāk nekā 50%, RD = 0 | Asins skābekļa piesātinājums - mazāks par 70% (pO2 zem 5,33 kPa; dekompensēta acidoze (pH mazāka par 7,2). BE lielāka par 6-8; hiperkapnija (PCO2, vairāk nekā 9,87 kPa), samazināts bikarbonātu un bufera līmenis bāzes (BE) |