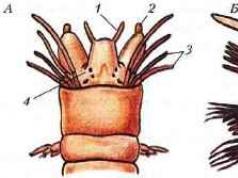
البروتون هو جسيم مستقر من فئة الهادرونات، نواة ذرة الهيدروجين.
من الصعب تحديد الحدث الذي يجب اعتباره اكتشاف البروتون: فهو معروف منذ زمن طويل كأيون الهيدروجين. إنشاء نموذج كوكبي للذرة بواسطة إ. رذرفورد (1911)، واكتشاف النظائر (ف. سودي، ج. طومسون، ف. أستون، 1906-1919)، ومراقبة نوى الهيدروجين التي تم إخراجها من النوى بواسطة لعبت جسيمات ألفا دورًا في اكتشاف نيتروجين البروتون (E. Rutherford, 1919). في عام 1925، تلقى ب. بلاكيت الصور الأولى لآثار البروتون في غرفة السحاب (انظر أجهزة الكشف عن الإشعاع النووي)، مما يؤكد اكتشاف التحول الاصطناعي للعناصر. في هذه التجارب، تم التقاط جسيم بيتا بواسطة نواة النيتروجين، التي أصدرت بروتونًا وتحولت إلى نظير أكسجين.
تشكل البروتونات مع النيوترونات النوى الذرية للجميع العناصر الكيميائيةوعدد البروتونات في النواة يحدد العدد الذري لعنصر معين. يمتلك البروتون شحنة كهربائية موجبة تساوي الشحنة الأولية، أي القيمة المطلقة لشحنة الإلكترون. وقد تم اختبار ذلك تجريبياً بدقة 10-21. كتلة البروتون mp = (938.2796 ± 0.0027) MeV أو ~ 1.6-10-24 جم، أي أن البروتون أثقل من الإلكترون بـ 1836 مرة! مع نقطة حديثةمن وجهة نظر ما، البروتون ليس جسيمًا أوليًا حقيقيًا: فهو يتكون من كواركين u بشحنة كهربائية +2/3 (بوحدات الشحنة الأولية) وكوارك d بشحنة كهربائية -1/3. ترتبط الكواركات ببعضها البعض من خلال تبادل الجسيمات الافتراضية الأخرى - الجلونات، وكمات المجال الذي يحمل تفاعلات قوية. تشير البيانات المستمدة من التجارب التي تم فيها النظر في عمليات تشتت الإلكترون على البروتونات بالفعل إلى وجود مراكز تشتت نقطية داخل البروتونات. وهذه التجارب تشبه إلى حد ما تجارب رذرفورد التي أدت إلى اكتشاف النواة الذرية. نظرًا لكونه جسيمًا مركبًا، فإن حجم البروتون محدود يصل إلى 10-13 سم تقريبًا، على الرغم من أنه لا يمكن تمثيله ككرة صلبة بالطبع. إن البروتون يشبه سحابة ذات حدود غامضة، تتألف من جسيمات افتراضية مخلوقة ومفنية. ويشارك البروتون، مثله كمثل كل الهادرونات، في كل من التفاعلات الأساسية. لذا. التفاعلات القوية تربط البروتونات والنيوترونات في النوى، والتفاعلات الكهرومغناطيسية تربط البروتونات والإلكترونات في الذرات. من أمثلة التفاعلات الضعيفة اضمحلال بيتا للنيوترون أو التحول النووي للبروتون إلى نيوترون مع انبعاث البوزيترون والنيوترينو (بالنسبة للبروتون الحر، فإن مثل هذه العملية مستحيلة بسبب قانون حفظ وتحويل الطاقة، لأن النيوترون له كتلة أكبر قليلاً). دوران البروتون هو 1/2. تسمى الهادرونات ذات الدوران نصف الصحيح بالباريونات (من الكلمة اليونانية التي تعني "ثقيل"). تشمل الباريونات البروتون والنيوترون ومختلف الهايبرونات (؟،؟،؟،؟) وعدد من الجسيمات ذات الأعداد الكمومية الجديدة، ومعظمها لم يتم اكتشافه بعد. لتوصيف الباريونات تم تقديمه رقم خاص-- شحنة الباريون، تساوي 1 للباريونات، - 1 -- للباريونات المضادة و O -- لجميع الجسيمات الأخرى. شحنة الباريون ليست مصدرًا لحقل الباريون، بل تم تقديمها فقط لوصف الأنماط الملحوظة في التفاعلات مع الجسيمات. يتم التعبير عن هذه الأنماط في شكل قانون حفظ شحنة الباريون: يتم الحفاظ على الفرق بين عدد الباريونات والباريونات المضادة في النظام في أي تفاعل. إن الحفاظ على شحنة الباريون يجعل من المستحيل على البروتون أن يتحلل، لأنه أخف الباريونات. وهذا القانون تجريبي بطبيعته، وبالطبع يجب اختباره تجريبيا. وتتميز دقة قانون حفظ شحنة الباريون بثبات البروتون، الذي يعطي التقدير التجريبي لعمره قيمة لا تقل عن 1032 سنة.
وفي الوقت نفسه، تتنبأ النظريات التي تجمع بين جميع أنواع التفاعلات الأساسية بالعمليات التي تؤدي إلى تعطيل شحنة الباريون واضمحلال البروتون. لم يتم تحديد عمر البروتون في مثل هذه النظريات بدقة شديدة: حوالي 1032 ± 2 سنة. هذه المرة هائلة، وهي أطول بعدة مرات من وجود الكون (~ 2*1010 سنة). ولذلك فإن البروتون مستقر عمليا، مما جعل تكوين العناصر الكيميائية وظهور الحياة الذكية في نهاية المطاف أمرا ممكنا. ومع ذلك، فإن البحث عن اضمحلال البروتون يمثل الآن أحد أهم الاكتشافات أهم المهامالفيزياء التجريبية. مع عمر بروتون يبلغ ~ 1032 عامًا في حجم ماء يبلغ 100 متر مكعب (يحتوي 1 متر مكعب على ~ 1030 بروتونًا)، ينبغي توقع اضمحلال بروتون واحد سنويًا. كل ما تبقى هو تسجيل هذا الاضمحلال. سيكون اكتشاف اضمحلال البروتون خطوة مهمة نحو الفهم الصحيح لوحدة قوى الطبيعة.
النيوترون هو جسيم محايد ينتمي إلى فئة الهادرونات. اكتشفه الفيزيائي الإنجليزي ج. تشادويك عام 1932. جنبا إلى جنب مع البروتونات، والنيوترونات هي جزء من النوى الذرية. الشحنة الكهربائية للنيوترون qn هي صفر. يتم تأكيد ذلك من خلال القياسات المباشرة للشحنة من انحراف شعاع النيوترونات بقوة المجالات الكهربائيةمما أظهر أن |qn|<10-20e (здесь е -- элементарный электрический заряд, т. е. абсолютная величина заряда электрона). Косвенные данные дают оценку |qn|< 2?10-22 е. Спин нейтрона равен 1/2. Как адрон с полуцелым спином, он относится к группе барионов. У каждого бариона есть античастица; антинейтрон был открыт в 1956 г. в опытах по рассеянию антипротонов на ядрах. Антинейтрон отличается от нейтрона знаком барионного заряда; у нейтрона, как и у протона, барионный заряд равен +1.Как и протон и прочие адроны, нейтрон не является истинно элементарной частицей: он состоит из одного u-кварка с электрическим зарядом +2/3 и двух d-кварков с зарядом - 1/3, связанных между собой глюонным полем.
النيوترونات مستقرة فقط في النوى الذرية المستقرة. النيوترون الحر هو جسيم غير مستقر يضمحل إلى بروتون (p) وإلكترون (e-) وإلكترون مضاد النيوترينو. ويبلغ عمر النيوترون (917–14) ثانية، أي حوالي 15 دقيقة. وفي المادة، توجد النيوترونات في شكل حر بدرجة أقل بسبب امتصاصها القوي بواسطة النوى. ولذلك فهي تحدث في الطبيعة أو يتم إنتاجها في المختبر فقط نتيجة للتفاعلات النووية.
بناءً على توازن الطاقة في التفاعلات النووية المختلفة، تم تحديد الفرق بين كتلتي النيوترون والبروتون: mn-mp(1.29344 ±0.00007) MeV. وبمقارنتها بكتلة البروتون، نحصل على كتلة النيوترون: mn = 939.5731 ± 0.0027 MeV؛ وهذا يتوافق مع mn ~ 1.6-10-24، ويشارك النيوترون في جميع أنواع التفاعلات الأساسية. التفاعلات القوية تربط النيوترونات والبروتونات في النوى الذرية. مثال على التفاعل الضعيف هو اضمحلال بيتا للنيوترون.
هل يشارك هذا الجسيم المحايد في التفاعلات الكهرومغناطيسية؟ للنيوترون بنية داخلية، ومع الحياد العام توجد فيه تيارات كهربائية تؤدي بشكل خاص إلى ظهور عزم مغناطيسي في النيوترون. بمعنى آخر، في المجال المغناطيسي، يتصرف النيوترون مثل إبرة البوصلة. وهذا مجرد مثال واحد على التفاعل الكهرومغناطيسي. وقد حظي البحث عن عزم ثنائي القطب الكهربائي للنيوترون، والذي تم الحصول على حد أعلى له، باهتمام كبير. هنا، تم إجراء التجارب الأكثر فعالية من قبل علماء من معهد لينينغراد للفيزياء النووية التابع لأكاديمية العلوم في اتحاد الجمهوريات الاشتراكية السوفياتية؛ يعد البحث عن عزم ثنائي القطب النيوتروني أمرًا مهمًا لفهم آليات انتهاك الثبات في ظل انعكاس الزمن في العمليات الدقيقة.
وقد لوحظت تفاعلات الجاذبية للنيوترونات مباشرة من وقوعها في مجال الجاذبية الأرضية.
أصبح التصنيف التقليدي للنيوترونات وفقًا لطاقتها الحركية مقبولًا الآن:
النيوترونات البطيئة (<105эВ, есть много их разновидностей),
النيوترونات السريعة (105؟108 إلكترون فولت)، عالية الطاقة (> 108 إلكترون فولت).
النيوترونات البطيئة جدًا (10-7 إلكترون فولت)، والتي تسمى النيوترونات فائقة البرودة، لها خصائص مثيرة جدًا للاهتمام. اتضح أنه يمكن تجميع النيوترونات فائقة البرودة في "فخاخ مغناطيسية" ويمكن توجيه دورانها في اتجاه معين هناك. باستخدام مجالات مغناطيسية ذات تكوين خاص، يتم عزل النيوترونات فائقة البرودة عن الجدران الماصة ويمكنها "العيش" في المصيدة حتى تتحلل. وهذا يسمح بإجراء العديد من التجارب الدقيقة لدراسة خصائص النيوترونات. هناك طريقة أخرى لتخزين النيوترونات فائقة البرودة تعتمد على خصائصها الموجية. يمكن ببساطة تخزين مثل هذه النيوترونات في "جرة" مغلقة. وقد عبر عن هذه الفكرة الفيزيائي السوفييتي يا. بي. زيلدوفيتش في أواخر الخمسينيات من القرن العشرين، وتم الحصول على النتائج الأولى في دوبنا في معهد الأبحاث النووية بعد عقد من الزمان تقريبًا.
تمكن العلماء مؤخرًا من بناء وعاء تعيش فيه النيوترونات فائقة البرودة حتى اضمحلالها الطبيعي.
النيوترونات الحرة قادرة على التفاعل بنشاط مع النوى الذرية، مما يسبب التفاعلات النووية. نتيجة لتفاعل النيوترونات البطيئة مع المادة، يمكن ملاحظة تأثيرات الرنين، وتشتت الحيود في البلورات، وما إلى ذلك. وبسبب هذه الخصائص، تستخدم النيوترونات على نطاق واسع في الفيزياء النووية وفيزياء الحالة الصلبة. وهي تلعب دورًا مهمًا في الطاقة النووية، وفي إنتاج عناصر ما بعد اليورانيوم والنظائر المشعة، وتجد تطبيقًا عمليًا في التحليل الكيميائي والاستكشاف الجيولوجي.
§1. تعرف على الإلكترون والبروتون والنيوترون
الذرات هي أصغر جزيئات المادة.
إذا قمت بتكبير تفاحة متوسطة الحجم إلى حجم الأرض، فإن الذرات ستصبح بحجم تفاحة فقط. وعلى الرغم من هذه الأبعاد الصغيرة، تتكون الذرة من جسيمات فيزيائية أصغر.
يجب أن تكون على دراية ببنية الذرة من خلال دورة الفيزياء في مدرستك. ومع ذلك، دعونا نتذكر أن الذرة تحتوي على نواة وإلكترونات تدور حول النواة بسرعة كبيرة بحيث لا يمكن تمييزها - فهي تشكل "سحابة إلكترونية"، أو الغلاف الإلكتروني للذرة.
الإلكتروناتيشار إليها عادة على النحو التالي: ه − . الإلكترونات ه- خفيفة جدًا، وانعدام الوزن تقريبًا، لكنها موجودة سلبيالشحنة الكهربائية. وهو يساوي −1. التيار الكهربائي الذي نستخدمه جميعًا هو عبارة عن تيار من الإلكترونات التي تعمل في الأسلاك.
النواة الذرية، حيث تتركز كل كتلتها تقريبًا، وتتكون من جزيئات من نوعين - النيوترونات والبروتونات.
النيوتروناتيشار إليها على النحو التالي: ن 0
، أ البروتوناتلذا: ص +
.
من حيث الكتلة، فإن النيوترونات والبروتونات متماثلة تقريبًا - 1.67510−24 جم و1.67310−24 جم.
صحيح أنه من غير الملائم جدًا حساب كتلة هذه الجزيئات الصغيرة بالجرام، لذلك يتم التعبير عنها بالجرام وحدات الكربون، كل منها يساوي 1.673 10 −24 جم.
لكل جسيم نحصل عليه الكتلة الذرية النسبية، يساوي حاصل قسمة كتلة الذرة (بالجرام) على كتلة وحدة الكربون. الكتل الذرية النسبية للبروتون والنيوترون تساوي 1، لكن شحنة البروتونات موجبة وتساوي +1، بينما النيوترونات ليس لها شحنة.
. الألغاز حول الذرة
يمكن تجميع الذرة "في العقل" من جزيئات، مثل لعبة أو سيارة من أجزاء مجموعة بناء للأطفال. من الضروري فقط مراعاة شرطين مهمين.
- الشرط الأول: كل نوع من الذرة له خاصته مجموعة خاصة"تفاصيل" - الجسيمات الأولية. على سبيل المثال، من المؤكد أن ذرة الهيدروجين سيكون لها نواة ذات شحنة موجبة قدرها +1، مما يعني أنها يجب أن تحتوي بالتأكيد على بروتون واحد (وليس أكثر).
يمكن أن تحتوي ذرة الهيدروجين أيضًا على نيوترونات. المزيد عن هذا في الفقرة التالية.
سيكون لذرة الأكسجين (العدد الذري في الجدول الدوري 8) نواة مشحونة ثمانيةشحنات موجبة (+8)، مما يعني أن هناك ثمانية بروتونات. وبما أن كتلة ذرة الأكسجين تساوي 16 وحدة نسبية، فلكي نحصل على نواة الأكسجين، نضيف 8 نيوترونات أخرى. - الشرط الثانيهو أن كل ذرة ينبغي أن يكون محايد كهربائيا. وللقيام بذلك، يجب أن يكون لديها ما يكفي من الإلكترونات لموازنة شحنة النواة. بعبارة أخرى، عدد الإلكترونات في الذرة يساوي عدد البروتوناتفي جوهرها، وكذلك الرقم التسلسلي لهذا العنصر في الجدول الدوري.
كما ذكرنا سابقًا، تتكون الذرة من ثلاثة أنواع من الجسيمات الأولية: البروتونات والنيوترونات والإلكترونات. النواة الذرية هي الجزء المركزي للذرة، وتتكون من البروتونات والنيوترونات. البروتونات والنيوترونات لها الاسم الشائع نيوكليون، ويمكنها التحول إلى بعضها البعض في النواة. نواة أبسط ذرة - ذرة الهيدروجين - تتكون من جسيم أولي واحد - البروتون.
يبلغ قطر نواة الذرة حوالي 10-13 - 10-12 سم ويساوي 0.0001 من قطر الذرة. ومع ذلك، فإن كتلة الذرة بأكملها تقريبًا (99.95-99.98٪) تتركز في النواة. ولو أمكن الحصول على 1سم3 من المادة النووية النقية لكانت كتلتها 100-200 مليون طن. كتلة نواة الذرة أكبر بعدة آلاف المرات من كتلة جميع الإلكترونات التي تشكل الذرة.
بروتون- جسيم أولي، نواة ذرة الهيدروجين. تبلغ كتلة البروتون 1.6721 × 10-27 كجم، أي 1836 ضعف كتلة الإلكترون. الشحنة الكهربائية موجبة وتساوي 1.66×10-19 درجة مئوية. الكولوم هو وحدة شحنة كهربائية تساوي كمية الكهرباء التي تمر عبر المقطع العرضي للموصل في زمن 1 ثانية عند تيار ثابت قدره 1 أمبير (أمبير).
تحتوي كل ذرة من أي عنصر على عدد معين من البروتونات في النواة. هذا الرقم ثابت لعنصر معين ويحدد خواصه الفيزيائية والكيميائية. أي أن عدد البروتونات يحدد العنصر الكيميائي الذي نتعامل معه. على سبيل المثال، إذا كان هناك بروتون واحد في النواة، فهو الهيدروجين، وإذا كان هناك 26 بروتونًا، فهو الحديد. يحدد عدد البروتونات في النواة الذرية شحنة النواة (رقم الشحنة Z) والعدد الذري للعنصر في الجدول الدوري للعناصر D.I. مندليف (العدد الذري للعنصر).
نيوترون- جسيم متعادل كهربائيا كتلته 1.6749×10-27 كجم، أي 1839 ضعف كتلة الإلكترون. الخلية العصبية في الحالة الحرة هي جسيم غير مستقر، وتتحول بشكل مستقل إلى بروتون مع انبعاث إلكترون ومضاد النيوترينو. يبلغ عمر النصف للنيوترونات (الوقت الذي يتحلل فيه نصف العدد الأصلي للنيوترونات) حوالي 12 دقيقة. ومع ذلك، في حالة مرتبطة داخل نوى ذرية مستقرة، فهو مستقر. يُطلق على العدد الإجمالي للنيوكليونات (البروتونات والنيوترونات) في النواة العدد الكتلي (الكتلة الذرية - A). عدد النيوترونات الموجودة في النواة يساوي الفرق بين أرقام الكتلة والشحنة: N = A - Z.
الإلكترون- جسيم أولي، حامل أصغر كتلة - 0.91095x10-27 جم وأصغر شحنة كهربائية - 1.6021x10-19 درجة مئوية. هذا جسيم سالب الشحنة. عدد الإلكترونات في الذرة يساوي عدد البروتونات في النواة، أي. الذرة محايدة كهربائيا.
بوزيترون- جسيم أولي ذو شحنة كهربائية موجبة، وجسيم مضاد بالنسبة للإلكترون. كتلة الإلكترون والبوزيترون متساويان، والشحنتان الكهربائيتان متساويتان في القيمة المطلقة، ولكنهما متضادان في الإشارة.
تسمى الأنواع المختلفة من النوى النويدات. النويدة هي نوع من الذرة بأعداد معينة من البروتونات والنيوترونات. في الطبيعة توجد ذرات لنفس العنصر لها كتل ذرية مختلفة (الأعداد الكتلية):
، الكلور، الخ. تحتوي نوى هذه الذرات على نفس عدد البروتونات، لكن أعدادًا مختلفة من النيوترونات. تسمى أنواع ذرات العنصر نفسه التي لها نفس الشحنة النووية ولكن بأعداد كتلية مختلفة النظائر
. نظرًا لوجود نفس عدد البروتونات، ولكن مع اختلاف عدد النيوترونات، فإن النظائر لها نفس بنية الأغلفة الإلكترونية، أي. خصائص كيميائية متشابهة جدًا وتحتل نفس المكان في الجدول الدوري للعناصر الكيميائية.
يتم تحديدها بواسطة رمز العنصر الكيميائي المقابل مع وجود الفهرس A في أعلى اليسار - يتم أيضًا تحديد الرقم الكتلي، وأحيانًا عدد البروتونات (Z) في أسفل اليسار. على سبيل المثال، يتم تسمية النظائر المشعة للفوسفور بـ 32P، 33P، أو P وP، على التوالي. عند تعيين نظير دون الإشارة إلى رمز العنصر، يتم إعطاء العدد الكتلي بعد تسمية العنصر، على سبيل المثال، الفوسفور - 32، الفوسفور - 33.
تحتوي معظم العناصر الكيميائية على عدة نظائر. بالإضافة إلى نظير الهيدروجين 1H- البروتيوم، فإن الهيدروجين الثقيل 2H- الديوتيريوم والهيدروجين فائق الثقل 3H- التريتيوم معروفان. لليورانيوم 11 نظيرًا، ويوجد في المركبات الطبيعية ثلاثة (يورانيوم 238، يورانيوم 235، يورانيوم 233). لديهم 92 بروتونًا و146143 و141 نيوترونًا على التوالي.
حاليًا، هناك أكثر من 1900 نظيرًا لـ 108 عناصر كيميائية معروفة. ومن بين هذه النظائر الطبيعية، تشمل جميع النظائر المستقرة (حوالي 280 منها) والنظائر الطبيعية التي تشكل جزءًا من الفصائل المشعة (46 منها). يتم تصنيف الباقي على أنه اصطناعي ويتم الحصول عليه بشكل مصطنع نتيجة التفاعلات النووية المختلفة.
يجب استخدام مصطلح "النظائر" فقط عندما نتحدث عن ذرات العنصر نفسه، على سبيل المثال، الكربون 12C و14C. إذا كان المقصود ذرات عناصر كيميائية مختلفة، فمن المستحسن استخدام مصطلح "النويدات"، على سبيل المثال، النويدات المشعة 90Sr، 131J، 137Cs.
دعونا نتحدث عن كيفية العثور على البروتونات والنيوترونات والإلكترونات. هناك ثلاثة أنواع من الجسيمات الأولية في الذرة، ولكل منها شحنته الأولية وكتلته.
الهيكل الأساسي
لكي تفهم كيفية العثور على البروتونات والنيوترونات والإلكترونات، تخيل أنها الجزء الرئيسي من الذرة. يوجد داخل النواة بروتونات ونيوترونات تسمى نيوكليونات. داخل النواة، يمكن لهذه الجسيمات أن تتحول إلى بعضها البعض.
على سبيل المثال، للعثور على البروتونات والنيوترونات والإلكترونات في جهاز واحد، عليك معرفة رقمه التسلسلي. وإذا أخذنا في الاعتبار أن هذا العنصر هو الذي يتصدر الجدول الدوري، فإن نواته تحتوي على بروتون واحد.
ويبلغ قطر النواة الذرية عشرة آلاف من الحجم الكلي للذرة. أنه يحتوي على الجزء الأكبر من الذرة بأكملها. كتلة النواة أكبر بآلاف المرات من مجموع جميع الإلكترونات الموجودة في الذرة.

خصائص الجسيمات
دعونا نلقي نظرة على كيفية العثور على البروتونات والنيوترونات والإلكترونات في الذرة، والتعرف على ميزاتها. البروتون هو ما يتوافق مع نواة ذرة الهيدروجين. كتلته تتجاوز الإلكترون بـ 1836 مرة. لتحديد وحدة الكهرباء التي تمر عبر موصل بمقطع عرضي معين، يتم استخدام الشحنة الكهربائية.
تحتوي كل ذرة على عدد معين من البروتونات في نواتها. إنها قيمة ثابتة وتميز الخواص الكيميائية والفيزيائية لعنصر معين.
كيف تجد البروتونات والنيوترونات والإلكترونات في ذرة الكربون؟ العدد الذري لهذا العنصر الكيميائي هو 6، وبالتالي فإن النواة تحتوي على ستة بروتونات. وفقا للنظام الكوكبي، تتحرك ستة إلكترونات في مدارات حول النواة. ولتحديد عدد النيوترونات من قيمة الكربون (12)، نطرح عدد البروتونات (6)، فنحصل على ستة نيوترونات.
بالنسبة لذرة الحديد فإن عدد البروتونات يساوي 26، أي أن هذا العنصر له العدد الذري 26 في الجدول الدوري.
النيوترون هو جسيم متعادل كهربائيًا، وغير مستقر في حالته الحرة. يمكن للنيوترون أن يتحول تلقائيًا إلى بروتون موجب الشحنة، وينبعث منه مضاد النيوترينو والإلكترون. متوسط عمر النصف هو 12 دقيقة. العدد الكتلي هو إجمالي عدد البروتونات والنيوترونات الموجودة داخل نواة الذرة. دعونا نحاول معرفة كيفية العثور على البروتونات والنيوترونات والإلكترونات في الأيون؟ إذا اكتسبت الذرة أثناء التفاعل الكيميائي مع عنصر آخر حالة أكسدة إيجابية، فإن عدد البروتونات والنيوترونات فيها لا يتغير، فقط الإلكترونات تصبح أقل.

خاتمة
كانت هناك العديد من النظريات المتعلقة ببنية الذرة، لكن لم تكن أي منها قابلة للتطبيق. قبل النسخة التي أنشأها رذرفورد، لم يكن هناك تفسير مفصل لموقع البروتونات والنيوترونات داخل النواة، وكذلك دوران الإلكترونات في مدارات دائرية. بعد ظهور نظرية التركيب الكوكبي للذرة، أتيحت للباحثين الفرصة ليس فقط لتحديد عدد الجزيئات الأولية في الذرة، ولكن أيضًا للتنبؤ بالخصائص الفيزيائية والكيميائية لعنصر كيميائي معين.
→يعرف الكثير من الناس جيدًا من المدرسة أن جميع المواد تتكون من ذرات. وتتكون الذرات بدورها من بروتونات ونيوترونات تشكل نواة الذرات والإلكترونات الموجودة على مسافة ما من النواة. لقد سمع الكثيرون أيضًا أن الضوء يتكون أيضًا من جسيمات - فوتونات. ومع ذلك، فإن عالم الجسيمات لا يقتصر على هذا. حتى الآن، تم التعرف على أكثر من 400 جسيم أولي مختلف. دعونا نحاول أن نفهم كيف تختلف الجسيمات الأولية عن بعضها البعض.
هناك العديد من العوامل التي يمكن من خلالها تمييز الجسيمات الأولية عن بعضها البعض:
- وزن.
- الشحنة الكهربائية.
- حياة. تمتلك جميع الجسيمات الأولية تقريبًا عمرًا محددًا، وبعد ذلك تتحلل.
- يلف. ويمكن اعتبارها، بشكل تقريبي، كلحظة دورانية.
المزيد من المعلمات، أو كما يطلق عليها عادة في علم الأعداد الكمومية. هذه المعلمات ليس لها دائمًا معنى فيزيائي واضح، ولكنها ضرورية لتمييز بعض الجسيمات عن غيرها. يتم تقديم كل هذه المعلمات الإضافية كبعض الكميات التي يتم الاحتفاظ بها في التفاعل.
تمتلك جميع الجسيمات تقريبًا كتلة، باستثناء الفوتونات والنيوترينوات (وفقًا لأحدث البيانات، تمتلك النيوترينوات كتلة، ولكنها صغيرة جدًا لدرجة أنها غالبًا ما تعتبر صفرًا). وبدون الكتلة لا يمكن للجسيمات أن توجد إلا في حالة حركة. جميع الجسيمات لها كتل مختلفة. يمتلك الإلكترون أصغر كتلة، باستثناء النيوترينو. تمتلك الجسيمات التي تسمى الميزونات كتلة أكبر بـ 300-400 مرة من كتلة الإلكترون، والبروتون والنيوترون أثقل بحوالي 2000 مرة من الإلكترون. تم الآن اكتشاف جسيمات أثقل من البروتون بحوالي 100 مرة. الكتلة (أو ما يعادلها من الطاقة حسب صيغة أينشتاين:
يتم الحفاظ عليه في جميع تفاعلات الجسيمات الأولية.
ليست كل الجسيمات لها شحنة كهربائية، مما يعني أنه ليست كل الجسيمات قادرة على المشاركة في التفاعل الكهرومغناطيسي. جميع الجسيمات الموجودة بحرية لها شحنة كهربائية مضاعفة لشحنة الإلكترون. بالإضافة إلى الجسيمات الموجودة بحرية، هناك أيضًا جزيئات في حالة مقيدة فقط، وسنتحدث عنها بعد قليل.
إن الدوران، مثل الأرقام الكمومية الأخرى، يختلف باختلاف الجسيمات ويميز تفردها. يتم حفظ بعض الأعداد الكمومية في بعض التفاعلات، وبعضها في تفاعلات أخرى. تحدد كل هذه الأرقام الكمومية أي الجسيمات تتفاعل معها وكيف. 
يعد العمر أيضًا خاصية مهمة جدًا للجسيم، وسنتناولها بمزيد من التفصيل. لنبدأ بملاحظة. وكما قلنا في بداية المقال، فإن كل ما يحيط بنا يتكون من ذرات (إلكترونات وبروتونات ونيوترونات) وضوء (فوتونات). وأين إذن توجد مئات الأنواع المختلفة من الجسيمات الأولية؟ الجواب بسيط - في كل مكان حولنا، لكننا لا نلاحظه لسببين.
أولها هو أن جميع الجسيمات الأخرى تقريبًا تعيش لفترة قصيرة جدًا، تقريبًا 10 أس 10 أس ناقص ثانية أو أقل، وبالتالي لا تشكل هياكل مثل الذرات والشبكات البلورية وما إلى ذلك. أما السبب الثاني فيتعلق بالنيوترينوات؛ فبالرغم من أن هذه الجسيمات لا تضمحل، إلا أنها لا تخضع إلا للتفاعلات الضعيفة والجاذبية. وهذا يعني أن هذه الجسيمات تتفاعل بشكل ضئيل للغاية بحيث يكاد يكون من المستحيل اكتشافها.
دعونا نتصور مدى تفاعل الجسيم. على سبيل المثال، يمكن إيقاف تدفق الإلكترونات بواسطة صفيحة رقيقة إلى حد ما من الفولاذ، في حدود بضعة ملليمترات. سيحدث هذا لأن الإلكترونات ستبدأ على الفور في التفاعل مع جزيئات الصفائح الفولاذية، وتغير اتجاهها بشكل حاد، وتنبعث منها فوتونات، وبالتالي تفقد الطاقة بسرعة كبيرة. لكن هذا ليس هو الحال مع تدفق النيوترينو، إذ يمكن أن يمر عبر الأرض دون أي تفاعلات تقريبًا. وبالتالي من الصعب جدًا اكتشافها.
لذا، فإن معظم الجسيمات تعيش لفترة قصيرة جدًا، وبعد ذلك تتحلل. اضمحلال الجسيمات هي التفاعلات الأكثر شيوعا. نتيجة للتحلل، ينقسم أحد الجسيمات إلى عدة جسيمات أخرى ذات كتلة أصغر، وهي بدورها تتحلل أكثر. تخضع جميع حالات الاضمحلال لقواعد معينة - قوانين الحفظ. لذلك، على سبيل المثال، نتيجة للاضمحلال، يجب الحفاظ على الشحنة الكهربائية والكتلة واللف وعدد من الأعداد الكمومية الأخرى. قد تتغير بعض الأرقام الكمومية أثناء الاضمحلال، ولكنها تخضع أيضًا لقواعد معينة. إن قواعد الاضمحلال هي التي تخبرنا أن الإلكترون والبروتون جسيمات مستقرة. لم يعد بإمكانهم الاضمحلال خاضعين لقواعد الانحلال، وبالتالي فهم من ينهي سلاسل الانحلال.
هنا أود أن أقول بضع كلمات عن النيوترون. ويتحلل النيوترون الحر أيضًا إلى بروتون وإلكترون في حوالي 15 دقيقة. ومع ذلك، فإن هذا لا يحدث عندما يكون النيوترون في نواة الذرة. ويمكن تفسير هذه الحقيقة بطرق مختلفة. على سبيل المثال، عندما يظهر إلكترون وبروتون إضافي من نيوترون متحلل في نواة الذرة، يحدث رد فعل عكسي على الفور - يمتص أحد البروتونات إلكترونًا ويتحول إلى نيوترون. هذه الصورة تسمى التوازن الديناميكي. وقد لوحظ في الكون في مرحلة مبكرة من تطوره، بعد وقت قصير من الانفجار الأعظم.
بالإضافة إلى تفاعلات الاضمحلال، هناك أيضًا تفاعلات تشتت - عندما يتفاعل جسيمان أو أكثر في وقت واحد، ونتيجة لذلك يتم الحصول على جسيم آخر أو أكثر. هناك أيضًا تفاعلات امتصاص، عندما ينتج جسيمان أو أكثر جسيمًا واحدًا. تحدث جميع التفاعلات نتيجة لتفاعلات قوية ضعيفة أو كهرومغناطيسية. ردود الفعل الناتجة عن التفاعل القوي هي الأسرع، ويمكن أن يصل وقت هذا التفاعل إلى 10 ناقص 20 ثانية. تكون سرعة التفاعلات التي تحدث بسبب التفاعل الكهرومغناطيسي أقل، ويمكن أن يكون الوقت هنا حوالي 10 ناقص 8 ثوانٍ. وفي التفاعلات الضعيفة يمكن أن يصل الزمن إلى عشرات الثواني وأحيانا سنوات.
في نهاية القصة عن الجسيمات، دعونا نتحدث عن الكواركات. الكواركات هي جسيمات أولية لها شحنة كهربائية تعادل ثلث شحنة الإلكترون ولا يمكن أن توجد في حالة حرة. يتم ترتيب تفاعلهم بطريقة لا يمكنهم العيش إلا كجزء من شيء ما. على سبيل المثال، مزيج من ثلاثة كواركات من نوع معين يشكل بروتونًا. مزيج آخر ينتج النيوترون. إجمالي 6 كواركات معروفة. مجموعاتها المختلفة تعطينا جسيمات مختلفة، وعلى الرغم من أن القوانين الفيزيائية لا تسمح بجميع مجموعات الكواركات، إلا أن هناك الكثير من الجسيمات المكونة من الكواركات.
وهنا قد يطرح السؤال: كيف يمكن تسمية البروتون بأنه أولي إذا كان يتكون من كواركات؟ الأمر بسيط للغاية - البروتون عنصر أساسي، لأنه لا يمكن تقسيمه إلى الأجزاء المكونة له - الكواركات. جميع الجسيمات التي تشارك في التفاعل القوي تتكون من كواركات، وهي في نفس الوقت أولية.
إن فهم تفاعلات الجسيمات الأولية مهم جدًا لفهم بنية الكون. كل ما يحدث للأجسام الكبيرة هو نتيجة تفاعل الجزيئات. إن تفاعل الجزيئات هو الذي يصف نمو الأشجار على الأرض، وردود الفعل داخل النجوم، والإشعاع الصادر عن النجوم النيوترونية، وغير ذلك الكثير.
| الاحتمالات وميكانيكا الكم | > |