7. Ərimə və kristallaşma (§ 12-14)
1. Tədris materialını öyrənin
Maddənin məcmu halları
Ərimə və kristallaşma
2. Özünüzü sınayın. Testlər "Materiyanın aqreqativ halları", "Ərimə və bərkimə"
3. Suallara cavab verin:
1. Ərimə və bərkimə prosesində molekulların sürətləri və aralarındakı boşluqlar necə dəyişir? Hansı proses orqanizmin daxili enerjisinin artması, hansının azalması ilə müşayiət olunur?
2. Sıfır temperaturda buz eyni temperaturda suya qoyularsa, onunla nə baş verir?
3. İsti suyun temperaturunu nə daha çox aşağı salacaq: bir buz parçası və ya sıfır temperaturda eyni miqdarda su?
4. “Ərimə nöqtəsi” cədvəlindən istifadə edərək tapın: 230°C temperaturda qalay hansı vəziyyətdədir; 1503 ° C temperaturda polad; -215°C temperaturda azot?
5. Qrafikdən istifadə edərək suallara cavab verin:
İlkin bədən istiliyi nədir?
- Bədənin əriməsi hansı dövrdə başlayıb?
- İstilik prosesləri hansı maddə ilə baş verdi?
- isitmə başlayandan 3 dəqiqə sonra bədən hansı vəziyyətdə idi?
- Bədənin əriməsi nə qədər çəkdi?
- isitmə başlayandan 8 dəqiqə sonra bədən hansı vəziyyətdə idi?
6. Orqanizmdə baş verən istilik proseslərinin qrafikini qurun:
su: 80°С —› - 10°С
Buz bir qaba qoyularsa və yanan ocağın üzərinə qoyularsa, konteyner qızar və buz əriməyə başlayır. Bununla belə, bütün buz mayeləşənə qədər, sobanın nə qədər isti olmasından asılı olmayaraq, suyun temperaturu 0°C-dən (32°F) yuxarı qalxmayacaq. Bu, buza verilən bütün istiliyin onun molekullarını bir-birinə bağlayan fiziki qüvvələri aradan qaldırmaq üçün istifadə edilməsi ilə əlaqədardır.
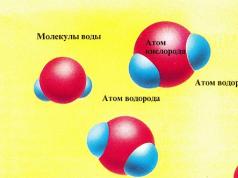
Buzda su molekulları bir molekulun hidrogen atomu (mavi rənglə göstərilmişdir) və digərinin oksigen atomu (qırmızı rənglə göstərilmişdir) arasında əmələ gələn molekullararası bağlarla bir yerdə saxlanılır. Yaranan altıbucaqlı kristal quruluş kifayət qədər yüksək gücə malikdir. 0°C-də molekullar o qədər sürətlə hərəkət edir ki, bağlar zəifləyir. Molekullararası bağların bəziləri qırılır və su molekullarının maye əmələ gəlməsi üçün buzdan ayrılmasına imkan verir. Bu proses faza keçidi (suyun bərk fazadan maye fazaya keçməsi) adlanır və onun baş verdiyi temperatura ərimə nöqtəsi deyilir.
Suyun bərk vəziyyətdə qalmasına imkan verən bağları qırmaq üçün enerji lazımdır və çox böyük miqdarda, buna görə də ocaq tərəfindən yaranan bütün istilik buzun temperaturunu artırmağa deyil, bu bağları qırmağa gedir. Yuxarıda təsvir olunan faza çevrilməsini başa çatdırmaq üçün tələb olunan istilik ərimənin gizli istiliyi və ya faza dəyişmə istiliyi adlanır, çünki bu istilik temperaturun artmasına səbəb olmur. Yalnız sonuncu bağlar qırıldıqdan və bütün buzlar əridikdən sonra suyun temperaturu artmağa və 0°C-dən yuxarı qalxmağa başlayacaq.
Buz necə əriyir?
- Buzda su molekulları o qədər yavaş hərəkət edir ki, onlar həmişə bir-birinə bağlı qalaraq bərk cisim əmələ gətirirlər. Buza istilik tətbiq edildikdə (sağdakı şəkildə sarı toplar kimi göstərilir) su molekulları əlavə enerji qazanır və daha sürətli hərəkət edir, lakin yenə də buz kimi bir-birinə bağlıdır.
- İstilik tədarükü davam edərsə, buz səthindəki su molekulları əvvəllər onları yerində saxlayan molekullararası bağları qıraraq, vibrasiya hərəkətlərinin sürətini artırır. Bu molekullar buzu tərk edərək suyun maye fazasını əmələ gətirir. Əlavə istilik təchizatı qalan molekullararası bağların məhvinə və buzun tədricən əriməsinə səbəb olur.
- Davamlı istilik əlavəsi nəticədə donmuş su molekullarının sonuncusuna onları buz kimi bir yerdə saxlayan molekullararası bağları aradan qaldırmaq üçün kifayət qədər enerji verir. İndi bütün su maye halına gəldi.

Buz, su və temperatur

Buza istilik verildikdə (soldakı rəqəm) əvvəlcə onun temperaturu artır. Lakin 0°C-də (32°F) temperaturun artması dayanır və faza keçidi baş verir: buz əriməyə başlayır. Qrafikdəki mavi əyridən göründüyü kimi, əlavə istilik girişi suyun temperaturunu artırmadan buzun daha da əriməsinə gətirib çıxarır. Yalnız bütün buzlar maye vəziyyətə çevrildikdən sonra (mətnin üstündəki rəqəm) əlavə istilik təchizatı suyun temperaturunun artmasına səbəb olur.
Maddənin bərk kristal vəziyyətindən maye halına keçməsi adlanır ərimə. Bərk kristal cismi əritmək üçün onu müəyyən bir temperatura qədər qızdırmaq, yəni istilik vermək lazımdır.Bir maddənin əridiyi temperatur deyilirmaddənin ərimə nöqtəsi.
Əks proses - mayedən bərk vəziyyətə keçid - temperatur azaldıqda, yəni istilik çıxarıldıqda baş verir. Maddənin maye haldan bərk vəziyyətə keçməsi adlanırsərtləşmə , və ya kristallizizasiya . Bir maddənin kristallaşdığı temperatur deyilirkristal temperaturus .
Təcrübə göstərir ki, istənilən maddə eyni temperaturda kristallaşır və əriyir.
Şəkildə kristal cismin (buz) istiləşmə müddətinə (nöqtədən) qarşı temperaturunun qrafiki göstərilir. A nöqtəsinə D) və soyutma vaxtı (nöqtədən D nöqtəsinə K). Üfüqi ox boyunca vaxtı və şaquli ox boyunca temperaturu göstərir.
Qrafik göstərir ki, prosesin müşahidəsi buzun temperaturu -40 ° C və ya necə deyərlər, zamanın ilk anındakı temperatur olduğu andan başlayıb. tBaşlanğıc= -40 °C (nöqtə A qrafik üzrə). Daha çox isitmə ilə buzun temperaturu artır (qrafikdə bu bölmədir AB). Temperatur 0 °C-ə qədər yüksəlir - buzun ərimə temperaturu. 0°C temperaturda buz əriməyə başlayır və onun temperaturu yüksəlməyi dayandırır. Bütün ərimə zamanı (yəni bütün buz əriyənə qədər) buzun temperaturu dəyişmir, baxmayaraq ki, ocaq yanmağa davam edir və buna görə də istilik verilir. Ərimə prosesi qrafikin üfüqi hissəsinə uyğundur Günəş . Yalnız bütün buzlar əriyib suya çevrildikdən sonra temperatur yenidən yüksəlməyə başlayır (bölmə CD). Suyun temperaturu +40 ° C-ə çatdıqdan sonra brülör söndürülür və su soyumağa başlayır, yəni istilik çıxarılır (bunun üçün su ilə bir qabı başqa, buzla daha böyük bir qabda yerləşdirə bilərsiniz). Suyun temperaturu azalmağa başlayır (bölmə DE). Temperatur 0 °C-ə çatdıqda, istilik hələ də çıxarılsa da, suyun temperaturu azalmağı dayandırır. Bu suyun kristallaşması prosesidir - buz əmələ gəlməsi (üfüqi hissə E.F.). Bütün su buza çevrilənə qədər temperatur dəyişməyəcək. Yalnız bundan sonra buzun temperaturu azalmağa başlayır (bölmə FK).
Baxılan qrafikin görünüşü aşağıdakı kimi izah olunur. Məkan aktivdir AB Verilən istilik hesabına buz molekullarının orta kinetik enerjisi artır və onun temperaturu yüksəlir. Məkan aktivdir Günəş kolbanın məzmunu tərəfindən alınan bütün enerji buz kristal şəbəkəsinin məhvinə sərf olunur: onun molekullarının nizamlı məkan düzülüşü nizamsız olanı ilə əvəz olunur, molekullar arasındakı məsafə dəyişir, yəni. Molekullar elə yerləşdirilib ki, maddə maye olur. Molekulların orta kinetik enerjisi dəyişmir, buna görə də temperatur dəyişməz qalır. Ərinmiş buz-suyun temperaturunun daha da artması (bölgədə CD) ocaq tərəfindən verilən istilik hesabına su molekullarının kinetik enerjisinin artması deməkdir.
Suyu soyudarkən (bölmə DE) enerjinin bir hissəsi ondan alınır, su molekulları daha aşağı sürətlə hərəkət edir, onların orta kinetik enerjisi aşağı düşür - temperatur azalır, su soyuyur. 0°C-də (üfüqi hissə E.F.) molekullar kristal qəfəs əmələ gətirərək müəyyən ardıcıllıqla düzülməyə başlayır. Bu proses başa çatana qədər, istiliyin çıxarılmasına baxmayaraq, maddənin temperaturu dəyişməyəcək, yəni bərkidikdə maye (su) enerji buraxır. Bu, buzun udduğu, mayeyə çevrildiyi enerjidir (bölmə Günəş). Mayenin daxili enerjisi bərkinkindən böyükdür. Ərimə (və kristallaşma) zamanı bədənin daxili enerjisi kəskin şəkildə dəyişir.
1650 ºС-dən yuxarı temperaturda əriyən metallar adlanır odadavamlı(titan, xrom, molibden və s.). Volfram onların arasında ən yüksək ərimə nöqtəsinə malikdir - təxminən 3400 ° C. Odadavamlı metallar və onların birləşmələri təyyarə tikintisində, raket və kosmik texnologiyada, nüvə enerjisində istiliyədavamlı materiallar kimi istifadə olunur.
Bir daha vurğulayaq ki, maddə əriyərkən enerjini udur. Kristallaşma zamanı isə əksinə, onu ətraf mühitə buraxır. Kristallaşma zamanı ayrılan müəyyən miqdarda istilik qəbul edərək, mühit qızdırılır. Bu, bir çox quşlara yaxşı məlumdur. Təəccüblü deyil ki, onları qışda şaxtalı havada çayları və gölləri əhatə edən buzun üzərində oturaraq görmək olar. Buz əmələ gələndə enerji ayrıldığına görə onun üstündəki hava meşədəki ağaclara nisbətən bir neçə dərəcə isti olur və quşlar bundan yararlanır.
Amorf maddələrin əriməsi.
Müəyyən bir mövcudluq ərimə nöqtələri- Bu kristal maddələrin mühüm xüsusiyyətidir. Məhz bu xüsusiyyətinə görə onları bərk cisimlərə də aid edilən amorf cisimlərdən asanlıqla ayırmaq olar. Bunlara, xüsusən də şüşə, çox viskoz qatranlar və plastiklər daxildir.
Amorf maddələr(kristal olanlardan fərqli olaraq) xüsusi bir ərimə nöqtəsi yoxdur - onlar ərimir, lakin yumşalır. Qızdırıldıqda, bir şüşə parçası, məsələn, əvvəlcə sərtdən yumşaq olur, asanlıqla əyilə və ya uzana bilər; daha yüksək temperaturda parça öz ağırlıq qüvvəsinin təsiri ilə şəklini dəyişməyə başlayır. Qızdırıldıqda qalın viskoz kütlə yatdığı qabın şəklini alır. Bu kütlə əvvəlcə bal kimi qalın, sonra xama kimi olur və nəhayət, su ilə demək olar ki, eyni az özlülüklü mayeyə çevrilir. Lakin burada bərk cismin mayeyə keçməsinin müəyyən temperaturunu göstərmək mümkün deyil, çünki o, mövcud deyil.
Bunun səbəbləri amorf cisimlərin quruluşunun kristal quruluşundan əsas fərqindədir. Amorf cisimlərdəki atomlar təsadüfi düzülür. Amorf cisimlər quruluşuna görə mayelərə bənzəyirlər. Onsuz da bərk şüşədə atomlar təsadüfi düzülüb. Bu o deməkdir ki, şüşənin temperaturunun artırılması yalnız onun molekullarının vibrasiya diapazonunu artırır və onlara getdikcə daha çox və daha çox hərəkət azadlığı verir. Buna görə də, şüşə tədricən yumşalır və molekulların ciddi qaydada düzülüşündən nizamsız birinə keçid üçün xarakterik olan kəskin "bərk-maye" keçidini nümayiş etdirmir.
Birləşmə istiliyi.
Ərimə istiliyi- bu, maddənin bərk kristal vəziyyətindən maye halına tam çevrilməsi üçün ərimə nöqtəsinə bərabər sabit təzyiq və sabit temperaturda ona verilməli olan istilik miqdarıdır. Birləşmə istiliyi maddənin maye halından kristallaşması zamanı ayrılan istilik miqdarına bərabərdir. Ərimə zamanı maddəyə verilən bütün istilik onun molekullarının potensial enerjisini artırmağa gedir. Ərimə sabit bir temperaturda baş verdiyi üçün kinetik enerji dəyişmir.
Eyni kütləli müxtəlif maddələrin əriməsini eksperimental olaraq öyrənməklə onları mayeyə çevirmək üçün müxtəlif miqdarda istilik tələb olunduğunu görmək olar. Məsələn, bir kiloqram buzu əritmək üçün 332 J, 1 kq qurğuşunu əritmək üçün isə 25 kJ enerji sərf etmək lazımdır.
Bədənin buraxdığı istilik miqdarı mənfi hesab olunur. Buna görə də kütləsi olan maddənin kristallaşması zamanı ayrılan istilik miqdarını hesablayarkən m, eyni düsturdan istifadə etməlisiniz, lakin mənfi işarə ilə:
Yanma istiliyi.
Yanma istiliyi(və ya kalorifik dəyər, kalori məzmunu) yanacağın tam yanması zamanı ayrılan istilik miqdarıdır.
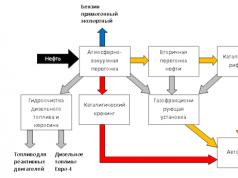
Bədənləri qızdırmaq üçün tez-tez yanacağın yanması zamanı ayrılan enerji istifadə olunur. Adi yanacaq (kömür, neft, benzin) karbon ehtiva edir. Yanma zamanı karbon atomları havadakı oksigen atomları ilə birləşərək karbon qazı molekullarını əmələ gətirir. Bu molekulların kinetik enerjisi ilkin hissəciklərinkindən daha böyük olur. Yanma zamanı molekulların kinetik enerjisinin artmasına enerji buraxılması deyilir. Yanacağın tam yanması zamanı ayrılan enerji bu yanacağın yanma istiliyidir.
Yanacağın yanma istiliyi yanacağın növündən və kütləsindən asılıdır. Yanacağın kütləsi nə qədər çox olarsa, onun tam yanması zamanı ayrılan istilik miqdarı bir o qədər çox olar.
1 kq ağırlığında yanacağın tam yanması zamanı nə qədər istilik ayrıldığını göstərən fiziki kəmiyyət deyilir. yanacağın xüsusi yanma istiliyi.Xüsusi yanma istiliyi hərflə təyin olunurqvə kiloqram üçün joul ilə ölçülür (J/kq).
İstiliyin miqdarı Q yanma zamanı sərbəst buraxılır m kq yanacaq düsturla müəyyən edilir:
İxtiyari kütləli yanacağın tam yanması zamanı ayrılan istilik miqdarını tapmaq üçün bu yanacağın xüsusi yanma istiliyini onun kütləsinə vurmaq lazımdır.
Fizikadan müstəqil iş Maddənin aqreqat halları 8-ci sinif şagirdləri üçün Kristal cisimlərin əriməsi və bərkiməsi. Müstəqil iş hər birində 5 tapşırıq olan 2 variantdan ibarətdir.
1 seçim
1. Ərimə və bərkimə prosesində molekulların sürətləri və aralarındakı boşluqlar necə dəyişir? Hansı proses daxili enerjinin artması və hansının azalması ilə müşayiət olunur?
2. Sıfır temperaturda buz eyni temperaturda suya qoyularsa, onunla nə baş verir?
3. İsti suyun temperaturunu nə daha çox aşağı salacaq: bir buz parçası və ya sıfır temperaturda eyni miqdarda su?
4. Payızda borularda su qalıb, yazda isə boruların partladığı məlum olub. Niyə?
5. Bəzən avtomobilin ön şüşəsində çiplər və ulduzlar görünür. Buna səbəb isə qarşıdakı avtomobillərdən daşların vurmasıdır. Niyə ilk dondan əvvəl bu şüşə qüsurlarını aradan qaldırmaq lazımdır?
Seçim 2
1. Kalay bir aqreqasiya vəziyyətindən digərinə keçir. Daxili enerjisini artırdığı məlumdursa, bərk və ya əriyib?
2. Hansı halda su daha yüksək temperatura qədər qızacaq: bərkimə temperaturunda ona maye qalay tökülsə və ya ərimə temperaturunda bərk qalay atılacaqsa?
3. Niyə zirzəmiyə qoyulmuş su ilə böyük bir gəmi tərəvəzləri ilk dondan xilas edir?
4. Bəzən dondurucuda qalan su şüşələri çatlayır. Niyə?
5. Buzlaqlar harada və nə vaxt əmələ gəlir?
Fizikadan müstəqil işə cavablar Maddənin aqreqat halları Kristal cisimlərin əriməsi və bərkiməsi
1 seçim
1. Əritmə zamanı molekulların sürəti artır, bərkidikdə isə əksinə, azalır. Əritmə zamanı daxili enerji artır, bərkidikdə isə azalır.
2. Buz mütləq suda üzəcək, çünki buzun sıxlığı suyun sıxlığından azdır, lakin buz mütləq əriməyəcək, çünki sudan ərimək üçün istilik almayacaq, çünki eyni temperaturda istilik mübadiləsi mümkün deyil.
3. Bir parça buz, çünki qızdırmaqdan əlavə, buzun əriməsinə bir qədər istilik sərf olunacaq.
4. Su donduqda genişlənir.
5. Çünki su bu çiplərin içinə girəcək və donduqda buzun həcmi suyun həcmindən çox olacaq və buz şüşəni məhv etməyə davam edəcək, çipi və ölçüsünü artıracaq.
Seçim 2
1. Daxili enerjini artırdığı üçün əriyib. Sərtləşmə isə bu enerjini buraxması ilə xarakterizə olunur.
2. Qatılaşma temperaturunda maye qalay töksəniz.
3. Qəfil soyuqluq olarsa, su donar. Su donduqda bir qədər istilik ayrılır.
4. Dondurma zamanı suyun həcmi artır.
5. Temperaturun şaxtadan yuxarı olduğu yerdən suyun temperaturun sıfırdan aşağı olduğu yerə yavaş-yavaş axması zamanı buzlaqlar əmələ gəlir. Məsələn: günəş damı qızdırır və qar əriyir.