12884 0
При хистероскопия в първата половина на фазата на пролиферация (до 7-ия ден от цикъла) ендометриумът е блед, тънък, с малки кръвоизливи и единични бледорозови участъци от неотхвърлен ендометриум. Устите фалопиевите тръбидобре различими.
През втората половина на фазата на пролиферация (от 9-ия ден на цикъла) ендометриумът е блед Розов цвят, удебелени, съдовете не са изразени. По-късно в определени области се разграничават удебелени надлъжни или напречни гънки.
Във фазата на секреция ендометриума жълтеникав цвят, удебелени. Установяват се гънки, които са особено добре изразени в горната трета на тялото на матката. 2-3 дни преди менструацията ендометриумът е червен с области на тъмно лилаво отхвърляне. Отворите на фалопиевите тръби могат да бъдат скрити от гънките на ендометриума.
Първите 2-3 дни по време на менструацията маточната кухина е изпълнена с отхвърлени слоеве на ендометриума: в горната трета е тъмно лилаво на цвят, в долната и средната третина е бледо розово.
По време на постменопаузалния период хистероскопията разкрива картина на ендометриална атрофия. В този случай ендометриумът е изтънен и има блед цвят.
По време на колпоскопия лигавицата на шийката на матката е гладка, лъскава и розова.
При жени след менопауза обикновено се открива изтъняване на епитела, през който се виждат съдовете.
По време на лапароскопия непроменената матка е покрита с лъскав перитонеум, има гладка повърхност и характерна форма със симетрия спрямо надлъжната равнина.
При хистеросалпингография сянката на маточната кухина има формата на триъгълник с леко вдлъбнати страни и ясни, равномерни контури. Основата на триъгълника е обърната нагоре, а върхът - надолу.
Горните ъгли съответстват на отворите на фалопиевите тръби, долният ъгъл съответства на вътрешния отвор на цервикалния канал. Маточната кухина съдържа от 4 до 6 ml контрастна течност.
При ултразвук контурите на нормалната матка са ясни и равномерни, с овална или крушовидна форма. Плътността на ехото на ендометриума е по-висока от плътността на ехото на миометриума, която не се променя в зависимост от фазата менструален цикъл. Ехоструктурата на непроменения миометриум е фино диспергирана поради множество точкови и линейни ехо сигнали.
Ендометриумът се определя като ехо-позитивна формация, която е линейна (след края на менструалното кървене), овална или капковидна. Веднага след края на менструалния цикъл ендометриумът може да се проследи под формата на ехоположителна ивица с дебелина 1-2 mm.

На 8-10 дни от цикъла (средата на фазата на пролиферация) ендометриумът се удебелява донякъде, средно до 8 mm (от 5 до 10 mm). Структурата на ехото остава практически непроменена в сравнение с предходния период.

В късната фаза на пролиферация (11-14 дни), в допълнение към по-нататъшното удебеляване, средно до 11 mm (от 7 до 14 mm), ехогенността на ендометриума започва леко да се увеличава и става близка до средната.

В ранната фаза на секреция (15-18 дни) скоростта на растеж на ендометриума намалява, достигайки дебелина от 12 mm. Ехогенността на ендометриума продължава да се увеличава от периферията към центъра, в резултат на което хипоехогенният централен фрагмент придобива форма на сълза ( широка частв областта на фундуса на матката се стеснява към шийката на матката). По време на тази фаза хиперехогенната линия в центъра вече не се вижда ясно.

Във фазата на средна секреция (19-23 дни) ендометриумът достига максималната си дебелина - средно 14 mm (от 12 до 18 mm). Ехогенността на ендометриума се увеличава още повече, хиперехогенната линия в центъра не се визуализира ясно.

На 24-27 дни от цикъла (късна секреция) дебелината на ендометриума леко намалява - средно до 12 mm (от 10 до 17 mm). Характеристика на този период е високата ехогенност на ендометриума в комбинация с неговата хетерогенна вътрешна ехоструктура, поради което линията на затваряне престава да се визуализира.

По време на менструация в маточната кухина се открива тънка хиперехогенна ивица или хиперехогенни ехоструктури (кръвни съсиреци). Понякога кухината изглежда леко разширена поради ехо-отрицателно съдържание.

Маточната кухина в постменопаузата е М-ехо под формата на тънка хиперехогенна линия, обикновено с дебелина 1-2 mm (не повече от 4-5 mm).

При ядрено-магнитна томография (NMT) през първата половина на цикъла, ендометриумът в средния сагитален участък се определя като тънка линия (до 3 mm), миометриумът изглежда като хомогенна структура с гладки контури.

През втората половина на цикъла ендометриумът се визуализира като доста хомогенна структура със средна дебелина 7 mm, по-интензивна от миометриума.

В постменопаузалния период томограмите показват намаляване на обема на матката с намаляване на интензивността на изображението на миометриума, докато ендометриумът, като правило, не се визуализира.

Шийката на матката се определя на томограмите като неинтензивна цилиндрична зона с ясна гладък контур, чиято структура и кухина съответстват на тялото на матката. Ултразвуковото изследване обикновено не визуализира цервикалния канал.
В.Н. Серов, И.Н. Звенигородски
Dueholm, C. Møller, S. Rydbjerg, E. S. Hansen, G. Ørtoft
P.G.Leone, D.Timmerman, T.Bourne, L.Valentin, E.Epstein, S.R.Goldstein, H.Marret, A.K.Parsons, B.Gull, O.Istre, W.Sepulveda, E.Ferrazzi, T.Van den Bosch
Трансвагинално ултразвуково изследванеТо има голямо значениепри диагностицирането на рак на ендометриума при жени с постменопаузално кървене. Жените с дебелина на ендометриума ≤ 4 mm, измерена чрез трансвагинално сканиране, имат нисък риск от развитие на рак на ендометриума (1 на 100 случая), ако не приемат хормонална заместителна терапия. хормонална терапия, 1 на 1000, ако приемат терапия). Жени с постменопаузално кървене и дебелина на ендометриума ≥ 5 mm имат висок рискрак на ендометриума (1 от 4 случая), така че е необходимо да се получи висококачествено вътрематочно остъргване за хистологичен анализ. Ултразвукът може да предостави информация за индивидуалния риск злокачествени новообразуванияпри жени в постменопауза с кървене и дебелина на ендометриума ≥ 5 mm.
Нашето проучване включва жени с постменопаузално кървене и дебелина на ендометриума ≥ 5 mm, измерено с трансвагинална сонда. Проучването е проведено в университетската болница в Орхус, Дания, между ноември 2010 г. и февруари 2012 г. Всички жени са подложени на трансвагинално сканиране (TVS) и сонография с гел инфузия (GIS) и всички са планирани за хистероскопия с резектоскопска биопсия и допълнителен кюретаж за оценка на вътрематочни патологии (Таблица 1).
Маса 1. Схема за избор на пациенти за изследването.
Трансвагинално сканиране (TVS)
TVS се извършва на Voluson E8 Expert, оборудван с ендовагинален сензор (6-12 MHz), съгласно протокола за сканиране. Доплеровите параметри бяха зададени предварително, стандартизирани (честота 6 MHz, доплерово усилване на мощността 50, динамичен диапазон 10 dB; устойчивост 2, цвят на картата 1, филтър 3).
TVS сканирането включваше визуална оценка на следните определени параметри Международна групаАнализ на ендометриален тумор (IETA): дебелина на ендометриума, неговата ехогенност (хипер-, хипо- и изоехогенна, хомо/хетерогенна), кистозна компонента (да/не), ако е налице, след това гладки или неравни граници, ендометриални граници (гладки или неравни) , хомо-/хетерогенен), линия на затваряне (да/не), прекъсната (да/не)).
Мощният доплеров анализ включва визуална оценка на следните параметри: съдове (наличие (да / не), наличие на доминиращ съд (да / не), ако има доминиращ съд, тогава единичен (да / не) или двоен (да / не), произход (фокални / мултифокални) множество съдове (да / не); разклонения (да / не), ако има разклонения, тогава подредени / неподредени, кръгова посока на съдовете (да / не) Оценяваме субективно: големи съдове (да/не), цветен доплер (да/не), съдова плътност (да/не).
Инфузионна сонография с гел (GIS)
ГИС е извършена след TVS. Използвахме малък гъвкав стерилен катетър, снабден със спринцовка от 10 ml, съдържаща Instillagel® (E.Tjellesen A/S, Lynge, Дания), който беше вкаран в маточната кухина. При пациентки със запушена шийка на матката използвахме малък дилататор Hegar. Гелът се въвежда в маточната кухина под ултразвуков контрол.
След това маточната кухина се сканира в сагиталната и напречната равнина, като се оценяват същите параметри, както при конвенционалните TVS. Оценени са още: наличието на образувание, местоположението му и процентът на увреждане на ендометриума (т.е. ≤ 25% от повърхността е увредена) (да/не); Повърхностна структура на локално увреждане (равномерно / неравномерно); Структурата на общата повърхност на ендометриума (гладка, полиповидна, неравна).
Хистероскопия
При всички пациенти е извършена амбулаторна хистероскопия с локално или обща анестезия. При 112 пациентки хистероскопията е извършена веднага след ултразвуковото изследване, при останалите пациентки при следващо посещение до 3 седмици след ехографското изследване. По време на хистероскопията са направени опити за отстраняване на цялата тъкан от маточната кухина. Три до пет ендометриални проби бяха събрани от един пациент.
Изчисляване на риска от развитие на рак на ендометриума с помощта на точкова система
(Риск от рак на ендометриума скор (REC скор))
Въз основа на нашите анализи разработихме система за оценка на риска за рак на ендометриума (Фиг. 1). Системата за оценяване включва индекс на телесна маса (≥30 = 1 точка), дебелина на ендометриума (≥10 mm = 1 точка), (≥15 mm = 1 точка), наличие на васкуларизация, доминиращ съд (наличен = 1 точка), множество съдове (наличен = 1 точка), големи съдове (наличие = 1 точка) и плътни съдове (наличие = 1 точка), прекъсната ендомитриална зона (наличие = 1 точка) и неравна ендометриална повърхност на GIS (наличие = 1 точка). Добавянето на тези стойности създава резултат за риск от рак на ендометриума. Резултат 3 за TVS или 4 за GIS показва добри резултати от сканирането и правилна диагноза високо ниворазвитие на рак на ендометриума при около 90% от всички пациенти.

Фиг. 1. Схематично представяне на определяне на риска от развитие на рак на ендометриума с помощта на точкова система.
Параметрите за ултразвуково изследване на ендометриума са определени от Международната група за анализ на ендометриален тумор (IETA)
Дебелината на ендометриума се измерва в сагиталната равнина. Калиперите трябва да се поставят на границата на ендометриума и миометриума, перпендикулярно на средната линия на ендометриума (фиг. 2). При наличие на течност се измерва дебелината на отделните части на ендометриума и се записва сумата им (фиг. 2b).

Фиг.2. Схематично и ултразвуково изображение на измерване на ендометриума при нормални условия (а) и при наличие на вътрематочна течност (б).
Ехогенността на ендометриума се оценява в сравнение с ехогенността на миометриума като хиперехогенност, изоехогенност или хипоехогенност.
Хомогенността на ендометриума се оценява от неговата структура. „Хомогенният” ендометриум е хомогенен и има трислойна структура (фиг. 3). „Хетерогенен“ ендометриум се описва, когато има хетерогенност в структурата, асиметрия или кистозни образувания(фиг.4).

Фиг.3. „Хомогенен“ ендометриум: (а) схематично представяне на трислоен ендометриум, (б) хипоехогенен, (в) хиперехогенен, (г) изоехогенен.
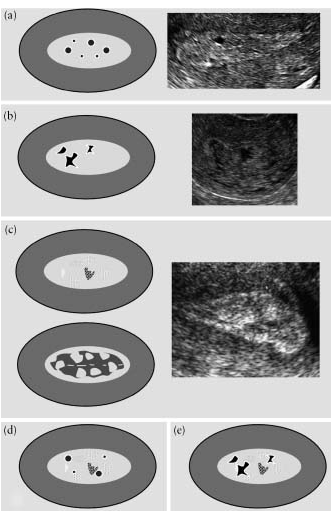
Фиг.4. „Хетерогенен“ ендометриум: кистозни образувания с гладки ръбове се визуализират на хомогенен фон (а), кистозни образувания с неравни ръбове се наблюдават на хомогенен фон (б), хетерогенен фон без кистозни зони (в), кистозни образувания с гладки ръбове присъстват на разнороден фон (d) и на разнороден фон, кистозни образувания с неравни ръбове (e).
Ендометриумът се счита за „линеен“, ако линията на затваряне на слоевете на ендометриума е определена като права, и „нелинеен“, ако линията на затваряне се визуализира като „назъбена“ или „прекъсната“ или напълно липсва (фиг. 5).
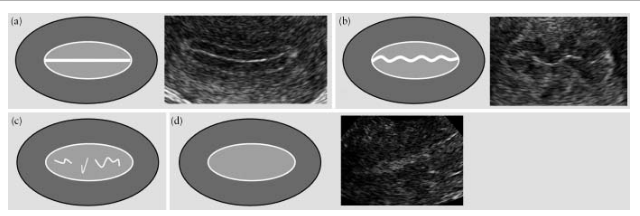
Фиг.5. Линията на затваряне на ендометриалните слоеве: „линейна“ (а), „назъбена“ (b), „прекъсната“ (c) и такава, която не се визуализира (d).
Ендометриално-миометриалната област се описва като „гладка“, „назъбена“, „прекъсната“ или „неопределена“ (фиг. 6).

Фиг.6. Ендометриално-миометриална област: „гладка“ (a), „неравна“ (b), „прекъсната“ (c) и „неопределена“ (d).
Вътрематочната течност се описва като анехогенна, изоехогенна или смесена ехогенност (фиг. 7).

Фиг.7. Вътрематочна течност: (а) хипоехогенна, (б) изоехогенна, (в) смесена ехогенност.
Доплер оценка
Настройките на Доплер трябва да се коригират, за да се осигури максимална чувствителност (ултразвукова честота най-малко 5,0 MHz, честота на повторение на импулса (PRF) 0,3-0,9 kHz, филтър на съдовата стена 30-50 Hz, доплеровото усилване на цвета трябва да се намали до, докато всички цветови артефакти изчезнат).
Доплер се оценява чрез наличието на кръвен поток: оценка 1 се дава, когато няма поток от цветни сигнали в ендометриума, резултат 2, ако може да се открие само минимален поток, резултат 3, когато е наличен умерен поток, и резултат 4, когато е очевиден значителен кръвен поток (Фигура 8).
ДИСКУСИЯ
Изградихме система за точкуване (REC), която може ефективно да разграничи доброкачествените и злокачествени образуванияендометриум. Системата за оценяване на REC идентифицира правилно лезиите при девет от 10 жени в постменопауза с дебелина на ендометриума ≥ 5 mm. Подходът за оценяване може да се използва за намаляване на броя на извършваните инвазивни процедури.
Използвахме термини и класификации, определени от Международната група за анализ на ендометриален тумор (IETA), които могат да се използват за измерване и описание на патология, локализирана в маточната кухина. Основната цел на тази работа е да се създаде списък с термини и определения, които могат да се използват както в ежедневната практика на лекарите, така и в научните изследвания.
Според V.N. Демидов и А.И. Гуса, ехографияизследването на ендометриума трябва да се извърши през първите три дни след края на менструацията; обикновено ендометриумът трябва да бъде напълно хомогенен и хипоехогенен.
При жлезиста хиперплазия(GE) дебелината на ендометриума е 1-1,5 cm, рядко достига 2,0 cm. Ехогенността на хиперплазията е повишена, ехоструктурата е хомогенна, често с множество малки анехогенни включвания. Понякога се наблюдава ефект на акустично усилване дистално от GE (фиг. 1-4). При визуализиране на области с повишена ехогенност на фона на практически непроменен ендометриум е възможно да се заключи, че фокална хиперплазияендометриум (фиг.).
Ситуацията с ултразвукова диагностикаатипична ендометриална хиперплазия (AHE). Редица автори посочват, че няма специфични ехографски критерии за диагностициране на AGE. Дебелината на ендометриума при това състояние варира от 1,5-2,0 cm, в някои случаи достига до 3,0 cm. Ехогенността на AGE е средна, ехоструктурата е хомогенна (фиг. 5-6).
Както правилно отбеляза V.N. Демидов и А.И. Gus, въпреки значителните морфологични разлики в ендометриалните полипи (жлезисти, жлезисто-фиброзни, фиброзни, аденоматозни), техният ехографски образ има много общо. Типична ехо картина на ендометриален полип (PE) е овална или кръгла формация със средна или повишена ехогенност с ясна граница между полипа и околните тъкани, обикновено под формата на анехогенен ръб (фиг. 7-15).
Размерът на полипите може да варира много значително, от 0,5 cm до 4-6 cm (в случай на жлезиста фиброзна и аденоматозна PE). При наличие на малък PE (<0.5 см) диагностика затруднена, и, как замечают В.Н. Демидов и А.И. Гус, единственным эхопризнаком может явиться деформация срединной линейной гиперэхогенной структуры М-эхо.
Доплерографияс хиперпластични процеси на ендометриума. Според B.I. Zykin, с GE кръвният поток вътре в лигавицата или не е регистриран (при 75-80% от пациентите), или са визуализирани няколко цветни локуса (фиг. 16).
Цветната доплерография на ендометриалните полипи разкрива захранващ съд под формата на "цветен мост" между суб- и ендометриалните зони (фиг. 17-18).
Индикаторите на кръвния поток при доброкачествени ендометриални хиперпластични процеси се характеризират с ниска скорост и сравнително висока устойчивост (фиг. 19-21, таблица 1). Подобни данни са получени и от други автори.
Таблица №1.Индикатори на интраендометриалния кръвен поток по време на хиперпластични процеси (B.I. Zykin, 2001).
Рак на ендометриума
Много голям брой проучвания са посветени на опитите да се свърже рискът от рак на ендометриума (ЕК) с дебелината на М-ехото, особено в постменопаузата. По този начин A. Kurjak et al считат, че дебелината на ендометриума >8 mm в перименопаузата и >5 mm в постменопаузата е патогномонична за ЕК. S. S. Suchocki и др. не са открили нито един случай на рак или хиперплазия с дебелина на ендометриума, посочват редица автори Специално вниманиедо много ниската специфичност на удебеляването на ендометриума като критерий за ендометриална ендометриоза. И така, според I. Fistonic et al. при пациенти с постменопаузално кървене дебелината на ендометриума е: 6,2 mm с атрофия на ендометриума, 12,4 mm с проста хиперплазия, 13,4 mm със сложна хиперплазия, 14,1 mm с карцином. Авторите не откриват значителни разлики в дебелината на ендометриума между групите с хиперплазия и карцином. При което средна възрастпациенти с карцином е значително по-висок (62 години). Bakour и др. , използвайки дебелина на ендометриума от 4 mm като критерий за злокачествено заболяване, успяха да диагностицират ендометриален карцином с чувствителност, специфичност, PCR, PCR от 92,9%, 50,0%, 24,1%, 97,6%. Авторите заключават, че при жени с постменопаузално кървене дебелината на ендометриума<4 мм позволяет с высокой вероятностью исключить вероятность карциномы, однако толщина 4 мм не добавляет значимой информации о наличии или отсутствии малигнизации.
При диагностицирането на ЕК оценката на вътрешната ехо структура на М-ехото може да играе важна роля. Според Т. Дубински и др. тънкият хомогенен ендометриум е прогностичен белег за доброкачествена находка, докато визуализирането на хетерогенна ехоструктура винаги изисква хистологично изследване за изясняване на диагнозата. Комбинираното използване на три ехографски критерия (дебелина 5 mm, неравен контур, хетерогенна структура на ехото) позволи на G. Weber et al. диагностицира ендометриален карцином с чувствителност, специфичност, PCR, PCR 97%, 65%, 80%, 94%.
Възможността за ехографска оценка на злокачествена инвазия в миометриума е важна. Така според F. Olaya et al. при диагностициране на дълбока инвазия на ендометриален карцином в миометриума (>50%), чувствителността, специфичността и точността на трансвагиналната ехография са 94,1%, 84,8%, 88%. При диференциране на степента на инвазия на ендометриалния карцином в миометриума (без инвазия, инвазия на слоеве, съседни на ендометриума, дълбока инвазия), чувствителността, специфичността и точността на трансвагиналната ехография са 66,2%, 83,1%, 77,2%. Получените резултати са сравними с ефективността на ЯМР без контраст и малко по-ниски от ефективността на ЯМР с контраст.
Особено забележителни са произведенията, чиито автори описват случаи на ендометриален карцином при жени в постменопауза с тънък или дори невизуализиран ендометриум или с комбинация от ехо картина на ендометриална атрофия и серометра (смята се, че ехо картината на течност в маточната кухина придружава 50% от случаите на рак на ендометриума). Така S. Li et al. открива рак на ендометриума при 3,9% от пациентите с дебелина на ендометриума<5мм. По данным М. Briley и соавт. , при постменопаузальном кровотечении у 20% пациенток с невизуализируемым эндометрием имела место карцинома. Авторы считают, что у пациенток с постменопаузальным кровотечением при визуализации тонкого эндометрия (<6мм) биопсии можно избежать, однако утолщенный, и что важно - невизуализируемый эндометрий являются показанием для биопсии. H. Krissi и соавт. описали рак эндометрия при эхокартине атрофии в сочетании с серометрой, считая, что последняя может служить показанием для биопсии, поскольку компрессия стенок матки при серометре может скрывать патологические изменения эндометрия. В то же время R. Bedner и соавт. полагают, что небольшая серометра в постменопаузе (до 5 см3) вряд ли может ассоциироваться с карциномой эндометрия, описывая случай последней с объемом внутриматочной жидкости 12см3.
Преминавайки към детайлизиране на ехо признаците на ЕК, е необходимо да се припомни, че последният е разделен на патогенетичен вариант I (PE-I), който възниква на фона на хиперплазия на ендометриума, и патогенетичен вариант II, който възниква на фона на ендометриална атрофия (PE-II).
- Голяма дебелина на М-ехо, повече от половината от дебелината на матката
- Неравности и замъглени контури
- Повишена ехогенност
- Повишена звукопроводимост
- Хетерогенна вътрешна ехо структура
- Вътрешни течни включвания
- Неравномерно изтъняване на миометриума, показващо инвазия
- Течност в маточната кухина. Ехо картината на RE-II е напълно неспецифична, но този тип трябва да се подозира, ако се открият следните ехо признаци при жена с постменопаузално кървене (фиг. 28)
- Невизуализиран ендометриум
- Течност в маточната кухина.
|
По този начин, обобщавайки раздела, посветен на ехографската диагностика на ЕК, не можем да не се съгласим с B.I. Zykin, който смята, че за диагностицирането на рак на ендометриума показателят за дебелина не е определящ и заключава, че на настоящия етап трансвагиналната ехография (B-режим) се е изчерпала като метод за диагностициране на рак на ендометриума, достигайки таван на точност от 75-85%.
Доплерография за RE. Както отбелязва B.I. Zykin, с RE-I, интраендометриалният кръвен поток е открит при 100% от пациентите под формата на множество, често хаотично разположени цветни локуси (фиг. 24). Доплеровите показатели се характеризират с висока скорост и ниско съпротивление на кръвния поток (фиг. 25-27, табл. 2). Подобни данни са получени от повечето автори, занимаващи се с този проблем.
| Фигура 26 |
| Рак на ендометриума (I патогенетичен вариант) Ниско съпротивление на кръвния поток |
| Фигура 27 |
| Рак на ендометриума (I патогенетичен вариант) Висока скорост на кръвния поток |
При EC-II цветните локуси не се визуализират в проекцията на атрофиралата лигавица и ракът се разкрива само чрез забележимо увеличаване на кръвния поток в субендометриалните зони на миометриума (фиг. 28). По този начин единственият ултразвуков критерий за подозрение за злокачествено заболяване на ендометриума не е дебелината на ендометриума, а анормални цветни локуси.
Таблица 2.Показатели за интраендометриален кръвен поток при ендометриален карцином (B.I. Zykin, 2001).
Няма съмнение, че широкото използване на трансвагинална ехография и доплерография с висока разделителна способност значително ще повиши нивото на ранно откриване на ЕК и евентуално ще намали честотата на ненужните кюретажи при жени с постменопаузално кървене.
- Демидов V.N., Gus A.I. Ултразвукова диагностика на хиперпластични и туморни процеси на ендометриума В книгата: Клинично ръководство за ултразвукова диагностика / Изд. Миткова В.В., Медведева М.В. Т. 3. М.: Видар, 1997. С. 175-201.
- Демидов V.N., Zykin B.I. Ултразвукова диагностика в гинекологията // М. Медицина. 1990 г.
- Медведев M.V., Zykin B.I., Khokholin V.L., Struchkova N.Yu. Диференциална ултразвукова диагностика в гинекологията // M. Vidar. 1997 г
- Zykin B.I. Стандартизация на доплеровите изследвания в гинекологичната онкология // Дисертация за докторска степен по медицински науки. Москва. 2001. 275.P.
- Kurjak A., Kupesic S., (Ed.) Атлас на трансвагинален цветен доплер. Второ издание. // Издателска група Партенон. Ню Йорк. Лондон. 2000. P.161-178.
- Suchocki S., Luczynski K., Szymczyk A., Jastrzebski A., Mowlik R. Оценка на дебелината на ендометриума чрез трансвагинална ултразвук като метод за скрининг при ранна диагностика на рак на ендометриума // Ginekol-Pol. 1998 май., 69(5): 279-82.
- Bakour SH., Dwarakanath LS., Khan KS., Newton JR., Gupta JK. Диагностичната точност на ултразвуковото сканиране при прогнозиране на ендометриална хиперплазия и рак при постменопаузално кървене // Obstet Gynecol Scand. 1999 май., 78 (5): 447-51.
- Fistonic I., Hodek B., Klaric P., Jokanovic L., Grubisic G., Ivicevic Bakulic T. Трансвагинална сонографска оценка на премалигнени и злокачествени промени в ендометриума при постменопаузално кървене // J Clin Ultrasound. 1997 октомври, 25 (8): 431-5.
- Dubinsky TJ., Stroehlein K., Abu Ghazzeh Y., Parvey HR., Maklad N. Прогноза за доброкачествено и злокачествено заболяване на ендометриума: хистеросонографско-патологична корелация // Радиология. 1999 февруари, 210 (2): 393-7.
- Weber G., Merz E., Bahlmann F., Rosch B. Оценка на различни трансвагинални сонографски диагностични параметри при жени с постменопаузално кървене // Ultrasound Obstet Gynecol. 1998 октомври, 12 (4): 265-70.
- Olaya F.J., Dualde D., Garcia E., Vidal P., Labrador T., Martinez F., Gordo G. Трансвагинална сонография при ендометриален карцином: предоперативна оценка на дълбочината на миометриална инвазия в 50 случая // Eur J Radiol. 1998 февруари, 26 (3): 274-9.
- Медведев В.М., Чекалова М.А., Терегулова Л.Е. Рак на ендометриума // В книгата: Доплерография в гинекологията. Под редакцията на Zykin B.I., Медведев M.V. 1-во издание. М. РАВУЗДПГ, Реално време. 2000. стр. 145-149.
- Li S., Gao S. Диагностична стойност на оценката на ендометриума чрез трансвагинална ултрасонография при пациенти с постменопаузално кървене // Chung Hua Fu Chan Ko Tsa Chih. 1997 януари, 32 (1): 31-3.
- Briley M., Lindsell DR. Ролята на трансвагиналния ултразвук при изследване на жени с постменопаузално кървене // Clin Radiol. 1998 юли, 53 (7): 502-5.
- Криси Х., Бар Хава И., Орвието Р., Леви Т., Бен Рафаел З. Ендометриален карцином при жена след менопауза с атрофичен ендометриум и интракавитарна течност: доклад за случай // Eur J Obstet Gynecol Reprod Biol. 1998 април, 77 (2): 245-7.
- Bedner R., Rzepka Gorska I. Диагностична стойност на събирането на течност от маточната кухина при откриване на пренеопластични лезии и ендометриален карцином при асимптоматични жени след менопауза // Ginekol Pol. 1998 май., 69 (5): 237-40.
Copyright © 2000-2006 "Искра Медицинска Корпорация", Буланов М.Н.
Всички права запазени. Никаква част от тази страница (включително текст, илюстрации и файлове) не може да бъде възпроизвеждана под никаква форма или по какъвто и да е начин без писменото разрешение на собствениците на авторските права.Според световната статистика ракът на матката е на 7-мо място сред злокачествените заболявания. Анализът на онкологичната ситуация през последното десетилетие в Русия показва постоянно нарастване на честотата на рака на ендометриума, който до 2007 г. заема 2-ро място сред всички злокачествени тумори при жените. Делът на рака на матката в структурата на заболеваемостта от злокачествени новообразувания на 100 000 жени от населението на Русия в различни региони варира от 4,5 до 22,5. Наблюдава се устойчиво нарастване на заболеваемостта от 9,8 през 1990 г. до 13,9 през 2005 г., което съответства на 3-то място по нарастване на заболеваемостта от злокачествени новообразувания. В момента нарастването на броя на новодиагностицираните случаи на рак на матката не отстъпва на това на туморите на гърдата. В страните от третия свят рискът от развитие на рак на ендометриума като цяло е по-нисък, но смъртността остава висока. В Северна Америка и Европа това заболяване е много по-разпространено, като е най-честият злокачествен тумор на женската репродуктивна система и се нарежда на 4-то място сред всички злокачествени новообразувания след рака на гърдата, белия дроб и дебелото черво. Честотата на рака на ендометриума нараства рязко на възраст между 40 и 54 години, като пикът на заболеваемостта е между 60 и 64 години. Честотата на рака на ендометриума и неговата динамика в различните страни, като се вземе предвид влиянието на миграционните процеси и възрастта, показват специфичните характеристики на заболяването и зависимостта на неговото възникване от комплекс от причини от ендо- и екзогенен характер.
Сред рисковите фактори за развитие на рак на матката се обръща внимание на ниския брой раждания или безплодие, затлъстяване, късна менопауза и захарен диабет, предимно тип 2. В повечето случаи рискът от развитие на рак на ендометриума е свързан с различни форми на ендометриална хиперплазия - 81,3%, дисфункция поради синдром на поликистозни яйчници - 25%, ендометриална полипоза - 5,3-25%, маточни фиброиди - 1,6-8%. Напоследък се наблюдава значително увеличение на локално напредналите форми на рак на ендометриума, което е свързано с неефективни първични диагностични мерки. Въпросите за изясняване на диагнозата рак на ендометриума са обект на внимателно проучване.
В патогенезата на заболяването водещо значение има теорията за прекомерната естрогенна стимулация на ендометриума, съчетана с дефицит на прогестерон. Смята се, че прекомерното излагане на естроген може да доведе до ендометриална хиперплазия, която може да прогресира до атипичен вариант и в 20-25% от случаите да премине в аденокарцином. В същото време съществуващата връзка между степента на пролиферация на ендометриума и концентрацията на естроген в кръвта се наблюдава до определена прагова стойност и дори интензивната пролиферация не във всички случаи е придружена от злокачествена трансформация на ендометриума. Откритата корелация между съдържанието на естроген и увреждането на ДНК в нормалния и злокачествения ендометриум ни принуждава да обърнем повече внимание на ролята на молекулярно-генетичните и морфологични фактори при формирането на различни видове рак на матката. Ракът на ендометриума се характеризира с хетерогенен характер, който се проявява както на нивото на рисковите фактори, така и на неговата патогенеза, което определя характеристиките на формирането на рискови групи за това заболяване.
Понастоящем за идентифициране на патология на ендометриума се използват главно диагностичен кюретаж на маточната кухина, хистероскопия и аспирационно цитологично изследване, както и радиационни диагностични методи, сред които ултразвукът (ултразвукът) е от водещо значение. Въпреки това, няма единни методологично базирани ехографски критерии за инвазивен туморен растеж. Въвеждането на нови ултразвукови технологии в програмите за интегрирано изследване на пациенти, като импулсен доплер, ултразвукова ангиография и реконструкция на триизмерно изображение, значително повиши ефективността на първичната диагностика и наблюдение на пациенти с рак на ендометриума в процеса на специфична терапия.
Целта на тази работа беше да се проучат възможностите на сложния ултразвук с помощта на цветен доплер и (и ЕК) и реконструкция на триизмерно изображение при първичната и изясняваща диагноза на рак на ендометриума.
материали и методи
Изследвахме 139 пациенти на възраст от 21 до 87 години със съмнение за рак на ендометриума в пери- и постменопаузалния период. При 34 пациенти са открити хиперпластични процеси на ендометриума, при 105 - злокачествени процеси на ендометриума. Средната възраст на пациентите с доброкачествена патология е 42,6±7,2 години, на пациентите с рак на ендометриума - 65,4±7 години. Във всички случаи е получена хистологична проверка на диагнозата.
Всички пациенти бяха прегледани цялостно чрез ултразвук, използвайки трансабдоминален (3,5 MHz конвексен сензор) и трансвагинален (6,5-7 MHz сензор) достъпи на модерни ултразвукови апарати Logiq S6 (GE, Healthcare) и Accuvix-XQ (Medison) по определена програма, използваща най-новите ултразвукови техники, включително Доплер ехография на маточните съдове, цветна циркулация и ЕК с триизмерна реконструкция на изображението. По време на трансабдоминално изследване при пациенти с пълен пикочен мехур се оценява състоянието на матката и яйчниците, определят се обемите на тялото и шийката на матката, ширината на М-ехото. По време на трансвагинален ултразвук (TVUS) са използвани доплерови измервания за измерване на кръвния поток и индекса на резистентност в маточните артерии и за оценка на интензивността на интратуморния кръвен поток. На всички етапи от изследването се определя състоянието на ендо- и миометриалната структура, тяхната връзка и хомогенност. При откриване на фокални промени се определя техният размер, степен на разпространение и връзка с околните органи и структури и се извършва сравнителна оценка на дебелината на стената на матката в областта на тумора и извън зоната на туморния фокус . Ако е възможно, точно се определят линейните и обемните параметри на тумора, яснотата на контурите му и се оценява състоянието на съседната лигавица. Основният параметър за оценка на ендометриума остава промяната в неговата дебелина. Обемът на ендометриума се използва и за най-ранна диагностика на заболяването. Неговите стойности са по-надеждни при диференциалната диагноза на рак и доброкачествени хиперпластични процеси, отколкото измерванията на ширината на ендометриума. Критериите за злокачествени ендометриални лезии са стойности на обема на ендометриума над 13 cm 3 . Това гарантира 100% чувствителност и 92% предвидимост на положителен тест при диагностицирането на рак на ендометриума.
Най-важните характеристики на ендометриалната неоплазма са степента и естеството на нейната васкуларизация, която се оценява в режим на cine-loop, за да се получи най-пълно и визуално представяне. Извършва се качествена оценка на кръвоснабдяването според броя на цветните сигнали от съдовете на неоплазмата: хиповаскуларна, умерено васкуларна, хиперваскуларна. Използвахме технология, която преобразува обемните данни в серия от последователни секции с дебелина до 0,5 mm. Целенасоченият избор на определени участъци от 3D обемни данни позволи да се изберат оптимални участъци от тялото и маточната кухина и да се оцени възможно най-точно техният размер и да се определи връзката на идентифицираните промени със състоянието на околните органи и тъкани. Технологията Volume CT View направи възможно въз основа на 3D сканиране да се оценят контурите и структурата на ендометриума, естеството на неговото кръвоснабдяване, а използването на опцията за хистограма направи възможно точното определяне на индекса на васкуларизация.
Особено внимание беше отделено на оценката на дълбочината на миометриалната инвазия, възможния преход на злокачествения процес към цервикалния канал и състоянието на регионалните лимфни възли, което беше от решаващо значение за определяне на стадия на заболяването и избора на тактика на лечение.
Резултати и дискусия
В резултат на изследването при 34 пациенти бяха идентифицирани хиперпластични процеси на ендометриума, които идентифицирахме в отделни нозологични форми, които отговарят на препоръките на СЗО. В табл Фигура 1 показва разпределението на пациентите в зависимост от морфогенезата на идентифицираните ендометриални хиперпластични процеси.
маса 1. Разпределение на пациентите според вида на ендометриалните хиперпластични процеси.
Хиперпластичните процеси на ендометриума се проявяват с нарушения на менструалния цикъл като менометрорагия, анемия от I-II степен. В случай на доброкачествена патология на ендометриума, при 24 (71,4%) пациенти, средно увеличение на дебелината на М-ехото се определя чрез ултразвук в сива скала от 14,6 ± 3,2 mm. При трансвагинална ехография жлезистата кистозна хиперплазия се определя като образуване на повишена ехогенност, хомогенна структура, с множество точкови хипо- или анехогенни включвания до 1,5 mm, понякога с ефект на акустично усилване. При атипична хиперплазия в маточната кухина се открива хетерогенна хиперехогенна солидна структура. Полипите се определят като кръгли, овални или продълговати, в някои случаи на дълга дръжка, хиперехогенни образувания с различни размери, деформиращи маточната кухина и ясно диференцирани на фона на течното съдържание на маточната кухина. На импулсен доплер режим са количествено оценени хемодинамичните показатели в маточните артерии, които са: MSS - 9,3±2,1 cm/s, индекс на резистентност - 0,56±0,05.
Използвайки техниката, цветният интратуморален кръвен поток при жлезиста кистозна хиперплазия се записва под формата на единични сигнали от съдове, разположени по периферията. При фиброгландуларни полипи се визуализира умерено изразен венозен и артериален периферен кръвоток със средни стойности на периферното съдово съпротивление. При 2 пациенти с жлезиста хиперплазия се установява изразена хиперваскуларизация на ендометриума. При атипична хиперплазия се регистрира централен и периферен интратуморален кръвен поток с умерена интензивност. При 5 пациентки с жлезисто-кистична хиперплазия и атрофичен ендометриум не е регистриран кръвоток. Характерни признаци на доброкачествена неоплазма, дори при наличие на множество полипоидни израстъци, са запазването на формата на маточната кухина, ясното дефиниране на външния контур на ендометриума и равномерното разпределение на миометриалните съдове (фиг. 1 и 2). ).
Ориз. 1. TVUS, режим на енергийно картографиране. Жлезиста кистозна ендометриална хиперплазия.

Ориз. 2. TVUS, режим на енергийно картографиране. Ендометриален полип.
Злокачествена патология на ендометриума е диагностицирана при 105 пациенти. 80% от изследваните с тази патология са на възраст от 50 до 69 години, от които 82 (78%) имат злокачествена трансформация на ендометриума, придружена от постменопаузално кървене. При преглед на пациенти със съмнение за рак на ендометриума се установява увеличение на дебелината на М-ехото до 18,1±6,7 mm. При етап Ia дебелината на М-ехото е 11,5±3,7 mm, при етап Ib - 15,8±8,4 mm, при етап Ic - 17±3,4 mm, при етап II - 21±4,1 mm, при етап III - 27± 2,0 mm, на етап IV - повече от 30 mm. Стадият на рак на матката се определя съгласно Международната класификация на рака (FIGO, 1988). В табл 2 е направено сравнение на специфичен хистотип на рак на ендометриума със стадия на заболяването.
таблица 2. Сравнение на хистотипа и стадия на рак на ендометриума.
| Хистотип на тумора | сцена | Обща сума | |||||
|---|---|---|---|---|---|---|---|
| Ia | ib | Интегрална схема | II | III | IV | ||
| Аденокарцином: | |||||||
| силно диференциран | 12 | 3 | 3 | 4 | 2 | 1 | 25 |
| умерено диференциран | 22 | 6 | 2 | 6 | 6 | 2 | 44 |
| ниска оценка | 5 | - | - | 1 | 3 | 1 | 10 |
| серозно-папиларен | 3 | - | - | 1 | 3 | 1 | 8 |
| чиста клетка | - | 1 | - | - | - | 1 | 2 |
| Жлезист плоскоклетъчен карцином | 1 | 1 | - | 2 | 1 | - | 5 |
| Саркома | 2 | - | 1 | 1 | 3 | 2 | 9 |
| акантома | 1 | 1 | - | - | - | - | 2 |
| Обща сума | 46 | 12 | 6 | 15 | 18 | 8 | 105 |
Както се вижда от табл. 2, повече от 60% от пациентите са диагностицирани с рак на матката в стадий I, като 46 пациенти имат стадий Ia. Пациентите с общи форми на злокачествени заболявания на тялото на матката са 23%. В повечето случаи (89 пациенти, 85%) е диагностициран аденокарцином с различна степен на диференциация.
В нашето проучване степента на диференциация на тумора корелира със стадия на заболяването: при силно диференциран аденокарцином процесът е ограничен главно до тялото на матката. Слабо диференцирани, серозни папиларни и светлоклетъчни аденокарциноми са отбелязани в етапи II, III и IV с разпространение на тумора извън органа. Плоскоклетъчен карцином в стадий I е диагностициран при 2 пациенти, стадий II и III - при 3. Комбинация от аденокарцином и ендометриален стромален сарком е открита при 9 пациенти, от които 5 са диагностицирани с III и IV стадий на заболяването. Основните ултразвукови признаци на рак на ендометриума по време на трансабдоминални и трансвагинални изследвания в режим B-сканиране могат да се считат за увеличаване на М-ехото, което не е типично за този пациент, неравномерност и хетерогенност на ендометриума, в допълнение, по-висока ехогенност на неговия структура като цяло или идентифицирана фокална формация в сравнение с непроменен миометриум, наличие на неравен, външен контур, проникващ в различни дълбочини. При значително локално разпространение на тумора е възможно визуализиране на хипоехогенен ръб около тумора или липса на граница между туморния фокус и миометриума. В нашето изследване ние оценихме индекса на инвазивен растеж (IGI) - определящ съотношението на обема на променения ендометриум (AVI) към обема на тялото на матката. Получените данни са представени в табл. 3. Изчисляването на тези показатели е възможно само за рак на ендометриума в I стадий, когато границата на променения ендометриум е определена доста ясно (фиг. 3).
Таблица 3. Ултразвукови параметри на матката и М-ехо при рак на ендометриума в различни стадии.
В стадий Ia обемът на ендометриума е 4,2±2,2 cm3, IIR - 11,9±4,2, в стадий Ib AIE - 8,3±4,6 cm3, IIR - 7,5±5,4 cm3, в стадий Ic AIE - 15,4±5,3 cm3, IIR - 4,3±2,9. Както е показано в таблицата. 3 данни, има ясно увеличение на обема на ендометриума и намаляване на стойностите на IRI, тъй като степента на туморна инвазия в миометриума се увеличава. За повечето пациенти с рак на ендометриума неговата локализация е характерна за фундуса на матката или един от тубарните ъгли. Туморна некроза с деформация на маточната кухина и наличие на течност в нея се определят в етапи III и IV на процеса.
Въз основа на литературни данни идентифицирахме три основни типа растеж на инвазивен рак на ендометриума.
- Развитие на множество силно диференцирани туморни огнища на фона на хиперпластични процеси на целия ендометриум.
- Развитие на едно силно диференцирано туморно огнище, заобиколено от хиперпластична лигавица върху къс участък.
- Развитие на един умерено или слабо диференциран туморен фокус на фона на атрофична лигавица.
Екзофитната форма на туморен растеж се открива в 15% от случаите. Екзофитният туморен растеж се характеризира с липса на деформация на маточната кухина, ясни граници на ендо- и миометриума или откриване на образуване в лумена на маточната кухина. В 85% от случаите се отбелязва ендофитна форма на растеж с инвазия в миометриума. Нарушаването на целостта на хипоехогенния ръб при рак на ендометриума е специфичен признак на инвазия в миометриума. Ендофитният туморен растеж води до асиметрия и деформация на маточната кухина. При дълбок инфилтративен процес вторият вариант е отбелязан в 30%, третият вариант - в 70% от случаите. Ултразвукът дава възможност ясно да се определи формата на туморния растеж само в началните стадии на заболяването. При рак на ендометриума в стадий Ia, в случай на ултразвук в B-режим, се определя хомогенна хиперехогенна структура на средното М-ехо, а при 69,5% се разкрива хетерогенност на структурата на ендометриума поради включвания с кръгла форма, с гладки, в някои случаи неясни контури, повишена ехогенност, чийто среден размер е 6,3±3,8 mm. Границите на ендометриума при всички наблюдения в I стадий на заболяването се определят като ясни и равномерни.
Таблица 4. Хемодинамични показатели при доброкачествена и злокачествена патология на ендометриума.
Забележка. * - Р<0,05
Според нашите наблюдения беше възможно да се разграничат 1-ви и 2-ри тип развитие на тумора в обичайния В-режим само при 10 пациенти. В други случаи, поради значително локално разпространение на тумора, тези разлики не са определени. При дълбок инфилтративен процес в етапи III и IV на заболяването дебелината на М-ехото надвишава 27,0 mm. Границите между тумора и миометриума във всички случаи са неясни, контурите са неравни, а при 61 (58,0%) пациентки границите на тумора не са дефинирани до външния контур на матката. Структурата на М-ехото в 30,3% от случаите е хомогенна хиперехогенна, в 20,1% - хомогенна хипоехогенна и в 50% - хетерогенна, предимно хиперехогенна. Ехоструктурата на тумора също може да има различна ехогенност: в 44,6% от случаите е хомогенна хиперехогенна, в 10,4% - хомогенна хипоехогенна, в 45,0% - смесена.
Оценихме количествените показатели на хемодинамиката, извършени с помощта на маточните артерии и туморните съдове. В табл Таблица 4 показва сравнително описание на хемодинамичните параметри при доброкачествени и злокачествени ендометриални патологии.
Както се вижда от представените данни, хемодинамиката на регионалния кръвен поток при рак на ендометриума е придружена от тенденция за увеличаване на скоростта на кръвния поток в съдовете на матката и статистически значимо намаляване на индекса на периферното съпротивление в туморните съдове , което може да характеризира активността на интратуморния кръвен поток. MSS в маточните артерии зависи от обема на тялото на матката, което може да бъде свързано с наличието на фиброиди и естеството на туморната васкуларизация. Показателите за интратуморален кръвен поток и IR не са статистически зависими от хистотипа на рака на ендометриума.

Ориз. 4. TVUS, режим на енергийно картографиране. Рак на ендометриума стадий Ia. По протежение на предната стена на матката се идентифицира огнище на хиперваскуларизация.

Ориз. 5.

Ориз. 6. TVUS, цветен доплер, надлъжно сканиране. Етап Iа рак на ендометриума. Инфилтративно образуване на хиперехогенна структура в областта на фундуса на тялото на матката с намалена васкуларизация.
При анализиране на естеството и степента на васкуларизация на рака на ендометриума, оценени с помощта на режимите CDC и EC, бяха определени различни варианти за интраендометриален кръвен поток. Патологична васкуларизация на ендометриума се наблюдава при 92 (87,6%) пациенти с рак на ендометриума. В други случаи, дори при наличието на характерни ултразвукови признаци на злокачествени лезии, интратуморният кръвен поток не се визуализира с използваните техники. В случай на тумор на тялото на матката са идентифицирани три основни варианта на кръвоснабдяване (A, B, C) и се наблюдава определена зависимост на модела на цветна циркулация и ЕК от етапите и идентифицираните форми на туморен растеж. Интензитетът на кръвния поток в ендометриума и туморния възел, определен в режимите CDC и EC, зависи от вида на туморния растеж и може да бъде най-ясно представен в режим cine-loop. Зоните на туморния кръвен поток се откриват при рак на ендометриума в повече от 90% от случаите (фиг. 4-8).
Установено е, че вариант А е характерен за етап Ia: с инфилтрация на миометриума до дълбочина 5 mm, която се определя в 33,8% от случаите и се характеризира с неравномерно увеличаване на интраендометриалния кръвен поток поради локално увеличение на брой цветни петна с различен интензитет на цвета, при липса на цветни локуси в субендометриалната зона. Същият вариант е характерен за екзофитната форма на растеж с интратуморален тип неоваскуларизация.

Ориз. 7. TVUSI, CDC. Етап IV рак на ендометриума. Хиперваскуларизация на образуването на хетерогенна структура в областта на левия маточен ъгъл. Определя се ендометриалният и интратуморният кръвоток.

Ориз. 8. TVUS, комбинация от B-режим и режим на енергийно картографиране. IV стадий на рак на ендометриума. Огнище на хиперваскуларизация по протежение на задната стена на матката с хиперваскуларен ендометриален кръвоток.
Вариант Б (47,6%) се характеризира с общо увеличение на интраендометриалния кръвен поток поради голям брой хаотично разположени цветни локуси, с едновременно локално увеличаване на броя на цветните сигнали в субендометриалната зона. В 27,5% от случаите се установява умерена васкуларизация на тумора, съчетана с богата васкуларизация на миометриума. Този вариант е идентифициран при 78,3% от пациентите със смесена форма на рак на ендометриума.
Вариант С (19,6%) се характеризира с леко увеличение на интраендометриалния кръвен поток със значително общо увеличение на броя на цветните сигнали в субендометриалната зона. Този вариант е характерен за ендофитната форма на растеж (92,5%) и е придружен от интензивен интра- и перитуморален кръвоток.
Въпреки че не е установена пряка връзка между тежестта на туморния кръвен поток и стадия на заболяването, както и степента на диференциация, наличието на откриваема зона на неоваскуларизация съответства на по-висок стадий на процеса. При пациенти с добре диференциран аденокарцином се наблюдава хиповаскуларен и умерен кръвоток в ендометриума.
Неоваскуларизация на патологичния процес не е регистрирана в 12,4% от случаите. Причината за това може да бъде отстраняването на малък тумор в резултат на предварителен диагностичен кюретаж на маточната кухина и при силно диференциран аденокарцином, възникнал на фона на атрофия на ендометриума.
Чрез конструиране на фронтални равнини стана възможно по-точно да се определи състоянието на ендометриума и да се установи неговата асиметрия. Дезорганизираният съдов модел, разкрит чрез триизмерна ангиография в обемен блок, при комбиниране на режими на сканиране, беше важен допълнителен признак на злокачествени ендометриални лезии. Най-точни резултати при оценката на степента на инвазия на ендометриалния карцином се постигат с помощта на триизмерна реконструкция в режим на ултразвукова ангиография (фиг. 9-11). миометриум в съседство с туморните области.

Ориз. 9.Ултразвук, извършен с помощта на технологията за многослоен преглед. Използвайки срезове слой по слой, става възможно точно да се определи структурата на ендометриума и неговата васкуларизация.
Възможностите на ултразвуковия метод за диагностициране на рак на ендометриума имат своите ограничения поради факта, че хиперпластичните процеси и началните стадии на заболяването нямат специфични диференциално-диагностични характеристики. Съпътстващото маточно кървене с образуването на фибрин усложнява идентифицирането на области на удебеляване на ендометриума. Известни трудности възникват при определяне на дълбочината на миометриална инвазия в началните стадии на рак на ендометриума в границите до 5 mm, както и при съпътстваща аденомиоза. Ултразвукът не определя точно обема на раковите лезии при жени с големи и множество субмукозни миоматозни възли, които деформират маточната кухина.

Ориз. 10. TVUS, режим на енергийно картографиране. Ултразвук, извършен с помощта на технологията за наклонен изглед. 3D обемните данни ни позволяват да изясним състоянието на ендометриума и естеството на ендометриалната и субендометриалната васкуларизация.

Ориз. единадесет.Режим на многоравнинна реконструкция. Обемен КТ изглед. 3D данните ви позволяват да определяте обемите възможно най-точно.
заключения
Ултразвуковото изследване с импулсен доплер, цветен доплер, енергийно картографиране и реконструкция на триизмерно изображение е високоинформативен метод за неинвазивна уточняваща диагностика на ендометриална патология. Получените резултати показват високата ефективност на използваните методи за диференциална диагностика на доброкачествени и злокачествени процеси. Ултразвуковата ангиография и реконструкцията на триизмерно изображение при рак на ендометриума помагат да се получи допълнителна и много важна информация за характеристиките на туморния процес, дълбочината на туморна инвазия в миометриума и естеството на откритата неоваскуларизация позволява да се прогнозира скоростта на туморен растеж.
Използването на съвременни ултразвукови технологии позволява да се решат проблемите на интранозологичната диагностика на рака на ендометриума на напълно ново качествено и количествено ниво, както и да се наблюдават пациентите в процеса на специфично лечение.
Литература
- Давидов М.И., Аксел Е.М. Статистика на злокачествените новообразувания в Русия и страните от ОНД през 2005 г. // Бюлетин на Руския онкологичен изследователски център на име. Н.Н. Блохин RAMS. 2007. Т. 18.
- Урманчеева А.С., Тюляндин С.А., Моисеенко В.М. Практическа онкогинекология (Избрани лекции) // М.: Издателство. "Том център" 2008. 400 стр.
- Ашрафян Л.А., Харченко Н.В., Огрызкова В.Л. и др.. Съвременни принципи на първична и изясняваща диагностика на рак на ендометриума // Практическа онкология. 2004. Т. 5. № 1.
- Демидов V.N., вт. A.I. Ултразвукова диагностика на хиперпластични и туморни процеси на ендометриума // Ed. Миткова В.В., Медведева М.В. Клинично ръководство за ултразвукова диагностика, 3 тома, М.: Видар. 1997. стр. 120-131.
- Капустина I.N., Сидорова A.N., Саранцев A.N. Цветно доплерово картографиране при диагностицирането на рак на ендометриума // Sonoace international. Руска версия. Vol. 9, 2001. стр. 34-39.
- Максимова Н.А. Някои аспекти на ултразвуковата диагностика на рак на ендометриума // Ултразвукова диагностика в акушерството, гинекологията и педиатрията. 1999. № 3. С. 196-201.
- Столярова И.В., Минко Б.А., Сиразитдинов Б.Р. Възможностите на триизмерната ултразвукова ангиография при специфична диагностика на ендометриален карцином // 19 Международен конгрес за лечение на рак, Париж, 5-8 февруари; 2008. С. 255-256.
- Гаженова В.Е. Ултразвукова диагностика в гинекологията // М.: "MEDpress-inform". 2005. 264 стр.
- Титова В.А., Харченко Н.В., Столярова И.В. Автоматизирана лъчева терапия на женската репродуктивна система // М.: Медицина. 2006. 160 с.
- Gruboeck K., Jurkovic D., Lawton F. et al. Диагностичната стойност на измерванията на дебелината и обема на ендометриума чрез триизмерен ултразвук при пациенти с постменопаузално кървене // Ultrasound Obstet. Гинекол. 1996. № 8. С. 272-276.
- Столярова И.В., Минко Б.А., Лисянская А.С. и др.. Възможности на съвременните ултразвукови техники за изясняване на диагнозата рак на ендометриума // Международен конгрес Невски радиологичен форум "Нови хоризонти" 7-10 април 2007 г. Санкт Петербург, стр. 364-365.
- Чекалова М.А., Зуев В.М. Ултразвукова диагностика в гинекологичната онкология // М.: Издателство. къща "Руски лекар". 2004. 92 стр.
- Терегулова А.Е. Трансвагинална ехография с използване на цветно доплерово картографиране при пациенти с рак на ендометриума // Ултразвукова диагностика. 1996. № 4. С. 21-23.
- Kurjak A., Shalan H., Sosic A. и др. Ендометриален карцином при жени в постменопауза: оценка чрез трансвагинална цветна доплерова ултрасонография // Am. J. Obstet. Гинекол. 1993. V. 169. P. 1597-1603.








