Un mūsu aknas strādāja vairāk, saņemot no mums papildu holesterīnu un papildu stresu.
Iespējams, ir grūti atrast mūsu ķermenī citu orgānu, kas varētu izturēt triecienu dienu no dienas un izturēt visu, ko mēs ēdam un dzeram. Filtrē asinis, ražo žulti, bez kuras nesadalītos tauki, neitralizē toksīnus. Un pat tad, kad viņa jūtas slikti, viņa praktiski nedod SOS signālus. Aknās gandrīz nav nervu galu, tāpēc par problēmām ar tām uzzinām pārāk vēlu.
Tauki tiek nogulsnēti aknu šūnās. Laika gaitā šo saliņu kļūst arvien vairāk, tās daļēji aizvieto normālas aknu šūnas (hepatocītus). Tā rezultātā palielinās aterosklerozes risks, cukura diabēts, aknu ciroze.
Šo diagnozi dzird gandrīz katrs otrais cilvēks, kas ir vecāks par 40, kas ierodas uz kārtējo ultraskaņu.
Protams, tas nav īpaši patīkami, bet jums nevajadzētu būt sarūgtinātam. Aknas spēj pašatjaunoties un ir gatavas jums piedot gadu desmitiem ilgušo neuzmanību pret tām. Vienkārši no šī brīža jums jākļūst par viņas draugu.
Aknas spēj pareizi veikt savas funkcijas, pat ja tikai 20% to šūnu paliek “formā”.
Aknas ir galvenā ķermeņa bioķīmiskā laboratorija. Pateicoties aktīvam aknu darbam, asinis un organisms kopumā tiek pastāvīgi attīrīts no dažādiem toksīniem, kancerogēniem un atkritumiem. Ķermenī nav nevienas funkcijas, kurā nebūtu iesaistītas aknas!
Aknām ir daudz dažādu funkciju. Nosauksim dažus no tiem:
Ogļhidrātu metabolisms (glikozes uzkrāšanās un sadalīšanās);
Hormonālā vielmaiņa (hormonu attīrīšana);
Enzīms utt.
Turklāt aknas ir mūsu ķermeņa galvenais uztura speciālists, jo tā uzturēšana nepieciešamais līmenis asinīs ir daudz vitamīnu un mikroelementu, kurus aknas, ja tās tiek piegādātas pārmērīgi ar pārtiku, uzkrājas, un, ja tās ir nepietiekamas, izdalās asinīs.
Aknas ir arī galvenā organisma imunoloģe, kas apgādā čaklo imūnsistēmu ar svarīgākajām lietām – aminoskābēm un olbaltumvielām imūnglobulīnu, interferona un antivielu sintēzei.
Ja dažās aknu šūnās dažādu iemeslu dēļ ir veikta taukainā deģenerācija, tad tiek traucēta ne tikai atlikušo aknu šūnu spēja ražot žulti. Tiek traucēta arī asins attīrīšana no toksīniem, holesterīna un kancerogēniem. Un tas noved pie citām tikpat bīstamām slimībām. Biežāk rodas akūti iekaisuma slimības, hroniskas pasliktinās, aktīvi attīstās asinsvadu ateroskleroze, attīstības iespējamība onkoloģiskās slimības. Tajā pašā laikā, samazinoties dienā sintezētās žults daudzumam, tiek traucēta aknu spēja absorbēt pārtikā esošos A, E, D vitamīnus un daudzus makro un mikroelementus, kas ar žulti nonāk organismā no zarnām. Un ar tādu šķietami nekaitīgu aknu stāvokli kā taukainā hepatoze deģeneratīvie procesi aktīvi notiek citos orgānos un audos. Jo īpaši imunitāte samazinās.
Īpaši jārūpējas par aknām, jo... Tieši šis orgāns ražo visvairāk organismam nepieciešamo vielu, nodrošina atjaunošanās procesus, neitralizē kaitīgās vielas, sintezē urīnvielu, imūnās vielas, olbaltumvielas, glikozi, holesterīnu, asins recēšanas faktorus, kā arī attīra organismu no netipiskām šūnām, kas var veidot audzējus.
Šis ir orgāns, kas veic atjaunošanas darbu un var pats atjaunoties. Mūsdienās ir pierādīts, ka laba aknu darbība nodrošina normālu sirds un asinsvadu darbību, jo regulē holesterīna līmeni asinīs, kas savukārt uztur tīrus asinsvadus, normālu asinsspiedienu, labu garastāvokli, lielisku atmiņu un ilgu, laimīga dzīve bez slimības ēnas.
Uzņēmums Argo piedāvā plašu hepatoprotektīvo zāļu izvēli, kuru pamatā ir dabīgas sastāvdaļas, kas pēc sava sastāva ir vispiemērotākās cilvēka ķermenim.
Gepatosols ir Sibīrijas auga Solyanka kholmovoy ekstrakts, kas ir populārs Sibīrijas un Tibetas tautas medicīnā.
Hepatosols ir indicēts akūtu hepatītu (galvenokārt zāļu, toksisko, alkoholisko), hronisku hepatītu, dažādu etioloģiju taukainu hepatozi, hronisku holecistītu un aknu cirozes sākuma stadiju. Zāles palīdz praktiski optimizēt aknu, aizkuņģa dziedzera, kuņģa-zarnu trakta un nieru funkcijas. veseliem cilvēkiem, kā arī strādājot ar aknām kaitīgiem faktoriem.
Reishi-Kan ir Krievijas Zinātņu akadēmijas Sibīrijas filiāles Citoloģijas un ģenētikas institūta fundamentāla attīstība.
Satur reishi sēņu ekstraktu, steviozīdu, koncentrētus dzērveņu, smiltsērkšķu ekstraktus, šķiedrvielas (dzērveņu un smiltsērkšķu milti, diždadža saknes, kviešu graudu čaumalas).
Šis produkts ir efektīvs profilakses līdzeklis rūpniecisko pilsētu iedzīvotājiem, cilvēkiem, kas strādā bīstamās nozarēs un lieto potenciāli hepatotoksiskas zāles. Reishi-Kan ne tikai novērš vielmaiņas, strukturālās un funkcionālie traucējumi aknās, bet arī aptur patogēnās zarnu mikrofloras augšanu disbakteriozes laikā, mazina stresa izpausmes, atjauno spēkus, nomierina centrālo nervu sistēmu.
Preparāta Reishi-Kan lietošanai profilaktiskos nolūkos un aknu slimībām nav kontrindikāciju, izņemot atsevišķu sastāvdaļu nepanesamību. Steviozīda kā cukura aizstājēja klātbūtne ļauj izmantot Reishi-Kan aknu slimībām, kas saistītas ar cukura diabētu.
Litovit O ir efektīvs bioloģiski aktīvs uztura bagātinātājs, ko izstrādājusi AS NPF nov. Papildus spēcīgajām hepatoprotektīvajām īpašībām, sērijas “Litovit” uztura bagātinātāji paātrina bojāto aknu šūnu un pat apkārtējo limfmezglu atjaunošanos, aizstājot vietas ar atmirušajām šūnām ar normāliem veseliem hepatocītiem. Litovit-O efektivitāte šajā situācijā ir ievērojami augstāka nekā citiem Litovit sērijas uztura bagātinātājiem.
Ir pierādīta Litovit izteiktā iedarbība toksiskā un infekciozā hepatīta gadījumā:
aknu izmēra samazināšanās. astenoveģetatīvā sindroma likvidēšana, normalizēšana funkcionālie testi aknas, samazinot bilirubīna līmeni, atvieglojot intoksikācijas simptomus, samazinot dzeltes smagumu, samazinot pacientu uzturēšanās ilgumu slimnīcā.
Pectolact ir unikāls želejveida produkts. Laktuloze sadala olbaltumvielu sadalīšanās produktus, ar kuriem aknas nevar tikt galā; pektīns ir nepieciešams labvēlīgas mikrofloras atražošanai
Aknu šūnu aizsardzībai jābūt balstītai uz iekaisuma procesa atvieglošanu, normālas žults aizplūšanas nodrošināšanu, membrānu saglabāšanu un šūnu metabolisma normalizēšanu. Īpaši šiem nolūkiem Apifarm ir izstrādājis uztura bagātinātāju Hepatoleptin.
"Hepatoleptīns" satur propolisa un ārstniecības augu ekstraktus - timiānu, nemirstīgo ziedu, kliņģerīšu un kukurūzas zīda. Pateicoties tiem, hepatoleptīnam ir spēja aizsargāt aknu šūnas no infekcijām un skābekļa radikāļiem, samazināt iekaisuma procesu, iedarboties ar holērisku iedarbību, uzlabot žults ķīmisko sastāvu un novērst žultsakmeņu veidošanos. Bioloģiski aktīvs uztura bagātinātājs.
Hepal – ieteicams kā flavoligānu, glicirizīnskābes avots un kā papildu C vitamīna avots, lai aizsargātu aknas. Satur mežrozīšu ekstraktu, piena dadžu augļu ekstraktu, lakricas saknes ekstraktu, pantohematogēnu.
Uztura bagātinātājā “Hepal” esošā mežrozīšu ekstrakta maigais holerētiskais efekts uzlabo vielmaiņas procesus aknās, samazina holesterīna līmeni asinīs un efektīvi neitralizē iekaisuma procesus un veicina aknu šūnu atjaunošanos. Pateicoties augstajam C vitamīna saturam, tai ir tonizējoša iedarbība un tas stiprina imūnsistēmu.
Rūpējieties par savām aknām jau no mazotnes: galvenās briesmas, ar kurām saskaras jūsu aknas
Vai esat zīdainis un domājat, ka tāpēc jūsu aknas nav apdraudētas? Vienalga kā ir. Uzziniet par asimptomātiskām briesmām, kas jebkurā brīdī var sagraut jūsu veselību.
Pēc pirmās meitas piedzimšanas es sapratu, ka ir pienācis laiks mainīties. Nodzīvojis līdz 32 gadu vecumam bez īpašām raizēm, kādu dienu es atklāju, ka esmu atbildīgs par citu cilvēku. Mums jāsāk uzraudzīt mūsu veselību vai vismaz jāsagatavo plāns gadījumam, ja mūsu ķermenis nopietni sabojājas. Man šķita, ka otrais variants ir kaut kā vienkāršāks, un es nolēmu apdrošināt savu dzīvību.
Bet tad izkapts negaidīti uzkrita uz akmens. Saskaņā ar apdrošināšanas kompānijas noteikumiem pirms polises saņemšanas man bija jāiziet pilna medicīniskā pārbaude. Lielākā daļa rādītāju, piemēram, asinsspiediens, holesterīna līmenis un glikozes līmenis plazmā, bija pieļaujamās robežās, taču viens punkts apdrošinātājiem lika izbrīnā pacelt uzacis: dažu aknu enzīmu saturs manās asinīs bija pat 3 reizes lielāks. nekā parasti.
Jūtot nemierīgu raižu un pārsteiguma sajaukumu, es devos pie terapeita. Viņš saspieda manu labo pusi un bija neapmierināts: aknas patiešām bija nedaudz palielinātas. Atkārtoti testi apstiprināts paaugstināts aknu enzīmu līmenis. Terapeita spriedums mani neiepriecināja: šī simptomu kombinācija var liecināt par aknu bojājumiem. Aknu bojājumi? "Kas pie velna?" - tas ir viss, ko es varēju izspiest no sevis, atbildot.
Ikviens zina, ka mūsu aknas visbiežāk cieš no infekcioza hepatīta un alkohola. Turpmākie testi hepatītu izslēdza no saraksta, bet varbūt es tiešām pārmērīgi lietoju alkoholu? Viens vai divi alus dienā, kā arī reizēm burbona glāze naktī — es nekad agrāk nedomāju, ka tas ir daudz. Īpaši salīdzinoši jaunam vīrietim, kurš vairāk vai mazāk vada veselīga dzīve: Es skrienu 3 km 3 reizes nedēļā, desertā ēdu augļus, nevis maizītes ar krējumu un pat dažreiz palutinu savu ķermeni ar dažiem vārītu brokoļu ziediem.
Tiesa, uztura speciālistei man joprojām ir ko pārmest: es neliedzu sev picu un burgerus, kā arī kartupeļus un tako. Es sveru zem simts svara, un mans ķermeņa masas indekss (svars kg dalīts ar augumu metros kvadrātā) ir 32, kas nozīmē, ka man ir ne tikai liekais svars, bet arī aptaukošanās. Bet šie kilogrami nekad nav radījuši veselības problēmas, mani testi līdz nesenam laikam vienmēr ir bijuši tuvu ideālam, un galvenais, es jūtos lieliski. Pat pēc tam, kad terapeits radīja aizdomas, ka man ir “aknu bojājumi”.
Kuru tieši? Tauku infiltrācija. Viņš izdomāja spilgtu attēlu, lai man ar pirkstiem izskaidrotu šo diagnozi: "Iedomājieties, ka aknu šūnās veidojas tauku nogulsnes, un, kad tās uzbriest, tas kļūst kā sablīvēta skvoša kaviāra kunkuļi." Ārsts nepārprotami nesaudzēja ne manu iztēli, ne mani. Šķiet, viņš nolēma, ka nedēļas laikā es izdzeru tālu no 3-4 alkohola standarta porcijām (1 alkohola standarta porcija ir 330 ml alus vai 40 ml stiprā alkohola), kā norādīts anketā, bet daudz vairāk. Nevienam nepatīk alkoholiķi, kuri pārvērš savas aknas par foie gras.
Dažas nedēļas vēlāk, sēžot gastroenterologa kabinetā, kā mantru sev atkārtoju, ka alkohola porcija dienā ir veselīgi, kaut kur lasīju. Bet slaidais, sirmais ārsts pievīla manas cerības. Sākumā viņš ilgi jautāja par to, kā manai mātei ir diabēts, un pēc tam nolēma precizēt: "Vai jūs ēdat maizi, rīsus, cukuru, kartupeļus, makaronus?" Jā, protams. Es arī elpoju skābekli un dzeru ūdeni.
Pat nejūtot vēderu, gastroenterologs atsēdās krēslā un teica, ka ir gatavs derēt, ka manas problēmas nav tieši saistītas ar alkohola lietošanu. Tauki manās aknās nokļuva (fakts, ko vēlāk apstiprināja ultraskaņa un biopsija), bet ne no alkohola, tāpēc manu slimību sauc par bezalkoholisko tauku aknu slimību vai saīsināti NAFLD. Citiem vārdiem sakot, es staigāju pa pasauli ar speķa gabalu labajā pusē.
1. Normālas aknas
Vesels orgāns ir tieši tāds: plāns un skaists
2. Cirozes aknas
Daudz rētaudu, kas novērš normālu asinsriti aknās
3. Aknas ar taukainu infiltrāciju
Viņas šūnās ir sakrājies daudz tauku
Kāpēc viņa ir tik slikta
Mani pārsteidza vairāk nekā mana diagnoze, ka trīs maniem draugiem nesen tika diagnosticēts tieši tas pats. Iedomājieties, veseli, maz dzeroši vīrieši vecumā no 30 līdz 35 gadiem, un šeit jums ir taukainas aknas. Kāpēc?
Jo mēs visi esam resni. Saskaņā ar pētījumu, kas publicēts American Journal of Epidemiology, NAFLD sastopams 19% amerikāņu, un vīrieši vecumā no 30 gadiem ir vadošie šajā statistikā. Rietumeiropas valstīs un Krievijā situācija ir līdzīga. Eksperti šo slimību tieši saista ar divu riska faktoru kombināciju: aptaukošanos un iedzimtu noslieci uz diabētu (tātad gastroenterologa interese par manas mātes diabētu). Ārsti jau sen runā par aptaukošanās epidēmiju Rietumeiropā un Amerikā, un tā strauji uzņem apgriezienus.
Piemēram, saskaņā ar Apvienotās Karalistes valdības pasūtīto prognozi ir sagaidāms, ka līdz 2050. gadam šajā valstī 60% visu pieaugušo vīriešu neatgriezeniski zaudēs savu dzimumlocekli. Starp citu, tauku infiltrāciju aknās var izraisīt arī citi iemesli, piemēram, saindēšanās, ko izraisa pārmērīga alkohola lietošana. Bet jūs labi apzināties šos riskus pat bez mums; Krievijā visi vīrieši, kas vecāki par 15 gadiem, zina par alkoholisko cirozi.
Kāpēc tauki aknās ir bīstami? Mariana Lazo, kura Džona Hopkinsa universitātē (ASV) studē NAFLD, stāsta, ka 30% amerikāņu aknās ir tauku nogulsnes, ko izraisa liekais svars, taču ne visiem ir veselības problēmas. NAFLD diagnoze parasti tiek veikta tikai tad, ja ķermeņa tauku procentuālais daudzums pārsniedz 5–10%. No šī brīža, ja neveiksit nekādas darbības, tauku daudzums aknās palielināsies, līdz attīstīsies bezalkoholisks steatohepatīts (NASH), tas ir, nākamais taukaino aknu slimības posms, kurā parādās neatgriezeniskas izmaiņas, piemēram, rētas. orgānā. Turklāt aknu iznīcināšanas procesu ir grūti mainīt, un, visticamāk, jūs saskarsities ar cirozi un pēc tam pilnīgu svarīgā orgāna mazspēju. Turklāt NAFLD var izraisīt aknu vēža attīstību, kas ir praktiski neārstējama.
Galvenās taukaino aknu briesmas ir tādas, ka no NAFLD diagnozes līdz NASH diagnozei parasti paiet gadi, ja ne gadu desmiti, kuru laikā jums praktiski nav simptomu. Bieži vien vienīgā netiešā NAFLD attīstības pazīme, tāpat kā manējā, ir paaugstināts noteiktu aknu enzīmu līmenis asinīs.
Es domāju, ka ir pienācis laiks, kad jums vajadzētu saņemt labas ziņas. Mums par laimi cilvēka aknas ir slavenas ar savām spējām atjaunoties. Tātad, saskaņā ar Lazo teikto, ja pacientiem ar NAFLD izdodas zaudēt 5% svara, viņu aknu enzīmu testa rezultāti ievērojami uzlabojas. Tāpēc, ārstējot NAFLD, daudzi ārsti iesaka pacientiem diētu ar zemu vienkāršo ogļhidrātu saturu, īpaši, piemēram, miltus un cukuru (aknas var pārstrādāt liekos ogļhidrātus savos tauku nogulsnēs). Turklāt svarīgas ir fiziskās aktivitātes – saskaņā ar pētījumu, kas publicēts žurnālā Gut, spēka treniņi 3 reizes nedēļā 8 nedēļas samazināja aknu tauku daudzumu par 13%, paātrinot vielmaiņu taukaudos. Ir arī pētījumi, kas liecina, ka aerobikas treniņi ir arī efektīvi cīņā pret NAFLD.
Neatliec uz rītdienu
Ņemot vērā to, ka man bija agrīna NAFLD stadija, gastroenterologs bija pārliecināts, ka es varētu novērst bojājumus, ko esmu nodarījis aknām. Viņš ieteica man turpināt parasto skriešanu un krasi samazināt ogļhidrātu uzņemšanu. Es aizstāju parasto maizi ar pilngraudu maizi, baltos rīsus ar brūnajiem rīsiem, pilnībā izslēdzu frī kartupeļus un kartupeļu biezeni, kā arī lielāko daļu ceptu un treknu ēdienu, lai mēģinātu samazināt savu kopējo kaloriju patēriņu. Savu vietu manā šķīvī ieņēma salāti un lapu zaļumi.
Rezultātā sešu mēnešu laikā es zaudēju apmēram 20 kg. Bet, lai arī cik apmierināts es būtu ar skalas rādījumiem, sešu mēnešu miesas nogalināšanas galvenajam rezultātam vajadzēja būt aknu enzīmu līmenim asinīs, kas bija nokrities līdz normai. Un tā arī notika. Es atviegloti uzelpoju. Es gribētu tam izbeigt, bet tad jūs nezināsit visu patiesību par NAFLD (ja jums ir apnicis šis saīsinājums, varat izmantot frāzi “aknu steatoze” - tā tas ir).
Kā zināms, filmās viss beidzas ar kāzām, bet iekšā īsta dzīve Viss tikai sākas ar viņu. Ak, mani tik ļoti iedvesmoja ātrā uzvara pār aknu taukiem, ka sāku atgriezties savā vecajā dzīvesveidā: atļāvos desertiem, sāku palīdzēt meitai tikt galā ar frī kartupeļiem no Happy Meals. Un kā, jūsuprāt, manas aknas reaģēja uz manas diētas relaksāciju? Tieši tā, jaunu tauku rezervju uzkrāšanās.
Vēl pēc sešiem mēnešiem man atkal palielinājās aknu enzīmu līmenis asinīs. Gastroenterologs, redzot izmeklējumus, teica, ka man vienreiz būs jāmaina diēta uz veselīgu. Godīgi sakot, es garīgi apņēmos to darīt. Tas ir labāk, nekā izaudzēt vēderā kaut ko, kas izskatās pēc sablīvēta skvoša kaviāra kamola, kas turklāt pēc 10 gadiem mani, visticamāk, novedīs pie kapa.
Dodiet viņai pareizo ēdienu, uzmaniet viņu, un viņa netraucēs jums visu atlikušo mūžu.
Ja jums ir liekais svars vai pat aptaukošanās, zaudējiet šīs papildu mārciņas. Pārmērīgs ķermeņa tauku daudzums, cita starpā, izraisa paaugstinātu insulīna rezistenci, kas tiek uzskatīts par vienu no galvenajiem faktoriem NAFLD attīstībā.
Jūsu mērķis Pārliecinieties, ka jūsu ķermeņa masas indekss nekad nepārsniedz 23. Taivānas zinātnieki ir atklājuši, ka tas ir ideāls rādītājs tiem, kas vēlas izvairīties no aknu steatozes. Piemēram, tieši šāds ķermeņa masas indekss būs puisim, kura augums ir 178 cm un svars 73 kg.
Jūsu aknas sadala taukus un ogļhidrātus, kurus jūs tik ļoti mīlat, kā arī izvada toksīnus. Citiem vārdiem sakot, viņai ir smags darbs, lai neitralizētu visas šķebināšanās, ar kurām jūs piebāzaties pie galda. Mainot diētu, atvieglojiet šo uzdevumu aknām.
Tavs mērķis: apmierini izsalkumu ar riekstiem, sēklām, zaļajiem dārzeņiem un treknām zivīm. Zinātnieki no Dienvidkorejas ir atklājuši, ka šī diēta veiksmīgi aizsargā vīriešus no NAFLD, jo šajos pārtikas produktos ir daudz K vitamīna, folijskābes un omega-3. taukskābes.
Regulāras fiziskās aktivitātes palīdzēs jūsu ķermenim sadedzināt lipīdus tieši asinīs, pirms tie sasniedz aknas.
Jūsu mērķis: dodieties uz sporta zāli vismaz trīs reizes nedēļā. Dienvidkorejā un Apvienotajā Karalistē veiktie pētījumi liecina, ka tas ir minimums, kas var pasargāt jūs no bezalkoholiskās taukaino aknu slimības. Un nav svarīgi, kādus vingrinājumus jūs veicat, galvenais ir veikt vismaz dažus.
4. Neslīcini viņu vīnā
Jūsu aknas cieš, ja esat resns un ēdat treknu pārtiku. Arī aknas cieš, ja jūs piepildāt savu ķermeni ar alkoholu, un tām nav laika tikt galā ar alkohola sadalīšanās produktiem. Un, ja jūs esat resns, ēdat treknu pārtiku un dzerat pārāk daudz, jūs esat pilnīgi sajukuši.
Paracetamols ieteicamās devās ir labs pretsāpju līdzeklis, taču to nedrīkst ļaunprātīgi izmantot. ASV, saskaņā ar Pārtikas un zāļu administrācijas (FDA) datiem, tā ir paracetamola pārdozēšana. galvenais iemesls akūta aknu mazspēja.
Jūsu mērķis: Patērējiet ne vairāk kā 4000 mg dienā. Un neaizmirstiet, ka paracetamols ir ne tikai neatkarīga narkotika, bet arī daļa no daudzām citām zālēm zāles piemēram, tie, kas mazina saaukstēšanās simptomus.
Pirmais ir izaugsme un attīstība bērnībā un pusaudža gados.
Otrais ir nobriešana trešajā desmitgadē un ceturtās sākumā, kad muskuļu un ķermeņa blīvums turpina palielināties un fiziskās aktivitātes sasniedz maksimumu.
Trešais periods sākas no ceturtās desmitgades vidus, kad muskuļu masai ir tendence samazināties, bet tauku masai ir tendence palielināties (īpaši vēdera). Šo procesu aktivitāte ir atkarīga no uztura un fiziskās aktivitātes modeļa.
Ceturtais periods sākas piektajā dzīves desmitgadē. Raksturīgs ar vienmērīgu muskuļu masas un fiziskā spēka samazināšanos.
No ceturtā sākuma:
- liesa masa un citu ķermeņa sastāvdaļu masas, ieskaitot saistaudus, kolagēnu (piemēram, ādā un kaulos), imūnsistēmas šūnas, transportu un citus proteīnus;
- kopējā kālija saturs, un šis process ir nesamērīgs salīdzinājumā ar olbaltumvielu samazināšanos, jo skeleta muskuļu masa, kas satur lielāko kālija koncentrāciju, samazinās vairāk nekā citu proteīnu saturošu audu masa;
- kaulu minerālvielu blīvums (pamazām). Process sākas 30 gadu vecumā abiem dzimumiem, sievietēm menopauzes laikā tas ir īpaši aktīvs. Attīstās osteoporoze un palielinās kaulu lūzumu risks. Šis risks palielinās ar nepietiekamu uzturu, D vitamīna un kalcija deficītu, fizisko aktivitāti un pazeminātu dzimumhormonu līmeni;
- ūdens saturs organismā (par 17% sievietēm no trešās līdz astotajai dzīves desmitgadei, par 11% vīriešiem tajā pašā laika periodā), kas atspoguļo intracelulārā ūdens samazināšanos, jo ūdens saturs ārpusšūnu telpā saglabājas. nemainīgs;
Gremošanas sistēma novecošanas laikā
Ķermeņa fizioloģisko novecošanos pavada nopietna gremošanas sistēmas orgānu funkcionāla un organiska pārstrukturēšana. Šo procesu sauc par “involūciju”, un tas sākas ilgi pirms cilvēka bioloģiskās vecuma iestāšanās. Jau 40–50 gadu vecumā gremošanas orgānos notiek funkcionālas izmaiņas, kas ļauj kuņģa-zarnu traktam pielāgoties mainīgajiem dzīves apstākļiem un organisma aktivitātēm. Pēc tam funkcionālās izmaiņas iegūst neatgriezenisku organisku raksturu.
Izmaiņas gremošanas orgānu darbībā gados vecākiem un seniliem cilvēkiem, kā likums, dabā attīstās lēnām un notiek individuāli dažādos dzīves periodos. Involucionāro procesu attīstības ātrums ir atkarīgs no cilvēka dzīvesveida jaunā un vidējā vecumā. Vissvarīgākais nosacījumsĶermeņa agrīnas novecošanās profilakse ir pareiza uztura (gan racionāla, gan terapeitiska).
Mutes dobums
Vājums attīstās gadu gaitā košļājamie muskuļi, audu atrofiju, kā arī dziļus involutive procesus mutes gļotādā un in cietie audi augšā un apakšžoklis, aktivitāte samazinās siekalu dziedzeri. Košļājamo muskuļu vājums, pārtikas samitrināšanās ar siekalām un zobu skaita samazināšanās gadu gaitā būtiski pasliktina pārtikas pārstrādi. mutes dobums. Tas apgrūtina rīšanu un samazina siekalu baktericīdo iedarbību. Mutes dobumā notiek pūšanas procesi, radot apstākļus iekaisuma parādībām.
Barības vads
Gados vecākiem un seniliem cilvēkiem raksturīgi progresējošas barības vada muskuļu un gļotādas atrofijas procesi. Tas noved pie diskinēzijas attīstības. Līdz ar diskinēziju tiek novērotas arī spazmas, kas apgrūtina bolus izvadīšanu.
Aizkuņģa dziedzeris
Involutive izmaiņas aizkuņģa dziedzerī sastāv no progresējošas orgānu audu atrofijas, sekrējošo šūnu aizstāšanas ar saistaudiem. Gremošanas intensitāte un kvalitāte pasliktinās: notiek nepilnīga olbaltumvielu, tauku un ogļhidrātu sagremošana. Organisms nespēj uzņemt nesagremotas pārtikas sastāvdaļas, un rezultātā veidojas hronisks būtisku uzturvielu deficīts. Ja rodas deficīta apstākļi, piemēram, hipovitaminoze, imūndeficīts, tiek provocēti daudzu ķermeņa funkciju traucējumi.
Aknas
Vesela cilvēka organismā novecošanās process maz ietekmē aknu funkcionālo stāvokli. Aknas ilgu laiku adekvāti piedalās visos ķermeņa dzīvības atbalsta mehānismos. Tomēr vecumdienās tā asins piegādes intensitāte pakāpeniski samazinās un hepatocītu skaits samazinās. Tā rezultātā vecumdienās olbaltumvielu sintēze aknās samazinās par vairāk nekā 30%. Pasliktinās arī aknu funkcijas, kas ir atbildīgas par tauku, ogļhidrātu, pigmentu, ūdens un elektrolītu metabolismu. Tomēr, ja nav hronisku aknu slimību, neskatoties uz funkcionālās aktivitātes samazināšanos, aknas turpina nodrošināt visu ķermeņa audu un sistēmu darbību atbilstošā līmenī.
Zarnas
Būtiskākās izmaiņas līdz ar novecošanos notiek zarnu kustībā. Attīstās zarnu muskuļu atrofija, pasliktinās zarnu apgāde ar asinīm. Tā rezultātā pasliktinās tā satura kustība caur zarnām. Īpaši intensīvi šīs izmaiņas notiek cilvēkiem ar mazkustīgu dzīvesveidu un nepilnvērtīgu uzturu ar šķiedrvielu deficītu.
Gados vecākiem un gados vecākiem cilvēkiem pakāpeniski pasliktinās zarnu gļotādas gremošanas un uzsūkšanās spēja. Ar zarnu bārkstiņu atrofiju samazinās gremošanas un pārtikas sastāvdaļu uzsūkšanās aktivitāte. Tā sekas ir olbaltumvielu, vitamīnu, minerālvielu un mikroelementu trūkums organismā.
Vecumā zarnās attīstās disbiotiskas izmaiņas. Šis patoloģisks process ir atkarīgs no vairākiem faktoriem. Pirmkārt, skābuma samazināšanās dēļ kuņģa sula un žults sintēzes samazināšanās aknās, samazinās kuņģa-zarnu trakta aizsardzība pret iekļūšanu zarnās patogēni mikrobi, sēnītes, vīrusi un citi zarnu mikrofloras pārstāvji. Otrkārt, ar nepietiekamu uztura šķiedrvielu uzņemšanu uz novājinātas fona motora aktivitāte Zarnās tiek radīti apstākļi, kas veicina savas mikrofloras nomākšanu un veicina svešu mikroorganismu vairošanos. Zarnu disbiozes attīstību pavada fermentācijas procesi ar liela daudzuma gāzu veidošanos un zarnu cilpu uzpūšanos. Pārmērīga gāzu veidošanās izraisa pastiprinātu aizcietējumu, uzsūkšanos zarnās un pārmērīga toksīnu daudzuma iekļūšanu asinīs, ko traucētajai zarnu baktēriju florai nav laika neitralizēt. Augsta šo vielu koncentrācija asinīs izraisa sirds un asinsvadu sistēmas traucējumus gados vecākiem cilvēkiem (paaugstinās asinsspiediens, palielinās stenokardijas lēkmju biežums, sirds aritmijas utt.), veicina vispārējās labklājības, garastāvokļa, miega un izraisīt paaugstinātu nogurumu.
Lasi arī:
Kurš tiek uzskatīts par vecu un kurš par vecu
Kad sākas vecumdienas
Aicinājums uz ilgmūžību
Kā sinepes darbojas pret matu izkrišanu?
MATU KOPŠANA 3 GADUS VECAM BĒRNAM
Ceļa locītavas artrozes cēloņi, simptomi, pakāpes un ārstēšana
A grupas vitamīni pārtikas produktos
BĒRNU EĻĻA MASĀŽAI. BĒRNU MASĀŽAS EĻĻA
2018 Esi vesels. Vietnes administrācija nav atbildīga par sekām un rezultātiem, ko lasītāji var saņemt pēc mūsu vietnē esošās informācijas izmantošanas! Konsultējieties ar savu ārstu. Visas autortiesības uz materiāliem pieder to attiecīgajiem īpašniekiem
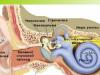
Aknu anatomija
Aknas ir viens no lielākajiem cilvēka iekšējiem orgāniem. Tās masa, kā likums, ir 1200–1500 g - apmēram viena piecdesmitā daļa no visa ķermeņa masas.
Šim orgānam ir nozīmīga loma cilvēka ķermeņa vielmaiņas procesos, tajā notiek milzīgs skaits dažādu bioķīmisko reakciju.
Aknu atrašanās vieta un struktūra
Aknas atrodas tieši zem diafragmas - augšējā labajā daļā vēdera dobums. Tās apakšējo malu sedz ribas, un augšējā mala ir vienā līmenī ar sprauslām. Aknu anatomija ir tāda, ka gandrīz visu to virsmu klāj vēderplēve, izņemot daļu aizmugurējās virsmas, kas atrodas blakus diafragmai. Mainot ķermeņa stāvokli, mainās arī aknu atrašanās vieta: in horizontālā stāvoklī tas paceļas, un vertikāli, gluži pretēji, tas krīt.
Ir ierasts atšķirt aknu labo un kreiso daivu, kuras augšpusē atdala falciforma saite un zemāk ar šķērsenisko rievu. Ir vērts atzīmēt, ka labā daiva ir daudz lielāka nekā kreisā, to var diezgan viegli sajust labajā hipohondrijā. Kreisā daiva atrodas tuvāk vēderplēves kreisajai pusei, kur atrodas aizkuņģa dziedzeris un liesa.
Anatomija ir noteikusi, ka šim orgānam parasti ir neasa augšējā un asa apakšējā mala, kā arī augšējā un apakšējā virsma. Augšējā (diafragmas) atrodas zem diafragmas labā kupola, bet apakšējā (viscerālā) atrodas blakus citiem iekšējiem orgāniem. Blakus aknu apakšējai virsmai atrodas žultspūslis, kas darbojas kā žults tvertne, ko ražo aknu šūnas (hepatocīti).
Paši hepatocīti veido prizmatiskas formas aknu strukturālās un funkcionālās vienības, ko sauc par aknu lobulām. Cilvēkiem šīs daivas ir diezgan vāji atdalītas viena no otras, starp tām iziet žults kapilāri, kas sakrājas lielākos kanālos. No tiem veidojas kopējais aknu kanāls, kas pāriet kopējā žultsvads, caur kuru žults nonāk divpadsmitpirkstu zarnā.
Galvenās funkcijas
Aknas tiek uzskatītas par diezgan daudzfunkcionālu orgānu. Pirmkārt, tas ir liels gremošanas dziedzeris, kas, kā jau minēts, ražo žulti. Bet aknu loma cilvēka organismā neaprobežojas ar to. Tas veic arī šādas svarīgas funkcijas:
- Neitralizē visa veida organismam svešas vielas (ksenobiotikas), piemēram, alergēnus, toksīnus un indes, pārvēršot tos mazāk toksiskos vai vieglāk izvadāmos savienojumos.
- Izvada no organisma liekos vitamīnus, mediatorus, hormonus, kā arī starpposma un gala toksiskos vielmaiņas produktus (fenolu, amonjaku, acetonu, etanolu, ketonskābes).
- Piedalās gremošanas procesos, nodrošinot glikozi organisma enerģijas vajadzībām. Aknas arī pārvērš dažus enerģijas avotus (aminoskābes, brīvos taukus, glicerīnu, pienskābi un citus) glikozē. Šo procesu sauc par glikoneoģenēzi.
- Papildina un saglabā ātri mobilizētās enerģijas rezerves, regulē ogļhidrātu vielmaiņu.
- Uzglabā un uzglabā dažus vitamīnus. Aknas satur taukos šķīstošos vitamīnus A, D, ūdenī šķīstošo vitamīnu B12 un mikroelementus, piemēram, varu, kobaltu un dzelzi. Tas arī metabolizē vitamīnus A, B, C, D, E, K, PP, kā arī folijskābi.
- Piedalās augļa hematopoētiskajos procesos, sintezē virkni asins plazmas proteīnu: globulīnus, albumīnus, vitamīnu un hormonu transporta proteīnus, antikoagulantu un asins koagulācijas sistēmu proteīnus utt. Pirmsdzemdību attīstības laikā aknas tiek iesaistītas hematopoēzes procesā.
- Sintē holesterīnu un tā esterus, lipīdus un fosfolipīdus, lipoproteīnus un regulē lipīdu metabolismu.
- Sintezē žultsskābes un bilirubīnu, kā arī ražo un izdala žulti.
- Tā ir liela asins daudzuma uzglabāšanas vieta. Ja rodas šoks vai tiek zaudēts ievērojams daudzums asiņu, aknu asinsvadi sašaurinās un asinis izdalās vispārējā asinsvadu gultnē.
- Sintezē hormonus un fermentus, kas iesaistīti pārtikas transformācijas procesā divpadsmitpirkstu zarnā un citās tievās zarnas daļās.
Asins piegādes iezīmes
Šī dziedzera asins piegādes anatomija un īpašības noteiktā veidā ietekmē dažas tā funkcijas. Piemēram, detoksikācijai ar asinīm aknās no zarnām un liesas caur vārtu vēnu nonāk toksiskas vielas un mikroorganismu atkritumi. Pēc tam portāla vēna sadalās mazākās starplobulārās vēnās. Arteriālās asinis, kas ir piesātinātas ar skābekli, iet caur aknu artēriju, kas rodas no celiakijas stumbra un pēc tam sazarojas starplobulārajās artērijās.
Šie divi galvenie asinsvadi ir iesaistīti asins apgādes procesā, tie iekļūst orgānā caur padziļinājumu, kas atrodas dziedzera labās daivas apakšā un tiek saukts par aknu portālu. Lielākais asins daudzums (līdz 75%) tajā nonāk caur vārtu vēnu. Katru minūti pa asinsvadu gultne Orgāns izlaiž apmēram 1,5 litrus asiņu, kas ir ceturtā daļa no kopējās asins plūsmas cilvēka organismā minūtē.
Reģenerācija
Aknas ir viens no nedaudzajiem orgāniem, kas spēj atjaunot savu sākotnējo izmēru, pat ja tiek saglabāti tikai 25% audu. Pēc būtības notiek reģenerācijas process, bet pats par sevi tas ir diezgan lēns.
Ieslēgts Šis brīdisŠī orgāna reģenerācijas mehānismi nav pilnībā izprotami. Savulaik tika uzskatīts, ka tā šūnas attīstās tāpat kā embrija šūnas. Bet paldies mūsdienu pētījumi, bija iespējams noskaidrot, ka atjaunojošo aknu izmērs mainās, palielinoties šūnu augšanai un skaitam. Šajā gadījumā šūnu dalīšanās apstājas, tiklīdz dziedzeris sasniedz sākotnējo izmēru. Visi faktori, kas to varētu ietekmēt, joprojām nav zināmi, un tos var tikai minēt.
Cilvēka aknu atjaunošanās process ilgst diezgan ilgu laiku un ir atkarīgs no vecuma. Jaunībā tas tiek atjaunots vairākas nedēļas un pat ar nelielu pārsvaru (apmēram 110%), bet vecumdienās atjaunošanās notiek daudz ilgāk un sasniedz tikai 90% no sākotnējā izmēra.
Ir zināms, ka individuālās īpašības organismi ietekmē to, cik intensīva notiek reģenerācija. Tāpēc ar nepietiekamu atveseļošanos pastāv iespēja attīstīt hronisku iekaisumu un turpmākus orgāna darbības traucējumus. Šādā gadījumā ir jāstimulē reģenerācija.
Ar vecumu saistītas izmaiņas
Atkarībā no vecuma šī dziedzera anatomija un iespējas mainās. Bērnībā funkcionālie rādītāji ir diezgan augsti un pakāpeniski samazinās līdz ar vecumu.
Jaundzimušam bērnam aknām ir masa. Maksimālo izmēru tas sasniedz apmēram pēc gada, pēc tam aknu masa sāk nedaudz samazināties. Kā jau minēts, gadu gaitā samazinās arī atveseļošanās spējas. Turklāt samazinās globulīnu un jo īpaši albumīnu sintēze. Bet tas nekādā veidā neizjauc audu uzturu un onkotisko asinsspiedienu, jo gados vecākiem cilvēkiem samazinās plazmas olbaltumvielu sadalīšanās procesa intensitāte un citi audi. Izrādās, ka arī vecumā aknas apmierina organisma vajadzību pēc plazmas olbaltumvielu sintēzes.
Tauku vielmaiņa un aknu glikogēna kapacitāte sasniedz maksimumu agrīnā vecumā un diezgan nedaudz samazinās vecumdienās. Aknu ražotās žults daudzums un tās sastāvs mainās dažādos organisma attīstības periodos.
Kopumā aknas ir maznovecojošs orgāns, kas var pienācīgi kalpot cilvēkam visu viņa dzīvi.
Kurš teica, ka nav iespējams izārstēt smagas aknu slimības?
- Ir izmēģinātas daudzas metodes, bet nekas nepalīdz.
- Un tagad esat gatavs izmantot jebkuru iespēju, kas sniegs jums ilgi gaidīto labsajūtu!
Efektīva aknu ārstēšana pastāv. Sekojiet saitei un uzziniet, ko ārsti iesaka!
Veiciet testu, lai noskaidrotu, cik uzņēmīgi esat pret aknu slimībām
Vai nesen esat piedzīvojis tādus simptomus kā slikta dūša, grēmas vai pārmērīga atraugas?
Vai pēc fiziskas slodzes jūtat sāpes labajā pusē zem ribām?
Nav noslēpums, ka novecošanās procesā organismā notiek nopietnas izmaiņas, kas noteikti ietekmē daudzu orgānu un sistēmu darbību. Šajā gadījumā viena vai otra orgāna slimība šādos apstākļos noritēs atšķirīgi.
Aknu darbības iezīmes vecumdienās
Būtiski mainās asins piegāde aknām, jo īpaši samazinās asins plūsma un asins daudzums, kas iet caur orgānu. Šīs izmaiņas var nopietni ietekmēt zāļu aktivitāti un iznīcināšanas ātrumu. Tas ietekmē aknu rezistences samazināšanos pret zāļu iedarbību, kas bieži izraisa toksisku hepatītu.
Papildus samazinātai asins plūsmai samazinās autoimūna reakcija pret audzēja šūnas un antigēni, kas nāk no ārējā vide. Papildus šim pavājinātas imūnās atbildes iemeslam gados vecākiem cilvēkiem šāda reakcija var rasties regulējošo T šūnu samazināšanās rezultātā.
Samazinās dažādu orgānu rezerves funkcijas, un tas savukārt samazina tolerances līmeni pret aknu slimībām. Tagad parunāsim par pašām slimībām.
Vīrusu hepatīts A
Slimības gaita ir pašierobežojošs process, bet gados vecākiem cilvēkiem šī infekcija bieži noved pie aknu slimības pazīmju attīstība aknu šūnu mazspējas veidā ar dažāda veida koagulopātijas un dzeltes attīstību. Turklāt komplikācijas bieži attīstās pankreatīta, žults stagnācijas un ascīta veidā, tas ir, brīvā šķidruma uzkrāšanās vēdera dobumā.
Kad vīrusu hepatīts A rodas gados vecākiem cilvēkiem, vienmēr ir augstāks mirstības un hospitalizācijas līmenis, salīdzinot ar citām vecuma kategorijām.
Gados vecākiem cilvēkiem noteikti jāveic imunoprofilakse, vakcinējoties, īpaši pirms došanās uz vietām, kur vīrusu hepatīts A ir endēmisks.
Vīrusu hepatīts B
Gados vecākiem cilvēkiem vīrusu hepatīts B ir reti sastopams, jo inficēšanās risks šai vecuma grupai ir diezgan zems. Neskatoties uz to, šīs slimības un vīrusu hepatīta C reģistrācijas rādītāji pansionātos ir augsti, jo ir paaugstināts riska faktoru blīvums:
- iespējama zobu suku maiņa;
- izmantojot atkārtoti lietojamas šļirces (lai gan mūsdienās tas notiek ārkārtīgi reti);
- atkārtoti lietojamu skūšanās piederumu izmantošana;
- dzimumakts.
Aknu slimības klīniskās pazīmes praktiski neatšķiras no slimības simptomiem jaunākiem cilvēkiem. Bet gados vecākiem cilvēkiem slimības progresēšanas ātrums ir daudz augstāks nekā jauniešiem.
Vīrusa B hepatīta uzliesmojuma gadījums pansionātā parādīja, ka gandrīz 60% cilvēku, kas vecāki par 65 gadiem, attīstījās hroniska infekcijas forma. Šis rezultāts var būt sekas samazinātai imūnās atbildes reakcijai pret infekcijas izraisītāju ieviešanu. Papildu riska faktori aknu cirozes un vēža attīstībai ir vīriešu dzimums un vecāka gadagājuma vecums.
Ārstēšana ar nukleozīdu zālēm gados vecākiem cilvēkiem ir tikpat efektīva kā mazu pacientu ārstēšanā. Interferona iedarbība gados vecākiem pacientiem ir nedaudz mazāka.
Vīrusu hepatīts C

Aknu struktūra
Vīrushepatīta C sastopamība ir atkarīga no vecuma, jo tā pārnešana galvenokārt notiek ar asins pārliešanu, intravenozu narkotiku lietošanu, militāro dienestu, hemodialīzi, tetovēšanu un citām medicīniskām procedūrām.
Vecums, nevis slimības ilgums, tika uzskatīts par riska faktoru aknu fibrozes un aknu vēža attīstībai. Vecumā aknu enzīmu līmeņa bioķīmiskie rādītāji bieži paliek normāli. Tomēr mēs atzīmējam, ka gados vecākiem cilvēkiem fibroze attīstās daudz ātrāk un nav atkarīga no enzīmu līmeņa asins serumā.
Hepatocelulārā karcinomas attīstība inficētiem pacientiem biežāk notiek gados vecākiem cilvēkiem nekā jauniešiem.
Vīrusu hepatīts Nopietna un grūti ārstējama slimība. Tās adekvātai terapijai ir izstrādāti pretvīrusu kursi, tostarp pegilētais interferons un ribavirīns. Protams, zāles ir smagas, un blakusparādības ir izplatītas gados vecākiem cilvēkiem. Dažiem gados vecākiem pacientiem slimība progresē un kļūst hroniska, jo blakusparādības liek atteikties no ārstēšanas sākuma stadijā.

Vīrusu hepatīts E
E hepatīta vīruss ir visizplatītākais Rietumu valstīs. Ir pierādījumi, ka 15% asins donoru, kas jaunāki par 60 gadiem, tika konstatētas antivielas pret vīrusu, bet vēl vairāk - 25% donoru, kas vecāki par 60 gadiem.
Autoimūnas aknu slimības
Gados vecākiem pacientiem autoimūnais hepatīts un primārā biliārā ciroze mūsdienās ir diezgan plaši izplatīta. Tomēr visi laboratorijas testi un ārstēšana praktiski neatšķiras no šo patoloģiju ārstēšanas jauniem pacientiem. Apskatīsim divas autoimūnas aknu slimības:
- Piektdaļai pacientu pēc 60 gadu vecuma saslimst ar autoimūnu hepatītu, un slimības progresēšana ir strauja un reizēm cilvēkam negaidīta. Tā attīstās ascīts un ciroze, kas nav bagāti ar simptomiem. Ja šādus pacientus ārstē ar kortikosteroīdiem, atbildes reakcija uz terapiju ir pozitīva. Vecāka gadagājuma cilvēkiem ir piecas reizes mazāk neefektīvas ārstēšanas gadījumu nekā jauniešiem, un mirstības rādītāji ir ievērojami zemāki. Bet, neskatoties uz šīm priekšrocībām, ar ārstēšanu tieši saistītu komplikāciju skaits ir lielāks gados vecākiem cilvēkiem. Starp komplikācijām mēs īpaši izceļam lūzumu risku.
- Primārā biliārā ciroze. Ja parādās šāda veida aknu slimības pazīmes jaunībā, prognoze vecumdienās ir nelabvēlīga. Ja slimība rodas vecumā virs 65 gadiem, tā progresē lēnāk un prognoze ir vieglāka. Ir divi slimības veidi. Vienam ir asimptomātiska gaita īpatnība, bet otrajam ir izteikta gaita smagi simptomi un bioķīmiskās izmaiņas. Galvenās zāles primārās biliārās cirozes ārstēšanai ir ursodeoksiholskābe, kas ir diezgan droša un tai ir maz blakusparādību.

Alkohola aknu slimība
Vecāka gadagājuma cilvēku vidū ir augsts pārmērīgas alkohola lietošanas biežums. Saskaņā ar Lielbritānijā veikto pētījumu aptuveni 6% gados vecāku cilvēku bija problēmas ar alkohola lietošanu. No tiem 12% vīriešu un 3% sieviešu dzēra stipri un bieži.
Alkohola aknu slimība gados vecākiem pacientiem attīstās lēnāk nekā jaunākiem cilvēkiem. Ja pacientam ir arī vīrusu hepatīts C, slimības progresēšana paātrinās vairākas reizes.
Bezalkoholiskā taukaino aknu slimība (NAFLD)
Aknu slimības pazīmesŠis tips rodas galvenokārt vidējā un vecumā. NAFLD bieži izraisa nezināmas etioloģijas cirozi. Šajā gadījumā vecums ir predisponējošs faktors aknu fibrozes un nāves attīstībai.
Mēs arī atzīmējam, ka gados vecākiem cilvēkiem ir papildu riska faktori, kas veicina NAFLD attīstību. Tas ir aptaukošanās, diabēts, arteriālā hipertensija, paaugstināts lipīdu līmenis asinīs. Slimības klīniskais iznākums pasliktinās dabisko organisma novecošanās procesu dēļ.
Zāļu izraisīts aknu bojājums
Nav šaubu, ka vecāks vecums būs riska faktors šīs patoloģijas attīstībai, jo gados vecāku cilvēku uzņēmība pret zāļu blakusparādībām ir daudz augstāka nekā citu vecuma grupu cilvēkiem.
Gados vecāki pacienti, kas vecāki par 75 gadiem ar zāļu izraisītu hepatītu, tiek hospitalizēti daudz biežāk. Šo patoloģisko stāvokļu sastopamības biežums ir izskaidrojams ar to, ka gados vecāki cilvēki lieto daudzus medikamentus vienlaicīgu slimību ārstēšanai.

Aknas ir neticami sarežģīta ķermeņa “ķīmiskā laboratorija”, kas vienlaikus ir atbildīga par gremošanas, asinsrites un vielmaiņas procesiem. Starp uzdevumiem, ko tā risina, viens no galvenajiem ir toksisko vielu (indes, toksīni, alergēni) filtrēšana un neitralizācija. Lai cik dīvaini tas nešķistu mūsdienu progresīvajā pasaulē, cilvēki pastāvīgi tiek pakļauti toksisku vielu iedarbībai. Pirmkārt, toksiskas vielas nonāk mūsu organismā no ārējās vides. Un mēs nerunājam par kaut kādu sabotāžu vai rupju drošības noteikumu pārkāpšanu zonā paaugstināts risks. Dzīve lielajās pilsētās (un arī vidējās) ir pastāvīgs toksīnu uzbrukums. Turklāt toksiskās vielas nonāk cilvēka organismā kopā ar pārtiku (indes, piemēram, konservanti, biezinātāji un garšas aizstājēji, pārtikas piedevas) vai veidojas tieši organismā. Kur? Piemēram, no viena un tā paša ēdiena, ja to ēda pārmērīgi.
Toksīni iekļūst aknās kā daļa no asinīm un “iestrēgst” tajās, it kā filtrā. Asinis atstāj aknas jau attīrītas un veselas. Kā ar aknām? Tās uzdevums ir neitralizēt toksīnus un nodrošināt to izvadīšanas procesu no organisma.
Bet aknas ir atbildīgas arī par citiem procesiem. Pateicoties aknām, veidojas žults, kas piedalās pārtikas sagremošanā, A, E, D, K vitamīnu uzsūkšanā un dažu daļu izvadīšanā. kaitīgās vielas(Skatīt iepriekš). Vissvarīgākā aknu darbības joma ir vielmaiņa. Konkrēti, aminoskābju vielmaiņa un olbaltumvielu veidošanās (kas nepieciešamas darbam imūnsistēma), ogļhidrātu un tauku metabolisms, līdzdalība vīriešu un sieviešu dzimuma hormonu apmaiņā. Nepārtraukto aknu “pienākumu” sarakstā ir arī vielmaiņas nodrošināšana, holesterīna līmeņa kontrole, asins ražošana un sarecēšana.
Vecuma krīze
Veselas un jaunas aknas viegli tiek galā ar visiem sev “uzliktajiem” uzdevumiem, un pat nepieciešamības gadījumā ir gatavas strādāt ārpus plāna. Taču ar vecumu slodze, īpaši pārmērīga slodze uz aknām sāk apgrūtināt. Un tas ir saistīts ne tik daudz ar pašu aknu nogurumu vai vājumu (aknas kopumā ir salīdzinoši lēni “novecojošs” orgāns), bet gan ar kumulatīvo efektu - pastiprinošām izmaiņām dzīvesveidā, palielinātām slodzēm (precīzāk, samazināšanos). atpūtas fāze), kaitīgās iedarbības ilgums un nepārtrauktība vidi kādā brīdī sasniedz savu kritisko masu.
Galu galā mūsu dzīves ceļa sākumā mēs diezgan ilgu laiku piekopjam pareizāku dzīvesveidu. Pat pieaugušā vecumā visi pašaizsardzības mehānismi ir ieslēgti. Mūsu uzturs lielākoties ir veselīgs un pareizs (nevēlama pārtika mūsu ieradumos iekļūst pakāpeniski, nejauši, laužot stereotipu par piesardzību pret to). Mēs vairāk guļam (mūsu miegu neapgrūtina ilgstošas rūpes), biežāk atpūšamies, esam pakļauti mazākam stresam un vairāk pozitīvisma. Jaunība tiecas uz spilgtiem, bet īslaicīgiem eksperimentiem (nakts ballītes, pirmais alkohols...), vecums jau ir ieradumu noslogots. Un bieži, diemžēl, kaitīgi. Mainās izvēlnes preferences. Tas arvien vairāk satur kaitīgas sastāvdaļas (taukaini un cepti ēdieni, ātrās ēdināšanas ēdieni, soda un alkohols). Esam nervozāki, uzņemamies atbildību nevis par sevi, bet arī par mīļajiem (ģimeni, bērniem). Mazāk guļam, saīsinātu atvaļinājumu apvienojot ar ikdienas problēmu risināšanu vai īslaicīgu nepilnas slodzes darbu.
Un turklāt mēs, diemžēl, slimojam arvien biežāk. Imunitāte samazinās, slimības kļūst hroniskas ar vecumu. Tas nozīmē, ka palielinās zāļu slodze uz aknām. Arvien biežāk tiek lietoti medikamenti ar ievērojamu toksicitāti, un pagarinās to lietošanas periods, ko pastiprina blakusparādības.
Aknām kļūst grūtāk ar to visu tikt galā.
Grūtāk tikt galā ar asins attīrīšanas uzdevumu - ar vecumu asins plūsma caur aknām samazinās, asinis, pilnībā nenokļūstot aknās, sāk iet pa alternatīviem ceļiem, turpinot saturēt nefiltrētus toksīnus. Organismā uzkrājas ķīmiskās vielas un smagie metāli, kas izraisa dažādas slimības un saindēšanos.
Ar vecumu ir samazinājums vielmaiņas procesi, samazinās proteīnu sintēzes procesu aktivitāte, detoksikācijas funkcijas, un aknu hepatocītu – daudzfunkcionālo aknu šūnu – enerģija. Aknu spēja regulēt holesterīna un žultsskābes līmeni parasti palēninās. Pamazām aknas zaudē savu spēju atjaunoties – pašatveseļošanās procesu. No vienas puses, pavājinās aknu žults sekrēcijas sistēma. Toksīni nosēžas un uzkrājas žults ceļā, bloķējot brīvu žults plūsmu, tā sabiezē, sacietē un pārvēršas akmeņos. Žults stagnācijas dēļ aknās tie sāk vairoties kaitīgie mikroorganismi izraisot iekaisumu. No otras puses, toksīni, uzkrājušies aknās, liek tām ražot vairāk žults nekā parasti. Pārmērīga žults iekļūst asinsritē un izplatās visā ķermenī.
Sākot jau no nobriedis vecums, cilvēka aknās notiek vairākas strukturālas izmaiņas. Pēc piecdesmit gadiem tas sākas ļoti lēna kontrakcija aknu masa, un, sākot no četrdesmit pieciem gadiem, samazinās kopējais hepatocītu skaits. Slimības un patoloģijas progresē.
Ko darīt?
Rūpējieties par aknām jau no mazotnes. Jums nevajadzētu gaidīt šo izšķirošo brīdi, kad pašām aknām ir nepieciešama ārstēšana. Labāk ir iepriekš konsultēties ar ārstu. Ne jau neatliekamās medicīniskās palīdzības dēļ, bet atbalstošas terapijas nolūkos, tā teikt - profilaktiskā režīmā.
Lai palīdzētu aknām, kuras ir spiestas rūpēties par bojāto šūnu atjaunošanu, un lai tās nodrošinātu ar “būvmateriālu”, ārsti bieži izraksta hepatoprotektoru kursu - šo zāļu iedarbība ir tieši vērsta uz aknu šūnu nostiprināšanu. un uzlabot savas darbības procesu. Mūsdienu hepatoprotektoru funkcionējošā viela, piemēram, “Progepara”, tiek iegūta no jaunu buļļu aknām. Mūsdienu medicīna dod priekšroku kompleksiem hepatoprotektoriem, kas satur svarīgākos elementus - holīnu, cisteīnu un mioinozītu, kā arī mikroelementus ar hepatoprotektīvu iedarbību - magniju, cinku, hromu un selēnu. Šādas zāles normalizē insulīna līmeni asinīs, atjauno enerģijas metabolismu, darbojas kā antioksidanti un aizsargā aknas no toksisko vielu iedarbības.
Palīdzēt aknām ir sarežģīts uzdevums. Lietojot uzturošos medikamentus, jādod priekšroka veselīgam uzturam, kura pamatā ir zema tauku satura, sautēti un cepti ēdieni. Protams, nevajadzētu aizrauties ar alkoholu (stingri jāizslēdz tabakas smēķēšana), pavadīt vairāk laika tīrā, svaigā gaisā, piespiest sevi atpūsties un no visa spēka koncentrēties uz pozitīvām emocijām.
Mēs dažreiz kaut ko svarīgu atlikām uz vēlāku laiku, pārliecībā, ka joprojām varam to paveikt. Nav acīmredzamas problēmas – nekas nav jārisina. Bet aknas ir unikāls orgāns tādā nozīmē, ka tajās praktiski nav nervu galu. Tas nozīmē, ka viņa "nepateiks", ja ar viņu kaut kas nav kārtībā, līdz viņa nesāks nopietni slimot. Nepalaid garām šo mirkli un esi vesels!
Īpaša uzmanība tiek pievērsta aknās notiekošajiem procesiem, kur tiek virzītas glikozes, eksogēno īso ķēžu taukskābju, taukaudos sintezēto endogēno taukskābju, brīvā holesterīna un holesterīna, kā arī oksiholesterīna plūsmas. Savukārt aknas izdala TG, brīvo holesterīnu un EK, ko saista apoproteīns B-100 VLDL, glikozē un žultī. Aknas veido galvenos glikozes krājumus glikogēna veidā. Glikozes, FA un holesterīna plūsmas aknās ir cieši saistītas vienā vielmaiņas mezglā. Līdzsvarotas plūsmas attiecības tiek regulētas šūnu un kodola membrānas receptoru un transkripcijas faktoru līmenī, kas kontrolē galveno gēnu ekspresiju, kas kontrolē šo substrātu metabolismu.
Glikozes iekļūšanu aknās regulē insulīns, kas mijiedarbojas ar IR. Glikoze šūnā tiek transportēta ar Glut 2 transporteri. Caur Glut 2 tiek panākts ātrs līdzsvars starp ārpusšūnu un intracelulāro glikozes koncentrāciju. Lai iedarbinātu regulēšanas mehānismu, pietiek ar fosfātu grupas pievienošanu glikozei un pārvērst to par glikozes-6-fosfātu. Glikozes pārvēršanu par glikozes-6-fosfātu izraisa insulīns. Aknās glikozes-6-fosfātu izmanto glikolīzē, pentozes fosfāta šuntā, glikogēna sintēzē un heksozamīna sintēzē. Muskuļos un taukaudos heksosamīna sintēze ir ceļš, pa kuru glikoze ietekmē gēnu ekspresiju. Ar insulīna starpniecību glikoze ietekmē arī lipīdu metabolisma un holesterīna transportēšanas regulēšanu aknās.
Hepatocītos FA un TG sintēzi un holesterīna transportu regulē ar sterīnu reaģējošu elementu saistošo proteīnu (SREBP-1c). Šis proteīns ir galvenais gēnu transkripcijas aktivators, kura darbību kontrolē insulīns.
Tādējādi insulīna galvenā darbība ir vērsta ne tik daudz uz glikozes uztveršanu un tās līmeņa uzturēšanu asinīs, bet gan uz taukskābju, triglicerīdu un glikogēna sintēzi no glikozes, t.i. un par enerģijas substrātu patēriņa regulēšanu un to nogulsnēšanos.
PPAR saimes faktori ir iesaistīti arī FA un holesterīna transportēšanas ceļu kontrolē gēnu transkripcijas līmenī. PPAR-α galvenokārt tiek ekspresēts aknās. Šeit tas kontrolē dažādus gēnus, kas saistīti ar FA, TG un holesterīna metabolismu. Ir pierādīta zivju eļļas īpašība samazināt TG veidošanos aknās. Tas ir saistīts ar polinepiesātināto FA ietekmi uz PPRA-α. Tas tiek aktivizēts, saistoties ar skābju oksidētajiem metabolītiem 20:5 un 22:6 (šīs skābes ir atrodamas zivju eļļa). Šo skābju oksidācijas produkti peroksisomās ir paši LPO jeb brīvo radikāļu produkti. Šķiet, ka brīvie radikāļi ir būtiski, lai regulētu endogēno FA izplatību organismā. PPAR saimes receptori izpaužas galvenokārt aknās un taukaudos, un mazākā mērā citos orgānos. To ekspresija citos orgānos palielinās, ja tajos tiek novērota TG uzkrāšanās, t.i. kad notiek taukaudu deģenerācija.
PPAR-α darbojas sinerģiski ar LXR. LXR ir kodolreceptors, kas kontrolē lipīdu homeostāzi mugurkaulniekiem. PPAR-α un LXR ir visvairāk pētītie hepatocītu kodolreceptori. LXR endogēnie aktivatori ir oksisterīni (oksiholesterīns) un holesterīna biosintēzes ceļu starpprodukti. Šīs ģimenes receptori regulē daudzu gēnu ekspresiju, kas iesaistīti holesterīna sekrēcijas, transportēšanas un izdalīšanās procesos. Turklāt tie ir iesaistīti vispārējā TG sintēzes un FA homeostāzes kontrolē.
Galvenais gēns, ko kontrolē LXR, ir gēns, kas kodē SREBP-1c. SREBP-1c savukārt kontrolē gēnus, kas kodē holesterīna biosintēzes enzīmus un lipoģenēzes enzīmus: acetil-CoA karboksilāzi, FA sintāzi, acetil-CoA sintetāzi, glicerīna-3-fosfāta aciltransferāzi, tas aktivizē stearoil-CoA desaturāzi-CoA desaturāzi. enzīms, kas katalizē stearīnskābes pārvēršanu oleīnskābē makrofāgos un adipocītos.
Taukskābju fizioloģiskās īpašības. Glikozes, FA un holesterīna vielmaiņas ceļi ir cieši saistīti, tāpēc to transportēšanas, patēriņa, uzglabāšanas un sintēzes regulēšanā ir iesaistīti praktiski tie paši hormoni un faktori. Tomēr šie savienojumi paši ir aktīvi gēnu ekspresijas regulatori.
Šobrīd valda izpratne, ka asins taukskābju līmenim un sastāvam ir izšķiroša nozīme augšanā un attīstībā, enerģijas homeostāzes uzturēšanā un novecošanās procesā. FA, kas veido PL, ir šūnu membrānu sastāvdaļas un ir iesaistītas ar membrānu saistīto proteīnu aktivitātes regulēšanā un signālu pārraidē uz šūnu un no tās. šūnas kodols. Polinepiesātinātie FA un to oksidācijas produkti, piemēram, kalpo kā ligandi kodolreceptoriem PPAR un LXR. Piesātinātie FA, mijiedarbojoties ar aizkuņģa dziedzera β-šūnām, palielina insulīna sekrēciju. Tajā pašā laikā piesātinātās taukskābes, galvenokārt palmitīnskābe, ir aktīvi apoptozes induktori. Šo palmitīnskābes efektu neitralizē oleīnskābe.
Taukaudi satur un izdala oleīnskābi lielos daudzumos. Oleīnskābes īpašība padarīt lipīdu kristālus “šķidrākus” tiek izmantota EK uzkrāšanās laikā makrofāgos un TG taukaudos, mainoties plazmas membrānas viskozitātei, kas ietekmē daudzu ar membrānu saistīto proteīnu un receptoru aktivitāti. .
FA viegli iekļūst plazmas membrānā. Bet to transportēšanai caur mitohondriju dubulto membrānu ir nepieciešams īpašs proteīns karnitīns. Šī proteīna aktivitāti regulē leptīns, ko izdala taukaudi, t.i. taukaudi kontrolē taukskābju β-oksidāciju. Ar leptīna rezistenci FA tiek pakļauti ekstramitohondriju oksidācijai, īpaši peroksisomās. Tas noved pie lipīdu peroksidācijas (LPO) produktu vai brīvo radikāļu veidošanās. LPO uzkrāšanās šūnās nav saistīta ar mitohondriju integritātes iznīcināšanu, bet ir intracelulāras TG uzkrāšanās sekas.
Brīvie FA ir aktīvi mazgāšanas līdzekļi, tāpēc tie tiek transportēti asinsritē, saistīti ar albumīnu. Albumīnam ir vislielākā afinitāte pret oleīnskābi. Albumīna-oleīnskābes komplekss inducē TG veidošanos aknās un to izdalīšanos asinsritē, t.i., oleīnskābe ir iesaistīta brīvo taukskābju līmeņa kontrolē asinīs. Brīvo taukskābju līmeni asinīs kontrolē arī asins lipolītisko enzīmu (LPL un aknu lipāzes) un aknu (HCL), insulīna, augšanas hormona un leptīna aktivitāte. Nesen lipāzes ir atklātas dažādu audu šūnās.
Insulīns un augšanas hormons veido antagonistu faktoru pāri. Taukaudos insulīns kontrolē glikogēna sintēzi un lipoģenēzi, t.i. enerģijas uzkrāšana, un augšanas hormona kontrolē notiek TG lipolīze un nogulsnēto FA izdalīšanās asinīs, t.i. enerģijas patēriņš. Tajā pašā laikā leptīna sekrēcija ir atkarīga no insulīna, kas izraisa taukskābju uzsūkšanos šūnās un to sadegšanu mitohondrijās. FA enerģija ir nepieciešama izaugsmei un attīstībai, t.i. šūnu proliferācijai. Tajā pašā laikā ar piesātināto FA pārpalikumu asinīs palielinās apoptoze. Holesterīns, no kura tiek sintezētas žultsskābes, veicina eksogēno taukskābju iekļūšanu organismā. Holesterīna transports tiek organizēts tā, lai apvienotu enerģijas plūsmu un reproduktīvo funkciju. Reproduktīvās funkcijas pasliktināšanās izraisa taukskābju sadales traucējumus.
Brīvo FA līmenim asinsritē ir liela fizioloģiska nozīme: tā palielināšanās izraisa FA uzkrāšanos beztauku audos, rezistenci pret insulīnu un leptīnu, kas patoloģiskos apstākļos izraisa organisma nāvi, bet fizioloģiskos apstākļos. ir galvenais novecošanās cēlonis.
Tā kā FA vielmaiņa ir cieši saistīta ar holesterīna un glikozes metabolismu, sistēmisko izmaiņu cēloņi ir jāmeklē ar vecumu saistītās FA sadalījuma izmaiņās. vielmaiņas traucējumi pamata patoloģijas, piemēram, insulīna rezistence, hiperglikēmija, 2. tipa cukura diabēts, hipertensija un ateroskleroze, t.i. slimības, kas visbiežāk sastopamas gados vecākiem un seniliem cilvēkiem.
2. Enerģijas vielmaiņas īpatnības novecošanas laikā
Ontoģenēzes laikā organismā notiek nepārtraukta tauku uzkrāšanās, kas organismā pakāpeniski “izspiež” ūdeni. Tauki organismā nogulsnējas arvien pieaugošos daudzumos, sākot ar agrīnu ontoģenēzi, kas norāda uz organismā nonākošās enerģijas izmantošanas efektivitātes pakāpi – šī enerģija netiek pilnībā patērēta.
Ar vecumu saistītas izmaiņas taukaudi un galvenās vecāka gadagājuma patoloģijas. Kopumā galvenajiem ontoģenēzes posmiem ir šādas īpašības. Zīdaiņa vecumā cilvēka enerģijas avoti ir cukuri (laktoze, glikoze) un īsās ķēdes taukskābes (piena tauki), no kurām organismā tiek sintezētas endogēnās taukskābes. Piens ir tauku emulsija, tāpēc, lai absorbētu taukus zarnās, tam nav nepieciešams liels daudzums žults. Bērns sāk lietot eksogēnās palmitīnskābes un stearīnskābes, kad ir pilnībā izveidots žults sintēzes mehānisms. Žults sintēze ietver holesterīna izplatīšanas ceļu veidošanos organismā. Eksogēno tauku pieplūdums nodrošina organismam papildu enerģiju, kas nepieciešama galvenokārt reproduktīvās funkcijas veikšanai. Caur SRB1 ABL holesterīns nonāk aknās žultsskābju sintēzei un steroidogēnos audos dzimumhormonu sintēzei – tas rada apstākļus reprodukcijai. Lielākā daļa holesterīna tiek pārnesta uz aknām ar ZBL, un ABL ir tikai papildu avots. Šis papildinājums ir nepieciešams, lai uzlabotu eksogēno tauku plūsmu. Holesterīna piegādi aknām regulē estrogēni, kas norāda uz nepieciešamību pēc papildu enerģijas piegādes sievietes ķermenim. Vīriešiem holesterīna ieplūšanu aknās daļēji regulē fakts, ka izveidojušos ZBL pārpalikums tiek “izgāzts” “attīrītāju” makrofāgos. Atšķirīgā holesterīna intensitāte, kas ieplūst aknās vīriešiem un sievietēm, acīmredzot izskaidro biežāku žultspūšļa holesterozes biežumu pusmūžā sievietēm un artēriju sieniņu holesterozi, ko izraisa pārmērīga EK nogulsnēšanās uztvērēju makrofāgos vīriešiem. Šādu patoloģiju parādīšanās pusmūžā norāda uz klīnisku izpausmi ar vecumu saistīti traucējumi enerģijas metabolisms, ko izraisa pakāpeniska neizmantoto taukskābju uzkrāšanās organismā. Šajā vecumā holesterīna sadalījuma traucējumi ir izteiktāki. Asinsritē palielinās ZBL holesterīna saturs, ko modificē oksidācijas sistēma un aktīvi uztver “savācēju” makrofāgi. Šajā vecumā ir grūti nodalīt ģenētisko noslieci uz aterosklerozi no ar vecumu saistītiem enerģijas metabolisma traucējumiem. Nevar izslēgt, ka ar vecumu saistīta reproduktīvās funkcijas samazināšanās izraisa holesterīna iekļūšanas intensitātes samazināšanos steroidogēnos audos un tā plūsmas palielināšanos makrofāgos un aknās, kas pārsniedz fizioloģisko normu. Organisms pielāgojas jaunajam stāvoklim, samazinot apoproteīna A-1 veidošanos, ABL veidošanos un EK sintēzi. Nāves gadījumi ko izraisa ateroskleroze pusmūžā, ir nepielāgošanās sekas.
Tuvojoties reproduktīvā perioda beigām, tauku noliktavas izmērs sasniedz maksimālo vērtību, un tad taukaudu masa sāk samazināties. Pēc 75 gadiem šis process pastiprinās. Tauku daudzuma samazināšanās fizioloģiskajos depo ir saistīta ar to uzkrāšanos beztauku audos - in kaulu smadzenes, aizkrūts dziedzeris, aknas, muskuļi utt., notiek mezenhimālo šūnu taukainā deģenerācija. Tāpēc kopējais tauku daudzums organismā vai nu nemainās, vai pat palielinās.
Neskatoties uz taukaudu masas zudumu pēcreproduktīvā vecumā, jaunizveidoto šūnu skaits šajos audos nemainās. Šūnu diferenciācija tiek pabeigta, kad tās zaudē spēju vairoties un iegūst tauku uzglabāšanas un mobilizācijas funkciju, reaģējot uz insulīna, kateholamīnu un citu hormonu iedarbību un izdalot dažādus specifiskus faktorus. Preadipocīti taukaudos atrodas visas cilvēka dzīves garumā, t.i. tas nezaudē savu spēju atjaunot šūnas pat organismam novecojot. Tauku depo lieluma samazināšanās līdz ar vecumu nav saistīta ar šūnu zudumu, bet gan ar adipocītu izmēra samazināšanos un tā spēju uzkrāties TG samazināšanos. Transkripcijas faktori, kas regulē par TG uzkrāšanos atbildīgo gēnu ekspresiju, vienlaikus kontrolē preadipocītu pārvēršanas procesu nobriedusi šūna, bet novecojoša organisma preadipocītos nav pilna šo faktoru kopuma. Preadipocītu diferenciācija adipocītos novecojošā organismā apstājas noteiktā stadijā. Preadipocītu diferenciāciju stimulē glikokortikoīdi, insulīns, citi hormoni, parakrīnie un autokrīnie faktori. Signāla transdukcijas mehānisms izraisa gēnu ekspresiju, kas ir atbildīgi par nobrieduša adipocītu fenotipa veidošanos. Diferenciācijas laikā notiek kodolreceptora PPAR-γ ekspresija. Šis receptors ir nepieciešams, lai saglabātu tauku šūnu fenotipu un saglabātu tā jutību pret insulīnu. Ja šī un citu faktoru nav, glikozes tolerance ir traucēta. Nepietiekama preadipocītu diferenciācija ir daļa no adaptācijas mehānisma, kas novērš turpmāku TG uzkrāšanos adipocītos.
Adaptācijas mehānisms ietver insulīna rezistences veidošanos taukaudos, kas veicina lieko tauku “izdalīšanu”, jo insulīns vairs neinhibē HSL un nekas netraucē lipolīzi. FA no taukaudiem sāk nepārtraukti iekļūt asinīs, kā rezultātā samazinās tauku rezerves tauku depo. IN normāli apstākļi liekā TG izdalīšanās noved pie IR funkcijas atjaunošanas. Ar novecošanos situācija ir citādāka: IR jutība netiek atjaunota un taukaudu masas zudums notiek vienmērīgi. FA, kas izdalās no taukaudiem, sāk uzkrāties mezenhimālajās šūnās. TG uzkrāšanās palielināšanās ne-tauku audos veicina transkripcijas faktoru aktivitātes palielināšanos šajās šūnās, kas nosaka adipocītu fenotipu. Ar vecumu saistītā mezenhimālo šūnu diferenciācija veicina to transformāciju dipocītiem līdzīgās šūnās. Bet tajā pašā laikā tiek saglabāta šūnu īpašā funkcija.
Galvenais iemesls pakāpeniskai taukaudu proliferācijai ontoģenēzes laikā ir leptīna rezistences izraisīti taukskābju sadalījuma traucējumi. Leptīns ir normāli funkcionējošu taukaudu produkts. Tas aktivizē AMP aktivēto proteīnkināzi, kas stimulē FA β-oksidāciju visu šūnu mitohondrijās. Ar leptīna rezistenci šūna pārstāj izmantot FA. Veidojas šī enerģētiskā substrāta “pārpalikums”, paaugstinās brīvo taukskābju līmenis asinīs. Reakcija uz brīvo taukskābju līmeņa paaugstināšanos asinīs ir lipolīzes pārtraukšana taukaudos, un TG sāk uzkrāties adipocītos pieaugošā daudzumā. Taukaudu proliferācija izraisa insulīna rezistenci, HSL aktivāciju un nepārtrauktu atbrīvoto taukskābju plūsmu asinīs. Brīvo taukskābju līmenis asinīs atkal palielinās, bet tagad tās uzkrājas beztauku audos. Pēcreproduktīvā vecumā tauku zudums no zemādas taukaudiem notiek ātrāk, t.i. no tauku depo, kas apgādā skeleta muskuļus ar enerģijas substrātu. Viscerālo/zemādas taukaudu attiecība mainās līdz ar vecumu par labu intraperitoneālajiem taukiem, t.i. FA plūsma aknās kļūst dominējoša. Palielinās hepatocītu TG sekrēcija, ko satur VLDL, un attīstās trigliceridēmija.
Novecojošā organismā veidojas situācija, kas raksturīga enerģijas substrāta pārpalikumam. Kādu procesu rezultātā vesela cilvēka organismā veidojas liekie enerģijas substrāti? Neizbēgamais enerģijas pārpalikums, kas rodas tās nepietiekamības dēļ, sākotnēji uzkrājas piesātinātu FA veidā dabiskos “šķidros” kristālos - plazmas šūnu lipīdu divslānī. Mainās plazmas membrānas īpašība, piemēram, viskozitāte, kas lielā mērā ir atkarīga no holesterīna satura: holesterīns, kas padara lipīdu divslāņu blīvāku. Holesterīnam ir augsta afinitāte pret piesātinātajām taukskābēm, tāpēc to proporcijas palielināšanās membrānas lipīdos veicina membrānas piesātinājumu ar holesterīnu.
Leptīna rezistence nozīmē, ka šūna pārstāj reaģēt uz ārējo faktoru stimulāciju, tā zaudē jutību pret ārējiem stimuliem, t.i. tiek traucēta transmembrāna signalizācija. Joprojām tiek pētīta plazmas membrānas fizikāli ķīmisko īpašību ietekme uz šūnu jutību pret insulīnu un leptīnu. Tomēr ir konstatēts, ka, piemēram, SRB1 receptors reaģē uz plazmas membrānas lipīdu sastāvu. Steroidogēnos audos un aknās ar vecumu saistītas izmaiņas membrānas struktūrā samazina SRB1 efektivitāti. Samazinās dzimumhormonu ražošana, kas noved pie pakāpeniskas reproduktīvās funkcijas zuduma, un palielinās EK plūsma makrofāgos un aknās caur ZBL receptoriem. Holesterozes seksuālā diferenciācija, kas izteikta šī procesa sākumposmā, izzūd, samazinoties dzimumhormonu sintēzei. Pēcreproduktīvā vecumā žultspūšļa holesterozes un asinsvadu sieniņu holesterozes sastopamība vīriešiem un sievietēm pakāpeniski izlīdzinās.
Miocītus raksturo vismazākā jutība pret insulīnu. Insulīna rezistence palielinās vienlaikus ar leptīna rezistenci. Saglabājot mitohondriju funkcionālo integritāti, samazinās FA β-oksidācija miocītos. FA patēriņa samazināšanās miocītos un citās šūnās izraisa stabilu brīvo FA līmeņa paaugstināšanos asinīs. Taukaudu proliferācija notiek pēc reproduktīvo spēju zuduma un sasniedz maksimumu reproduktīvā perioda beigās. Līdz tam laikam attīstās adaptīvā reakcija – rodas insulīna rezistence un sākas nepārtraukta lipolīze taukaudos. Zemādas taukaudu, kas ir jutīgāki pret insulīna darbību, samazināšanās notiek agrāk nekā viscerālo tauku depo masas samazināšanās. Jutība pret insulīnu taukaudos netiek atjaunota adipocītu diferenciācijas adaptīvo traucējumu dēļ. Pieaugošā daudzumā tauki tiek nogulsnēti beztauku audos.
Tādējādi enerģija, kas iepriekš tika izmantota reprodukcijai un fiziskais darbs, uzkrājas piesātināto taukskābju veidā mezenhimālajās šūnās. Šajās šūnās veidojas blīvu, nemetabolizējamo tauku uzkrājumi, jo enzīma stearoildesaturāzes augstā aktivitāte, kas novērš TG uzkrāšanās sablīvēšanos, ir raksturīga tikai tām šūnām, kuras ir fizioloģiski paredzētas lipīdu uzkrāšanai - adipocītiem un makrofāgiem. . Ne tikai plazmas membrānas, bet arī audi kopumā tagad ir bagātināti ar piesātinātajām taukskābēm un holesterīnu.
Mezenhimālajām šūnām nav tauku mobilizācijas sistēmas, reaģējot uz hormonu stimulāciju, un tās nevar noņemt tauku uzkrāšanos ārpusšūnu telpā. Lai kaut kā atbrīvotos no liekās kravas, šūna aktivizē ekstramitohondriālās FA oksidācijas sistēmu. Bet šis nefizioloģiskais substrāta pārpalikuma pārstrādes veids noved pie oksidētu starpproduktu un mazgāšanas līdzekļu uzkrāšanās. Lipotoksicitātes draudi ir pāri beztauku šūnām. Lipīdu oksidācijas produktu (LPO) uzkrāšanās beztauku audos kalpoja par pamatu novecošanās brīvo radikāļu teorijas radīšanai. Faktiski LPO ir neizbēgamas sekas TG uzkrāšanai ne-taukaudos. To koncentrācija audos var kalpot kā indikators nevēlama substrāta oksidācijas procesa intensitātei vai lipotoksicitātes pakāpei. Lipotoksicitāte palielina apoptozi un veicina funkcionālas audu mazspējas progresēšanu. TG uzkrāšanās ne-taukaudos izraisa iekaisuma procesa attīstību. Piemēram, reaģējot uz EK uzkrāšanos asinsvadu sieniņās, palielinās C-reaktīvā proteīna ražošana.
Izvairīties nevēlamas sekas piespiedu intracelulāra TG uzkrāšanās, diferencējošās šūnas šajos audos iegūst adipocītu pazīmes, tās pat izskatās pēc adipocītiem. Tomēr nespēja izteikt visu nepieciešamo transkripcijas faktoru kompleksu mezenhimālās šūnas diferenciācijas laikā padara tās fenotipu līdzīgu adipocītiem. Šīs šūnas ir maza izmēra, tām ir samazināta jutība pret insulīnu un palielināta citokīnu sekrēcija. Mezenhimālās šūnas ar adipocītiem līdzīgu fenotipu ražo dažādus citokīnus, kas izraisa šūnu diferenciāciju, kas palielina taukaudu deģenerācijas laukumu.
Tātad tā organismā nonākošās enerģijas daļa, kas netiek izmantota šūnu proliferācijas (augšanas un attīstības), fizisko aktivitāšu laikā, reproduktīvā potenciāla realizācijas laikā, tiek tērēta endogēno FA sintēzei, kas veido nemetabolizējamo uzkrājumus. tauki netaukaudos, t.i. lipīdu kristālu elementu sintēzei. Holesterozi var uzskatīt par brīvā holesterīna un holesterīna intracelulāru un ārpusšūnu kristālu veidošanos.
Nepieprasītu enerģijas substrātu pārpalikums, kas palielinās cilvēka dzīves laikā, vēlīnā ontoģenēzē noved pie žultspūšļa holesterozes (holecistīta) un asinsvadu sieniņu (ar vecumu saistītas aterosklerozes), insulīna rezistences, hiperglikēmijas un no insulīna neatkarīgas attīstības. tipa cukura diabēts, hipertensija un neirodeģeneratīvas slimības.
Ar vecumu saistīta dislipidēmija. Vispārīgākais rādītājs, kas liecina par asins lipīdu un lipoproteīnu spektra izmaiņām vecāka gadagājuma grupā, ir kopējā PL, ABL-H un apoproteīna A-1 satura samazināšanās. Ar vecumu saistītais ABL satura samazinājums ir holesterīna kā steroīdu hormonu sintēzes substrāta pieprasījuma trūkuma sekas. Rezultātā mainās žults īpašības, attīstās žultspūšļa holesteroze, tiek traucēta eksogēno tauku uzsūkšanās. Tādā veidā ķermenis ierobežo enerģijas piegādi, kas tiek izmantota reproduktīvās funkcijas veikšanai. ABL ir dabiski holesterīna sorbenti, kas ir pakļauti makrofāgu membrānai un EK sintēzes vietai. Pavājināta ABL funkcija veicina izmainīta, ļoti aterogēna ZBL parādīšanos asinīs un EK uzkrāšanos makrofāgos. Turklāt ABL kā galvenais PL transportētājs asinīs veicina šūnu bojājumu atjaunošanos, un stabils šo lipoproteīnu deficīts padara audu iznīcināšanas procesu neatgriezenisku. Pamatīgs PL līmeņa un ABL daļiņu skaita samazinājums ir raksturīgs neirodeģeneratīvām slimībām vecumdienās, īpaši Alcheimera slimībai.
Vecākajā vecumā vecuma grupa ABL-C samazināšanās un ZBL-H līmeņa paaugstināšanās notiek uz TG satura palielināšanās fona. Šāda veida dislipidēmija ir raksturīga insulīna rezistencei, kas novērota metaboliskā sindroma gadījumā, patoloģisks stāvoklis, ko izraisa pārmērīga enerģijas substrātu uzņemšana. TG saturs, kā likums, nepārsniedz augšējā robeža norma (200 mg/dl), bet tikai tai tuvojas. Pašlaik TG līmenis ≥150 mg/dl tiek uzskatīts par metaboliskā sindroma riska faktoru.
Kopumā vecākajai vecuma grupai raksturīgs tas pats patoloģiju komplekss, kas tiek novērots metaboliskā sindroma gadījumā - dislipidēmija, insulīna rezistence, glikozes tolerance, hipertensija, iekaisumi. Izņēmums ir aptaukošanās. Aptaukošanās attīstās neizmantoto enerģijas substrātu uzkrāšanās rezultātā taukaudos. Šis pārpalikums rodas, ja rodas disbalanss starp glikozes un eksogēno taukskābju daudzumu, kas organismā nonāk ar pārtiku, un to patēriņu, tostarp β-oksidācijas laikā skeleta muskuļos. Zemādas / viscerālo taukaudu attiecība aptaukošanās gadījumā mainās par labu viscerālajiem taukiem. Vēdera aptaukošanās ir galvenais metaboliskā sindroma riska faktors. Organismam novecojot, viscerālo taukaudu pakāpeniska dominēšana kopējā taukaudu masā ir riska faktors vecāka gadagājuma galvenajām patoloģijām.
Nav grūti saskatīt līdzības starp faktoriem, kas ir metaboliskā sindroma pamatā, un ar vecumu saistītām patoloģijām. Šiem diviem procesiem kopīgs ir neizlietotās enerģijas substrātu uzkrāšanās.
Metaboliskais sindroms. Kā parādīts iepriekš, holesterīna, FA (TG un brīvā FA formā) un glikozes vielmaiņas ceļi ir saistīti vienā sistēmā, kas apvieno ogļhidrātu un lipīdu metabolismu kopējā enerģijas substrātu apmaiņā. Šobrīd notiek pētnieku uzmanības pārorientācija no individuālas patoloģijas uz sistēmiskiem traucējumiem, kuru pamatā ir tāda paša veida vielmaiņas izmaiņas. Slimības, kas raksturīgākās vecāka gadagājuma cilvēkiem un senilajam vecumam, izraisa organisma darbības traucējumi kā vienota sistēma. Sakarā ar to, ka pastāv daudz līdzību starp ar vecumu saistītu patoloģiju faktoriem un metaboliskā sindroma riska faktoriem, ir nepieciešams sīkāk apsvērt šī sistēmiskā traucējuma raksturīgās pazīmes.
Metaboliskais sindroms mūsdienās tiek pētīts visintensīvāk. Tas apvieno izmaiņas glikozes (insulīna rezistences/hiperinsulinēmijas/2. tipa cukura diabēta) un lipīdu (dislipidēmijas) sadalījumā, t.i. izmaiņas iekšā kopējā sistēma enerģijas substrātu sadale. Šīs izmaiņas pavada tādi apstākļi kā aptaukošanās, hipertensija un ateroskleroze. Metaboliskais sindroms ir saistīts ar paaugstinātu sirds un asinsvadu slimību attīstības risku. Galvenais nāves cēlonis metaboliskā sindroma gadījumā ir kardiovaskulāras komplikācijas - infarkts, insults, savukārt attīstās dažādu asinsvadu gultņu asinsvadu aterosklerozes bojājumi. Citi sindromā novērotie faktori ir fibrinogēnija, zems līmenis audu plazminogēna aktivators, nefropātija, mikroalbuminūrija u.c.
Ogļhidrātu un lipīdu metabolisma traucējumiem metaboliskā sindroma gadījumā ir skaidri noteiktas pazīmes - insulīna rezistence (agrīnā stadijā) un hiperglikēmija (vēlīnā stadijā), kā arī noteikta veida dislipidēmija. Sākumā jutība pret insulīnu gandrīz pilnībā tiek zaudēta skeleta muskuļos, bet saglabājas taukaudos un aknās. Dislipidēmiju metaboliskā sindroma gadījumā raksturo šādi rādītāji:
TG līmeņa paaugstināšanās asins plazmā;
ABL līmeņa pazemināšanās (mazo daļiņu frakcijas izplatība);
EK satura samazināšanās ABL;
Maza blīva (ļoti aterogēna) ZBL daudzuma palielināšanās;
Brīvo taukskābju satura palielināšanās asins plazmā.
Ir viegli saprast, ka metaboliskajam sindromam raksturīgas tādas pašas lipīdu un lipoproteīnu satura izmaiņas kā enerģijas substrātu sadalījuma izmaiņām novecojošā organismā.
Tiek uzskatīts, ka brīvo taukskābju satura palielināšanās asins plazmā ir raksturīgākais rādītājs aptaukošanās, insulīna rezistences un 2. tipa cukura diabēta diagnostikā. Turklāt šobrīd paaugstināts brīvo taukskābju līmenis asinīs tiek uzskatīts par galveno metaboliskā sindroma attīstības cēloni.
Brīvo taukskābju koncentrācija plazmā atspoguļo līdzsvaru starp to veidošanos (lipoģenēze, intravaskulāra TG hidrolīze un taukskābju izdalīšanās no taukaudiem) un patēriņu (jo īpaši β-oksidācija skeleta un sirds muskuļos).
Insulīna rezistence galvenokārt rodas skeleta muskuļos. Šajos audos sāk veidoties TG uzkrājumi, kas ir pilnīgi neparasti miocītiem. Iemesls TG uzkrāšanai skeleta muskuļos ir pārmērīgs piesātināto FA pieplūdums miocītos, jo palielinās brīvo FA līmenis asinīs. Veseliem jauniem un pusmūža cilvēkiem brīvo FA līmeņa paaugstināšanās notiek, jo palielinās eksogēno FA vai FA pieplūdums, kas sintezēts aknās ar lieko glikozi uzturā. Ja šūnās ir pārmērīgs TG daudzums un ārpusšūnu telpā FA, IR funkcija tiek “izslēgta”.
Pateicoties lipofilitātei, brīvie FA pasīvi iekļūst šūnā, taču nesen tika pierādīts, ka šis process tiek aktivizēts caur CD36 receptoru. Šis receptors lielos daudzumos ir atrodams taukaudos, sirds un skeleta muskuļos, un tā praktiski nav aknās un nierēs. CD36 deficīts ir saistīts ar ievērojamiem FA transporta traucējumiem un insulīna rezistences attīstību. CD36 satura samazināšanās membrānā var būt saistīta ar tās viskozitātes īpašību izmaiņām. Ar augstu CD36 ekspresiju muskuļos samazinās taukaudu apjoms, VLDL un brīvo taukskābju līmenis asinīs.
Zemādas taukaudi, kas novirza taukskābes uz skeleta muskuļiem, samazina taukskābju sekrēciju, TG uzkrājas adipocītos, taukaudi proliferējas. Tas noved pie insulīna rezistences attīstības pašos taukaudos. FA sekrēcija asinīs kļūst nepārtraukta, un paaugstināts brīvā FA līmenis asinīs stabilizējas. Taukskābju pārpalikums sāk uzkrāties beztauku audos. HSL aktivitātes uzturēšana un nepārtraukta lipolīze palīdz taukaudiem “atbrīvoties” no liekā slodzes, un šajā orgānā tiek atjaunota jutība pret insulīnu.
Viscerālo taukaudu šūnas ir jutīgākas pret kateholamīnu lipolītisko iedarbību un izturīgākas pret insulīna iedarbību nekā zemādas taukaudu šūnas. Tāpēc, neskatoties uz lipoģenēzes intensitātes samazināšanos zemādas taukaudos, viscerālie audi turpina izmantot glikozi TG sintēzei. Pakāpeniski augot un dominējot viscerālajiem audiem, galvenā taukskābju plūsma plūst uz aknām. Neskatoties uz to, ka viscerālie tauki veido tikai 6% no kopējās taukaudu masas sievietēm un 20% vīriešiem, aknas saņem 80% no visām asinīm no vārtu vēnas, kur izdalās viscerālās taukskābes. Ar metabolisko sindromu palielinās viscerālo taukaudu īpatsvars, kas izraisa androgīna ķermeņa tipa parādīšanos.
Aknas reaģē uz palielinātu FA pieplūdumu, palielinot izdalītā TG līmeni. Attīstās trigliceridēmija. Ja FA pārpalikums aknās ir pietiekami liels, TG sāk uzkrāties hepatocītos. FA plūsmas normalizēšana aknās palīdz atjaunot IR jutīgumu skeleta muskuļos. Tomēr hroniska pārēšanās un mazkustīgs dzīvesveids padara insulīna rezistenci hronisku un veicina pilnīgu metaboliskā sindroma attīstību.
Citi faktori, kas veicina metaboliskā sindroma attīstību, papildus insulīna rezistencei, ir saistīti ar taukaudu kā endokrīnā orgāna disfunkciju. Metabolisko sindromu var uzskatīt arī par iekaisuma stāvokli. Piemēram, aknas ražo C-reaktīvo proteīnu (CRP), kas ir sistēmiska iekaisuma marķieris. Bija pozitīva korelācija starp aptaukošanās pakāpi (ķermeņa masas indeksu), CRP līmeni un kardiovaskulāriem riska faktoriem, piemēram, fibrinogēnu un ABL holesterīnu.CRP līmenis palielinās, reaģējot uz interleikīna-6 sekrēciju ar taukaudiem. Cilvēkiem ar aptaukošanos tiek aktivizēta TNF sistēma. TNF-α un interleikīna-6 sekrēcija palielinās, palielinoties taukaudu masai. Glikozes homeostāze un TNF sistēmas aktivitāte modulē leptīna sekrēciju. Leptīns izraisa interleikīna-1 izdalīšanos smadzeņu audos, ietekmējot proinflammatorisko citokīnu sekrēciju. Iekaisumam ir nozīme aterosklerozes patoģenēzē, kas savukārt tiek novērota cilvēkiem, kuri cieš no aptaukošanās, dislipidēmijas, diabēta un insulīna rezistences.
Lēnas darbības iekaisums var būt faktors hipertensijas attīstībā. Sistoliskā un diastoliskā asinsspiediena paaugstināšanās, pulsa piepildīšanās, arteriālais spiediens saistīta ar interleikīna-6 līmeni. Sievietēm šī korelācija ir izteiktāka. Vīriešiem tika novērota korelācija starp interleikīna-6 līmeni un insulīna līmeni tukšā dūšā. Tiek pieņemts, ka hipertensijas cēlonis metaboliskā sindroma gadījumā ir taukaudu disfunkcija.
Tādējādi insulīna rezistence taukaudos, nepārtraukta lipolīze un palielināta taukskābju izdalīšanās asinīs ar taukaudiem palielina to plūsmas intensitāti ne-taukaudos. Insulīna rezistenci pavada leptīna rezistence. Tas nozīmē, ka FA β-oksidācijas līmenis šūnās samazinās.
Tātad taukaudi reaģē ar insulīna rezistenci uz pārmērīgu glikozes un taukskābju pieplūdumu tajos. Taukskābju plūsma it kā tiek novirzīta uz citām depo, kas neizbēgami kļūst par beztauku audiem. Insulīna rezistence skeleta muskuļos un aknās ir arī reakcija uz enerģijas substrāta pārpalikumu. Lipoģenēzei skeleta muskuļos ir jāaktivizē funkcijas, kas nav raksturīgas miocītiem. Patiešām, ar TG uzkrāšanos skeleta muskuļos tiek novērota adipocītiem raksturīgu kodolreceptoru ekspresija, t.i. šūnas fenotips faktiski mainās. Nelīdzsvarotība starp enerģijas substrātu (glikozes un piesātināto taukskābju) uzņemšanu un to patēriņu pārēšanās un zema līmeņa uzturā fiziskā aktivitāte galu galā noved pie nemetabolizējamo tauku nogulsnēšanās taukaudos.
Tāpat kā ar novecošanos, hipertrigliceridēmiju metaboliskā sindroma gadījumā pavada ABL līmeņa pazemināšanās. Tajā pašā laikā samazinās uz makrofāgu membrānas pakļautā holesterīna sorbcija un EK sintēze, samazinās holesterīna plūsma steroidogēnos audos un aknās. Attīstās žultspūšļa un asinsvadu sieniņu holesteroze. Holesterīna plūsmas traucējumi aknās maina žults īpašības. Tāpat kā ar novecošanos, organisms cenšas samazināt eksogēno piesātināto taukskābju uzņemšanu. Bazolaterālās membrānas viskozo īpašību izmaiņu rezultātā tiek kavēta glikozes transportētāju Glut-2 un SGLT1 (no nātrija atkarīgā glikozes transportētāja) darbība zarnās, kas samazina glikozes uzņemšanu organismā.
Tādējādi metaboliskā sindroma un ar vecumu saistītās patoloģijas izplatītais cēlonis ir neizlietoto (“lieko”) enerģijas substrātu uzkrāšanās audos TG formā.
Starptautiskās Aterosklerozes biedrības speciālisti iesaka šādus rādītājus, lai noteiktu metaboliskā sindroma attīstības risku. Šie rādītāji tiek noteikti vīriešiem, kas vecāki par 45 gadiem, un sievietēm, kas vecāki par 55 gadiem:
Vēdera aptaukošanās;
50 mg/dl (1,3 mmol/l) sievietēm;
Asinsspiediens ≥ 130/85 mm Hg;
Glikoze tukšā dūšā ≥ 110 mg/dL (6,0 mM/L).
Vecuma grupā virs 65 gadiem aptaukošanās ir izslēgta. Turklāt jāņem vērā, ka ABL saturs vīriešiem un sievietēm šajā vecumā pakāpeniski izlīdzinās (kļūst vienlīdz zems).
ZBL saturs pašlaik ir izslēgts no šiem rādītājiem. Taču daudzi gados vecāki cilvēki piedzīvo pielāgošanos taukskābju sadales traucējumiem, kas izpaužas ar to, ka viņu TG līmenis nepārsniedz 100 mg/dl. Šai grupai raksturīgs ZBL satura pieaugums uz ABL satura samazināšanās fona, t.i. dominē holesterīna sadales traucējumi. Šāda vecāka gadagājuma cilvēku sadale divās grupās atbilstoši enerģijas vielmaiņas traucējumu veidam prasa diferencētu terapeitisko pieeju.
Ieteicamā literatūra
Brauns G., Dž. Vokens. Šķidrie kristāli un bioloģiskās struktūras//M. - Pasaule. – 1982. – 198. lpp.
Terešina E.V., N.N. Doroņina, O.P. Pleteņeva. Lipīdu vielmaiņa vecā un senīlā vecumā//Sest. "Pašreizējās gerontoloģijas problēmas." – M. – 1999. – P. 225-226.
Das U.N. Vai metaboliskais sindroms X ir iekaisuma stāvoklis?//Exp.Biol.Med. – 2002. – V. 227. – P. 989-997.
Febbraio M., D.F. Hajjars, R.L. Silveršteins. CD 36: B klases uztvērēja receptors, kas iesaistīts angioģenēzē, aterosklerozē, iekaisumos un lipīdu metabolismā//J.Clin.Invest. – 2001. – V. 108. – P. 785-791.
Freins K.N. Viscerālie tauki un insulīna rezistence: cēloņsakarība vai korelatīva?//Br.J.Nutr. – 2000. – V.83 (1.pielikums). – P. S71-S77.
Hanters S.J., W.T. Gārvijs. Insulīna darbība un insulīna rezistence: slimības, kas saistītas ar insulīna receptoru, signālu pārraides un glikozes transportēšanas efektoru sistēmas defektiem//Am.J.Med. – 1998. – V. 105. – P. 331-345.
Kirkland J.L., T. Tchkonia, T. Pirtskhalava, J. Han, I. Karagiannides. Adipoģenēze un novecošanās: vai novecošanās dēļ tauki kļūst traki?//Exp.Geront. – 2002. – V. 37. – P. 757-767.
Krīgers M. Scavenger receptoru B klases 1. tips ir daudzligandu ABL receptors, kas ietekmē dažādas fizioloģiskās sistēmas//J.Clin.Invest. - 2001. – V. 108. – P. 793-797.
Lūiss G.F., A. Karpentjē, K. Adeli, A. Džaka. Traucēta tauku uzglabāšana un mobilizācija insulīna rezistences un 2. tipa cukura diabēta patoģenēzē//Endocrine Rev. – 2002. – V. 23. – P. 201-229.
Lūiss G.F., G. Šteiners. Hipertrigliceridēmija un tās metaboliskās sekas kā aterosklerozes kardiovaskulāro slimību riska faktors insulīnneatkarīgā cukura diabēta gadījumā//Diadetes Metab.Rev. – 1996. – V. 12. – P. 37-56.
Zimmets P., E.J. Boiko, G.R. Koljē, M. de Kurtens. Metaboliskā sindroma etioloģija: insulīna rezistences, leptīna rezistences un citu dalībnieku iespējamā loma // Ann.N.Y.Acad.Sci. – 1999. – V. 892. – P. 25-44.
Difūzās izmaiņas aknās netiek ņemtas vērā atsevišķa slimība, to klātbūtne liecina tikai par orgānu parenhīmas proliferāciju, kas raksturīga daudziem patoloģiskiem stāvokļiem. Izmaiņas ir dažāda rakstura, visos gadījumos diagnozes apstiprināšanai tiek izmantota detalizēta izmeklēšana.
Klasifikācija
Atkarībā no smaguma pakāpes difūzās izmaiņas aknu parenhīmā var būt:
- Nenozīmīgs. Diagnosticēts diezgan bieži. Raksturīgs vīrusu vai baktēriju iekaisuma procesa sākuma stadijām un patoloģiskiem stāvokļiem, ko izraisa nelabvēlīgu faktoru iedarbība.
- Izteikts. To pavada orgāna pietūkums un palielināšanās. Raksturīgs hroniskam hepatītam, cirozei, cukura diabētam, smagai aptaukošanās pakāpei, primāriem un sekundāriem ļaundabīgiem audzējiem.
- Mērens. Mērenas difūzas izmaiņas attīstās uz ķermeņa intoksikācijas ar narkotikām, ilgstošas alkoholisko dzērienu un treknu pārtikas produktu lietošanas fona.
Pamatojoties uz izmaiņu raksturu aknu struktūrā, izšķir:
- Izkliedētas izmaiņas, piemēram, steatoze. Raksturīgs ar izkliedētu tauku ieslēgumu parādīšanās. Liela daudzuma tauku uzkrāšanās veicina veselīgu aknu šūnu iznīcināšanu, kam seko cistu veidošanās, kas maina orgāna struktūru. Izkliedētas fokusa izmaiņas aknās, piemēram, steatozi, var konstatēt gan gados vecākiem cilvēkiem, gan bērniem.
- Izmaiņas hepatozes veidā. Veseliem aknu audiem ir viendabīga struktūra, tajos ir asinsvadi un žultsvadi. Hepatozi raksturo lieko tauku uzkrāšanās orgānu šūnās. Veselīgi hepatocīti tiek pakāpeniski iznīcināti.
- Tauku infiltrācija. Aknas aktīvi piedalās barības vielu metabolismā. Pārtikas taukus zarnās sadala fermenti. Aknās iegūtās vielas pārvēršas holesterīnā, triglicerīdos un citos cilvēka organismam svarīgos savienojumos. Ceļā uz attīstību difūzās izmaiņas pēc tauku infiltrācijas veida audos uzkrājas liels daudzums triglicerīdu.

Atkarībā no iemesliem, kas veicināja orgāna struktūras izmaiņas, tam var būt šāda veida:
- pietūkums;
- sklerozes;
- hipertrofisks;
- distrofiski.
Cēloņi
Difūzās izmaiņas aknu audos ir simptoms tādām slimībām kā:

Aknu palielināšanās risks palielinās šādu faktoru dēļ:
- Slikts uzturs. Ēdot majonēzi, ātrās uzkodas, karstās mērces un pārstrādātus pārtikas produktus, aknām tiek radīts papildu stress, izraisot tās darbību avārijas režīmā.
- Alkohola pārmērīga lietošana. Etilspirts aknu enzīmu ietekmē sadalās aldehīdos, kas kaitīgi ietekmē hepatocītus. Regulāri lietojot alkoholu, audi sāk sadalīties, un tos pakāpeniski aizstāj ar tauku ieslēgumiem. Alkoholiskā hepatoze ar nepareiza ārstēšana pārvēršas par cirozi.
- Antibiotiku un dažu citu zāļu lietošana. Papildus terapeitiskajam efektam medikamentos esošajām aktīvajām vielām piemīt arī hepatotoksiska iedarbība. Tādēļ jebkuras zāles jālieto ārsta norādītajās devās.
- Dzīvošana nelabvēlīgā vides vidē. Toksiskās vielas, kas nonāk organismā, pa asinīm nonāk aknās, kur tās nogulsnējas un laika gaitā tiek neitralizētas. Tomēr laika gaitā orgāns pārstāj tikt galā ar šīm funkcijām, un rodas dažādas slimības. Riska grupā ietilpst cilvēki, kas dzīvo netālu no rūpnīcām, rūpnīcām un galvenajiem lielceļiem.
- Psihoemocionālā pārslodze. Stresa situācijās virsnieru dziedzeri sāk ražot adrenalīnu. Šis hormons, ko sadala aknas, ir bīstams tā audiem. Pastāvīgu stresu gandrīz vienmēr pavada hepatocītu bojājumi.
Slimības simptomi
Izkliedētu izmaiņu pazīmes aknās lielā mērā ir atkarīgas no cēloņa, kas veicināja to rašanos. Tomēr lielākajai daļai slimību ir līdzīgi simptomi, tie ir:
- Gremošanas traucējumi. Pacients sūdzas par sliktu dūšu, dedzināšanu, izkārnījumu krāsas maiņu un pastiprinātu vēlmi izkārnīties.
- Ādas stāvokļa pasliktināšanās. Patoloģiskas izmaiņas aknu struktūrā veicina ādas dzeltēšanu, pūtītes un papilomu parādīšanos. Bieži tiek novērotas alerģiskas reakcijas, stiprs nieze, pīlings un pietūkums.
- Plaisu un aplikuma parādīšanās uz mēles virsmas.
- Sāpju sindroms. Nepatīkamām sajūtām aknu patoloģiju dēļ ir atšķirīgs raksturs. Ar nelielām izmaiņām kreisajā daivā tiem raksturīgs vāji izteikts raksturs. Intensīvas sāpes parādās ar strutojošu iekaisuma procesi orgānu parenhīmā, traumās un ļaundabīgos audzējos.
- Pastiprināta svīšana. Kad aknu stāvoklis pasliktinās, sviedriem ir spēcīga, nepatīkama smaka.
- Rūgtums mutē. Visbiežāk tas parādās no rīta, kā arī pēc asu un treknu ēdienu ēšanas.
- Vispārējs vājums un paaugstināts nogurums. Pacients pamana, ka viņš sāk nogurt pat pēc nelielas fiziskas slodzes.
- Aizkaitināmība, garastāvokļa svārstības, galvassāpes.
- Paaugstināta ķermeņa temperatūra.
- Asinsvadu trauslums, kas veicina asiņošanas attīstību.

Diagnostikas pasākumi
Ultraskaņas diagnostika tiek uzskatīta par galveno aknu slimību noteikšanas metodi. Izmantojot ultraskaņu, tiek konstatētas difūzo izmaiņu atbalss pazīmes, tiek noteikts to raksturs un smagums. Procedūra neaizņem daudz laika. Ehoskopiskā izmeklēšanā tiek konstatētas anomālijas orgāna struktūrā, hepatīts, ciroze, primārie un sekundārie vēža perēkļi. Turklāt tiek veiktas šādas diagnostikas procedūras:
- Radionuklīdu skenēšana. Asinsrites sistēmā tiek ievadītas radioaktīvās vielas, kas caur asinsriti iekļūst aknu audos. Izmaiņas orgāna ehostruktūrā nosaka kontrasta sadalījuma raksturs. Šo metodi izmanto, lai diagnosticētu metastātiskus bojājumus un pēctraumatiskas izmaiņas audos.
- CT. Pētījums tiek izmantots, lai noteiktu parenhīmas asiņošanu, mazus audzējus un dažas citas izmaiņas.
- Smalkas adatas biopsija. Procedūras laikā iegūtais materiāls tiek nosūtīts histoloģiskai izmeklēšanai. To uzskata par palīgmetodi, ko izmanto, lai apstiprinātu vai atspēkotu iepriekš noteikto diagnozi.
- Asins analīze bioķīmijai. Ļauj novērtēt hepatocītu funkcionālo aktivitāti. Difūzu izmaiņu attīstība ir saistīta ar albumīna līmeņa pazemināšanos, ALAT un bilirubīna daudzuma palielināšanos.
- Antivielu pārbaude pret hepatīta vīrusu. Ļauj noteikt slimības veidu un infekcijas izraisītāja aktivitātes pakāpi.

Ārstēšana
Sarežģīta slimību ārstēšana, ko pavada patoloģiskās izmaiņas aknās, ietver medikamentu lietošanu, dzīvesveida maiņu un īpašas diētas ievērošanu. Narkotiku terapija ietver:
- Augu bāzes hepatoprotektori. Orgānu funkciju normalizēšanai izmanto piena sēnīšu preparātus (Karsil, Gepabene, Silymarin). Tie ir efektīvi pret hepatītu, cirozi, holecistītu un toksiskiem bojājumiem.
- Būtiski fosfolipīdi (Essentiale Forte, Phosphogliv, Essliver). Normalizē vielmaiņas procesus audos un paātrina to atjaunošanos.
- Dzīvnieku izcelsmes preparāti (Hepatosan, Sirepar). Ražots no liellopu aknu hidrolizātiem. Tiem piemīt aizsargājošas un attīrošas īpašības.
- Aminoskābes (Heptral, Heptor). Tiem piemīt izteikta detoksikācijas un antioksidanta iedarbība, aizsargā hepatocītus un paātrina to atveseļošanos.
- Pretvīrusu un imūnstimulējošas zāles. Virziens hepatīta vīrusu aktivitātes samazināšanai un organisma rezistences palielināšanai. Tiem ir liels blakusparādību skaits, tādēļ tās jālieto ārsta uzraudzībā.
Ieteicams ārstēt ar infūzijām ārstniecības augi: piena dadzis, pienenes un artišoka saknes, zemeņu lapas, kukurūzas zīds, mežrozīšu augi. Lai pagatavotu zāles 2 ēd.k. l. izejvielas, aplej ar 0,5 litriem verdoša ūdens, atstāj uz 3-4 stundām, filtrē un ņem pa 100 ml 3 reizes dienā.
Diēta
Atbilstība pareizas uztura principiem aknu audu difūzu izmaiņu klātbūtnē ir svarīga ārstēšanas sastāvdaļa. No tā ir atkarīga terapijas efektivitāte un ilgums. No uztura jāizslēdz:
- kafija un melnā tēja;
- tomāti un tomātu sula;
- alkohols;
- saldie gāzētie dzērieni;
- trekna gaļa;
- spēcīgi gaļas un sēņu buljoni;
- prosa, grūbas un miežu putra;
- taukainas mērces;
- kūpināta gaļa un desas;
- treknas zivis;
- saldie maizes izstrādājumi;
- taukskābju fermentēti piena produkti;
- marinēti un sālīti dārzeņi;
- pikanti dārzeņi;
- sēnes;
- pākšaugi;
- svaigi augļi un ogas;
- konditorejas izstrādājumi;
- šokolāde;
- garšvielas

Atļauto produktu sarakstā ir:
- dzērieni (mežrozīšu novārījums, vāja zaļā tēja, žāvētu augļu kompoti);
- rudzu vai kliju maize, cepumi, krekeri;
- liesa gaļa (vista, tītars, trusis, teļa gaļa);
- zema tauku satura zivis (līdaka, menca, zandarts);
- dārzeņi un sviests;
- piena produkti ar zemu tauku saturu;
- olas;
- vārīti un sautēti dārzeņi;
- griķu, auzu pārslu un rīsu putra;
- salāti ar neitrālu garšu;
- svaigi bulgāru pipari;
- makaroni;
- augļu ievārījums, marmelāde, medus.
Jums jāēd mazās porcijās, 5-6 reizes dienā. Ēdienu tvaicē, vāra vai cep. Zupas gatavo no gaļas, bet aspic – no zivīm. Ir atļauti nelieli daudzumi skābēti kāposti, skvoša kaviārs, vinegrets. Patērētā sāls daudzums ir ierobežots līdz 3 g dienā, cukuru aizstāj ar ksilītu.
Prognoze un profilakse
Palīdz novērst difūzās izmaiņas orgānā:
- savlaicīga vakcinācija pret vīrusu hepatītu;
- pacientu ar A hepatītu izolēšana;
- drošības noteikumu ievērošana bīstamās nozarēs, individuālo aizsardzības līdzekļu lietošana;
- svaigu produktu patēriņš, kas iegādāti no uzticamiem pārdevējiem;
- slikto ieradumu noraidīšana;
- aseptikas noteikumu ievērošana, veicot ķirurģiskas iejaukšanās, veicot injekcijas, veicot zobārstniecības procedūras;
- vienreizējās lietošanas medicīnas instrumentu lietošana;
- donoru asiņu daudzpakāpju pārbaude;
- atteikšanās no gadījuma intīmām attiecībām;
- pareiza uztura;
- regulāra pacientu ar hroniskām aknu patoloģijām izmeklēšana;
- nekontrolētas medikamentu lietošanas izslēgšana;
- profilaktiska hepatoprotektoru lietošana;
- nekavējoties konsultējieties ar ārstu, ja parādās aknu slimības simptomi;
- pareiza patoloģiju ārstēšana, kas var izraisīt aknu bojājumus.
Prognoze ir atkarīga no cēloņa, kas veicināja difūzo izmaiņu attīstību, slimības stadijas un formas. Kad audi mainās atbilstoši steatozes veidam, tiek sniegta prognoze savlaicīga ārstēšana izrādās labvēlīgs, tas pats attiecas uz hronisku persistējošu hepatītu. Nelabvēlīgs iznākums ir ciroze, kurā vidējais 5 gadu izdzīvošanas rādītājs nepārsniedz 50%.